Nanoshell
| Część serii artykułów na temat |
| nanomedycyny |
|---|
| Zobacz także |
Nanopowłoka , a raczej plazmon nanopowłoki , to rodzaj kulistej nanocząstki składającej się z dielektrycznego rdzenia, który jest pokryty cienką metaliczną powłoką (zwykle złotą ) . Te nanopowłoki obejmują kwazicząstkę zwaną plazmonem , która jest zbiorowym wzbudzeniem lub kwantową oscylacją plazmy, w której elektrony oscylują jednocześnie w odniesieniu do wszystkich jonów.
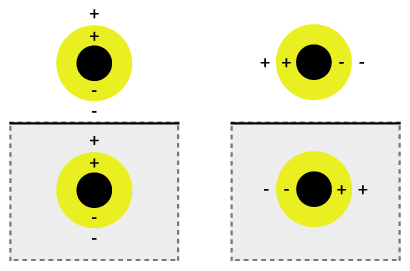
Jednoczesną oscylację można nazwać hybrydyzacją plazmonową, gdzie przestrajalność oscylacji jest związana z mieszaniem powłoki wewnętrznej i zewnętrznej, gdzie hybrydyzują, dając niższą lub wyższą energię. Ta niższa energia łączy się silnie z padającym światłem, podczas gdy wyższa energia jest antywiążąca i słabo łączy się ze światłem padającym. Oddziaływanie hybrydyzacyjne jest silniejsze w przypadku cieńszych warstw powłoki, stąd grubość powłoki i całkowity promień cząstki określają, z jaką długością fali światła się łączy. Nanopowłoki można zmieniać w szerokim zakresie widma światła która obejmuje zakres widzialny i bliską podczerwień. Oddziaływanie światła i nanocząstek wpływa na rozmieszczenie ładunków, co wpływa na siłę sprzężenia. Światło padające spolaryzowane równolegle do podłoża daje polaryzację s (rysunek 1b), stąd ładunki są dalej od powierzchni podłoża, co daje silniejsze oddziaływanie między powłoką a rdzeniem. W przeciwnym razie powstaje polaryzacja p, która daje silniej przesuniętą energię plazmonu, powodując słabsze oddziaływanie i sprzężenie.
Odkrycie
Odkrycia nanopowłoki dokonała profesor Naomi J. Halas i jej zespół z Rice University w 2003 roku. Kiedy ona i jej zespół odkryli nanopowłoki, początkowo nie byli pewni, jaki potencjał mają takie nanopowłoki. „Powiedzieliśmy:„ Rany, do czego to może być dobre? ”- powiedział Halas dla CNN. Po wielu sugestiach terapia przeciwnowotworowa wyłoniła się z trwającej współpracy z bioinżynierami poszukującymi różnych rodzajów zastosowań biomedycznych. „Jedna z naszych wizji”, stwierdził Halas, „nie mniej niż jednorazowa diagnostyka i leczenie raka”. Nanotechnology Now w kategorii Najlepsze odkrycie 2003 roku .
Produkcja
Najnowocześniejszą metodą syntezy złotych nanopowłok jest zastosowanie mikroprzepływowych pianek kompozytowych. Ta metoda może potencjalnie zastąpić standardową litograficzną metodę syntezy nanopowłok plazmonicznych. Proces produkcji opisany poniżej był eksperymentem przeprowadzonym przez Suhanyę Duraiswamy i Saif A. Khan z Wydziału Inżynierii Chemicznej i Biomolekularnej w Singapurze. Chociaż ta metoda była eksperymentem, reprezentuje przyszłość syntezy nanopowłok.
Materiały wymagane do produkcji nanopowłok są następujące; Ortokrzemian tetraetylu, wodorotlenek amonu, chlorowodorek hydroksyloaminy, 3-aminopropylotris, trihydrat wodorotetrachloroaurynianu(III), chlorek tetrakis(hydroksymetylo)fosfoniowy, wodorotlenek sodu, węglan potasu, etanol.
Pierwszym krokiem w syntezie nanopowłok w tej metodzie jest stworzenie urządzenia, w którym zajdzie reakcja. Wzory urządzeń mikroprzepływowych wykonano na płytkach krzemowych za pomocą standardowej fotolitografii przy użyciu negatywowego fotorezystu SU-8 2050. Urządzenia następnie uformowano w poli (dimetylosiloksanie) (PDMS) przy użyciu techniki miękkiej litografii. (40) W skrócie, PDMS formowano na matrycach SU-8 w temperaturze 70 ° C przez 4 godziny, obrano, pocięto i wyczyszczono. W urządzeniu wybito otwory wlotowe i wylotowe (1/16 cala średnicy). Mikrokanały zostały nieodwracalnie związane ze szkiełkiem pokrytym cienką warstwą PDMS po krótkiej 35-sekundowej obróbce plazmą powietrzną. Mikrokanaliki mają prostokątny przekrój i szerokość 300 μm, głębokość 155 μm i długość 0,45 m.
Rzeczywista produkcja nanocząstek polega na pompowaniu „oleju silikonowego, mieszaniny cząstek krzemionki pozłacanej i roztworu do powlekania złotem oraz roztworu środka redukującego do urządzenia mikroprzepływowego, podczas gdy gazowy azot był dostarczany z cylindra”. Roztwór powlekający pozostawiono następnie do starzenia w kontrolowanym środowisku na dłużej niż 24 godziny. Po procesie starzenia płyn jest pobierany z Urządzenia Mikroprzepływowego i umieszczany w wirówce. Powstała ciecz ma warstwę oleju na powierzchni z roztworem poniżej, który zawiera nanopowłoki.
Powodem, dla którego ta metoda jest rewolucyjna, jest to, że rozmiar i względną grubość złotej nanopowłoki można kontrolować, zmieniając czas trwania reakcji, a także stężenie roztworu do powlekania. Pozwala to naukowcom dostosować cząsteczki do ich potrzeb. Choćby dla optyki lub leczenia raka.
Lek na raka
Nanocząsteczki ze złotymi otoczkami, które są sferycznymi nanocząstkami z rdzeniami krzemionkowymi i/lub liposomowymi oraz złotymi otoczkami, są stosowane w terapii przeciwnowotworowej i ulepszaniu bioobrazowania. Sondy teranostyczne – zdolne do wykrywania i leczenia raka w jednym zabiegu – to nanocząsteczki , które mają miejsca wiązania na swojej powłoce, które pozwalają im przyczepić się do pożądanego miejsca (zwykle komórki nowotworowe), a następnie mogą być obrazowane za pomocą obrazowania dwumodalnego (strategia obrazowania wykorzystujące promieniowanie rentgenowskie i obrazowanie radionuklidów ) oraz fluorescencję w bliskiej podczerwieni. Powodem, dla którego stosuje się nanocząsteczki złota, są ich żywe właściwości optyczne, które są kontrolowane przez ich rozmiar, geometrię i plazmony powierzchniowe. Nanocząsteczki złota (takie jak AuNP) mają tę zaletę, że są biokompatybilne i elastyczne, że mają wiele różnych cząsteczek i podstawowych materiałów przyczepionych do ich powłoki (prawie wszystko, co normalnie może być przyłączone do złota, może być przyłączone do złotej nanopowłoki, które mogą być pomocne w rozpoznawaniu i leczeniu raka). Leczenie raka jest możliwe tylko dzięki zachodzącemu rozpraszaniu i wchłanianiu plazmonika . Pod wpływem rozpraszania pozłacane nanocząsteczki stają się widoczne w procesach obrazowania, które są dostrojone do właściwej długości fali, która jest zależna od rozmiaru i geometrii cząstek. Podczas absorpcji ablacja fototermiczna , która podgrzewa nanocząsteczki i ich bezpośrednie otoczenie do temperatur zdolnych do zabicia komórek rakowych. Osiąga się to przy minimalnym uszkodzeniu komórek w ciele dzięki wykorzystaniu „okna wodnego” (zakres widmowy między 800 a 1300 nm). Ponieważ ludzkie ciało składa się głównie z wody, optymalizuje to użyte światło w stosunku do renderowanych efektów.
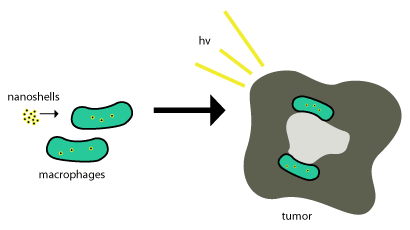
Te złote nanopowłoki są przenoszone do guzów za pomocą fagocytozy , w której fagocyty pochłaniają nanopowłoki przez błonę komórkową, tworząc wewnętrzny fagosom lub makrofag . Następnie jest przenoszony do komórki, a enzymy są zwykle używane do jego metabolizowania i przenoszenia z powrotem z komórki. Te nanopowłoki nie są metabolizowane, więc aby były skuteczne, muszą po prostu znajdować się w komórkach nowotworowych , a do zakończenia komórek nowotworowych stosowana jest fotoindukowana śmierć komórek (jak opisano powyżej). Schemat ten pokazano na rysunku 2.
Środki lecznicze oparte na nanocząstkach zostały z powodzeniem wprowadzone do guzów dzięki wykorzystaniu zwiększonej przepuszczalności i efektu retencji, właściwości, która pozwala na bierne wchłanianie nanoskalowych struktur do guzów bez pomocy przeciwciał.[4] Dostarczenie nanopowłok do ważnych obszarów guza może być bardzo trudne. W tym miejscu większość nanopowłok próbuje wykorzystać naturalną rekrutację monocytów przez guz do dostarczenia, jak widać na powyższym rysunku. Ten system dostarczania jest nazywany „końem trojańskim”.
Ten proces działa tak dobrze, ponieważ guzy składają się z około ¾ makrofagów, a po wprowadzeniu monocytów do guza różnicują się one w makrofagi, które również byłyby potrzebne do utrzymania nanocząstek ładunku . Gdy nanopowłoki znajdą się w centrum martwicy, do zniszczenia makrofagów związanych z guzem stosuje się oświetlenie bliskiej podczerwieni.
Dodatkowo, te nanocząstki można zmusić do uwalniania antysensownych oligonukleotydów DNA podczas fotoaktywacji. Te oligonukleotydy są stosowane w połączeniu z zabiegami ablacji fototermicznej w celu przeprowadzenia terapii genowej. Osiąga się to, ponieważ kompleksy nanocząstek są dostarczane do wnętrza komórek, a następnie ulegają indukowanemu światłem uwalnianiu DNA z ich powierzchni. Umożliwi to wewnętrzną manipulację komórką i zapewni środki do monitorowania powrotu komórek grupy do równowagi.
Inny przykład plazmoniki nanopowłokowej w leczeniu raka polega na umieszczaniu leków wewnątrz nanocząstki i używaniu jej jako nośnika do dostarczania toksycznych leków tylko do miejsc rakowych. Osiąga się to poprzez pokrycie zewnętrznej strony nanocząstki tlenkiem żelaza (umożliwiając łatwe śledzenie za pomocą urządzenia MRI ), a następnie po pokryciu obszaru guza nanocząstkami wypełnionymi lekiem, nanocząsteczki można aktywować za pomocą rezonansowych fal świetlnych w celu uwolnienia leku.