Analog stanu przejściowego
Analogi stanu przejściowego ( analogi stanu przejściowego ) to związki chemiczne o strukturze chemicznej , która przypomina stan przejściowy cząsteczki substratu w reakcji chemicznej katalizowanej enzymami . Enzymy oddziałują z substratem za pomocą naprężeń lub zniekształceń, przesuwając substrat w kierunku stanu przejściowego. Analogi stanu przejściowego mogą być stosowane jako inhibitory w reakcjach katalizowanych przez enzymy poprzez blokowanie miejsca aktywnego enzymu. Teoria sugeruje, że inhibitory enzymów który przypominał strukturę stanu przejściowego, wiązałby się z enzymem mocniej niż rzeczywisty substrat. Przykłady leków , które są inhibitorami analogów stanu przejściowego, obejmują leki przeciw grypie, takie jak inhibitor neuraminidazy oseltamiwir i inhibitory proteazy HIV sakwinawir w leczeniu AIDS.
Analog stanu przejściowego
Stan przejściowy struktury można najlepiej opisać w odniesieniu do mechaniki statystycznej , w której energie pękania i tworzenia wiązań mają równe prawdopodobieństwo przejścia ze stanu przejściowego wstecz do reagentów lub do przodu do produktów. W reakcjach katalizowanych przez enzymy całkowita energia aktywacji reakcji jest obniżana, gdy enzym stabilizuje przejście o wysokiej energii stan pośredni. Analogi stanu przejściowego naśladują ten wysokoenergetyczny związek pośredni, ale nie przechodzą katalizowanej reakcji chemicznej i dlatego mogą wiązać się z enzymem znacznie silniej niż proste analogi substratu lub produktu.
Projektowanie analogów stanu przejściowego
Aby zaprojektować analog stanu przejściowego, kluczowym krokiem jest określenie struktury stanu przejściowego substratu na konkretnym enzymie będącym przedmiotem zainteresowania za pomocą metody eksperymentalnej, na przykład kinetycznego efektu izotopowego . Ponadto strukturę stanu przejściowego można również przewidzieć za pomocą podejść obliczeniowych jako uzupełnienie KIE. Wyjaśnimy pokrótce te dwie metody.
Kinetyczny efekt izotopowy
Kinetyczny efekt izotopowy (KIE) jest miarą szybkości reakcji reagentów znakowanych izotopowo z bardziej powszechnym naturalnym substratem. Wartości kinetycznego efektu izotopowego są stosunkiem liczby obrotów i obejmują wszystkie etapy reakcji. Wewnętrzne wartości izotopów kinetycznych wynikają z różnicy w środowisku wibracyjnym wiązań atomu w reagentach w stanie podstawowym do środowiska stanu przejściowego atomu. Dzięki kinetycznemu efektowi izotopowemu można uzyskać wiele informacji na temat tego, jak wygląda stan przejściowy reakcji katalizowanej przez enzymy, i kierować rozwojem analogów stanu przejściowego.
Symulacja obliczeniowa
Podejścia obliczeniowe zostały uznane za przydatne narzędzie do wyjaśnienia mechanizmu działania enzymów. Sama mechanika molekularna nie jest w stanie przewidzieć transferu elektronu , który jest podstawą reakcji organicznych, ale symulacja dynamiki molekularnej dostarcza wystarczających informacji, biorąc pod uwagę elastyczność białka podczas reakcji katalitycznej. Metodą uzupełniającą byłoby połączenie symulacji mechaniki molekularnej/mechaniki kwantowej ( QM/MM ) metody. Dzięki takiemu podejściu tylko atomy odpowiedzialne za reakcję enzymatyczną w regionie katalitycznym zostaną poddane obróbce za pomocą mechaniki kwantowej , a pozostałe atomy zostaną poddane obróbce za pomocą mechaniki molekularnej .
Przykłady konstrukcji analogowych stanu przejściowego
Po określeniu struktur stanu przejściowego za pomocą KIE lub symulacji obliczeniowych, inhibitor można zaprojektować zgodnie z określonymi strukturami stanu przejściowego lub półproduktami. Poniższe trzy przykłady ilustrują, w jaki sposób inhibitory naśladują strukturę stanu przejściowego poprzez zmianę grup funkcyjnych, co odpowiada geometrii i rozkładowi elektrostatycznemu struktur stanu przejściowego.
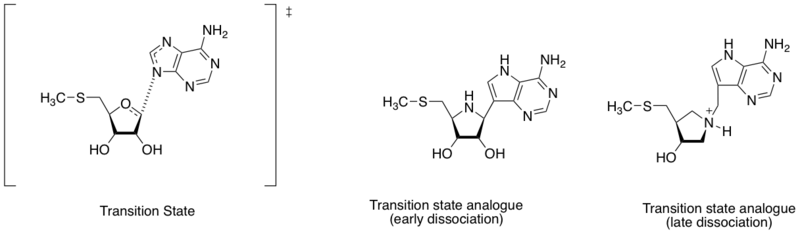
Inhibitor nukleozydazy metylotioadenozyny
Nukleozydaza metylotioadenozyny to enzymy, które katalizują reakcję hydrolitycznego deadenylowania 5'-metylotioadenozyny i S-adenozylohomocysteiny. Jest również uważany za ważny cel dla odkrywania leków przeciwbakteryjnych, ponieważ jest ważny w systemie metabolicznym bakterii i jest wytwarzany tylko przez bakterie. Biorąc pod uwagę różną odległość między atomem azotu adeniny a anomerycznym węglem rybozy (patrz diagram w tej sekcji), strukturę stanu przejściowego można zdefiniować na podstawie wczesnego lub późnego etapu dysocjacji. Opierając się na znalezieniu różnych struktur stanu przejściowego, Schramm i współpracownicy zaprojektowali dwa analogi stanu przejściowego naśladujące wczesny i późny dysocjacyjny stan przejściowy. Pokazano wczesny i późny analog stanu przejściowego powinowactwo wiązania (Kd) odpowiednio 360 i 140 pM.
Inhibitor termolizyny
Termolizyna jest enzymem wytwarzanym przez Bacillus thermoproteolyticus , który katalizuje hydrolizę peptydów zawierających aminokwasy hydrofobowe. Dlatego też jest celem dla środków przeciwbakteryjnych. Mechanizm reakcji enzymatycznej rozpoczyna się od małej cząsteczki peptydu i zastępuje cząsteczkę wody wiążącą cynk w kierunku Glu143 termolizyny. Cząsteczka wody jest następnie aktywowana zarówno przez jon cynku, jak i resztę Glu143 i atakuje węgiel karbonylowy, tworząc czworościenny stan przejściowy (patrz rysunek). Holden i współpracownicy następnie naśladowali ten czworościenny stan przejściowy, aby zaprojektować serię analogów peptydów amidofosfonowych. Wśród zsyntetyzowanych analogów R = L -Leu ma najsilniejsze działanie hamujące ( Ki = 9,1 nM).
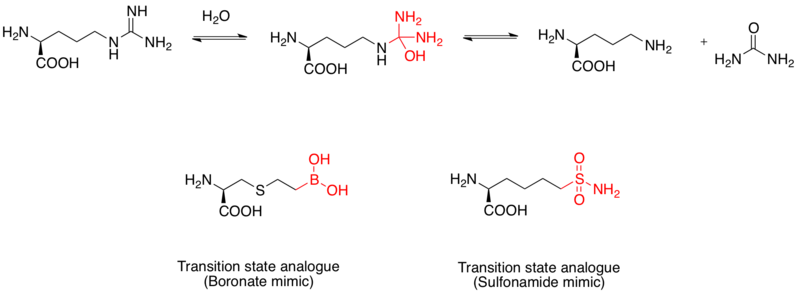
Inhibitor arginazy
Arginaza jest dwujądrową metaloproteiną manganu , która katalizuje hydrolizę L- argininy do L- ornityny i mocznika . Jest również uważany za cel leków w leczeniu astmy . Mechanizm hydrolizy L-argininy odbywa się poprzez nukleofilowy atak wody na grupę guanidynową, tworząc tetraedryczny związek pośredni. Badania wykazały, że kwasu boronowego przyjmuje konfigurację czworościenną i służy jako inhibitor. Ponadto sulfonamid grupa funkcyjna może również naśladować strukturę stanu przejściowego. Dowody na mimetyki kwasu boronowego jako inhibitory analogów stanu przejściowego ludzkiej arginazy I zostały wyjaśnione za pomocą rentgenowskich struktur krystalicznych.
Zobacz też
- Enzym
- Analog strukturalny , związki o podobnej budowie chemicznej
- Inhibitor enzymów
- Analog substratu
- Inhibitor samobójstwa
- podłoże