Oksokwas fosforowy
Oksokwas fosforowy (lub kwas fosforowy ) to ogólna nazwa dowolnego kwasu , którego cząsteczka składa się z atomów fosforu , tlenu i wodoru . Istnieje potencjalnie nieskończona liczba takich związków. Niektóre z nich są nietrwałe i nie zostały wyizolowane, ale pochodne aniony i grupy organiczne są obecne w trwałych solach i estrach . Najważniejsze z nich — w biologii, geologii, przemyśle i badaniach chemicznych — to tzw kwasy fosforowe , których estry i sole są fosforanami .
–O− ,
że grupa –OH może utracić proton H +
pozostawiając ujemnie naładowaną grupę iw ten sposób przekształcić kwas w oksoanion fosforu . Każdy dodatkowy utracony proton ma powiązaną stałą dysocjacji kwasowej Ka 1 kologarithm , Ka 2 Ka 3 , ( ..., często wyrażaną przez jego pK a 1 , pK a 2 , pK a 3 , ...). Atomy wodoru związane bezpośrednio z fosforem na ogół nie są kwaśne.
Klasyfikacja
Oksokwasy fosforowe można sklasyfikować na podstawie stopnia(ów) utlenienia atomu(ów) fosforu, który może wahać się od +1 do +5. Atomy tlenu są zwykle w stanie utlenienia -2, ale mogą być w stanie -1, jeśli cząsteczka zawiera grupy nadtlenkowe .
Stan utlenienia +1
-
Kwas podfosforawy (lub kwas fosfinowy), H
3 PO
2 (lub H
2 PO(OH) ), kwas monoprotonowy (co oznacza, że tylko jeden z atomów wodoru jest kwasowy). Jego sole i estry nazywane są podfosforynami lub fosfinianami.
Stan utlenienia +3
-
Kwas fosforawy (lub kwas fosfonowy), H
3 PO
3 (lub HPO(OH)
2 ), kwas diprotonowy (zawierający tylko dwa kwaśne atomy wodoru). Jego sole i estry nazywane są fosforynami lub fosfonianami.
Stan utlenienia +4
-
Kwas podfosforowy , H
4 P
2 O
6 (lub (HO)
2 P – P(OH)
2 ). Wszystkie cztery atomy wodoru są kwasowe. Jego sole i estry są podfosforanami.
Stan utlenienia +5
Najważniejszymi przedstawicielami tej grupy są kwasy fosforowe , w których każdy atom fosforu jest związany z czterema atomami tlenu, z których jeden poprzez wiązanie podwójne , ułożone jako rogi czworościanu . Dwa lub więcej z tych PO
4 może być połączonych wspólnymi pojedynczymi wiązaniami atomów tlenu, tworząc liniowe lub rozgałęzione łańcuchy, cykle lub bardziej złożone struktury. Atomy tlenu związane pojedynczymi wiązaniami, które nie są wspólne, są uzupełnione kwaśnymi atomami wodoru. Ich ogólna formuła to H n − x +2 P n O 3 n − x +1 , gdzie n to liczba atomów fosforu, a x to liczba podstawowych cykli w strukturze cząsteczki.
Kwasy te oraz ich estry i sole („ fosforany ”) obejmują jedne z najbardziej znanych i najważniejszych związków fosforu.
Najprostszym członkiem tej klasy jest:
-
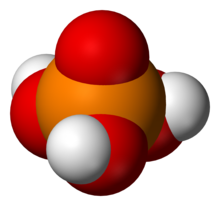
Kwas fosforowy właściwy (zwany także kwasem ortofosforowym lub kwasem monofosforowym), H
3 PO
4 (lub OP(OH)
3 ), kwas triprotyczny. Tworzy sole ortofosforanowe i estry, zwane potocznie fosforanami .
Najmniejsze związki tej klasy z dwoma lub więcej atomami fosforu nazywane są „kwasami oligofosforowymi”, a większe, z liniowymi szkieletami –P – O–, to „kwasy polifosforowe”; bez wyraźnego podziału między nimi. Niektóre z najważniejszych członków to:
-
Kwas pirofosforowy , H
4 P
2 O
7 (lub (HO)
2 P –O– P(OH)
2 ), z czterema kwaśnymi atomami wodoru. Tworzy pirofosforany . -
Kwas trifosforowy (lub kwas tripolifosforowy), H
5 P
3 O
10 (lub (HO)
2 P –O– P(OH) –O– P(OH)
2 ), z pięcioma kwaśnymi atomami wodoru. Tworzy trifosforany lub tripolifosforany. - Kwas tetrafosforowy, H
6 P
4 O
13 (lub (HO)
2 P (–O– P(OH) ) 2 –O– P(OH)
2 ), z sześcioma kwaśnymi atomami wodoru. Tworzy tetrafosforany.
Kręgosłup może być rozgałęziony, jak w:
- Kwas trifosfonofosforowy, H
6 P
4 O
13 lub P(O)(– OP(O)(OH)
2 ) 3 , rozgałęziony izomer kwasu tetrapolifosforowego.
Tetraedry PO
4 można łączyć w zamknięte łańcuchy –P–O–, jak w:
- Kwas trimetafosforowy (lub kwas cyklotrifosforowy), H
3 P
3 O
9 (lub (HPO
3 )
3 , (–P(O)(OH)–O–) 3 ), cykliczna cząsteczka z trzema kwaśnymi atomami wodoru. Tworzy sole i estry trimetafosforanowe.
Kwas metafosforowy to ogólne określenie kwasów fosforowych o jednym cyklu (–P(O)(OH)–O–) n , których wzór elementarny to HPO
3 .
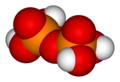
Kwas pirofosforowy H
4 P
2 O
7
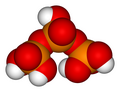
Kwas tripolifosforowy H
5 P
3 O
10
Innym związkiem, który można zaliczyć do tej klasy jest
- Kwas peroksomonofosforowy , H 3 PO 5 (lub OP(OH) 2 (OOH)), który można postrzegać jako kwas monofosforowy z grupą nadtlenkową zastępującą atom tlenu w jednej z grup hydroksylowych
Mieszane stopnie utlenienia
Niektóre oksokwasy fosforu mają dwa lub więcej atomów P na różnych stopniach utlenienia. Jednym z przykładów jest
-
Kwas izofosforowy , H
4 P
2 O
6 (lub H(OH)(O)P−O−P(O)(OH) 2 ), kwas tetraprotonowy i izomer kwasu podfosforowego, zawierający P na stopniu utlenienia +3 i +5
Zobacz też
Dalsza lektura
- Schröder HC, Kurz L, Muller WE, Lorenz B (marzec 2000). „Polifosforany w kości” (PDF) . Biochemia (Moskwa) . 65 (3): 296–303. Zarchiwizowane od oryginału (PDF) w dniu 25.08.2011.
Linki zewnętrzne
- Oznaczanie polifosforanów za pomocą chromatografii jonowej z detekcją przewodnictwa tłumionego, nota aplikacyjna 71 firmy Dionex
- US 3044851 , Young, Donald C., „Production of ammonium fosforans and its product”, opublikowany 1962-07-17, przeniesiony na Collier Carbon & Chemical Co.
- Fosfor + kwasy w US National Library of Medicine Medical Subject Headings (MeSH)