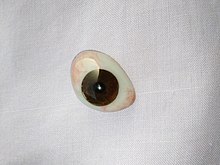
Proteza oka
Proteza oka , sztuczne oko lub szklane oko to rodzaj protezy twarzoczaszki , która zastępuje nieobecne naturalne oko po wyłuszczeniu , wytrzewieniu lub wytrzewieniu oczodołu . Proteza pasuje na implant oczodołu i pod powieki . Chociaż często nazywana jest szklanym okiem, proteza oka ma z grubsza kształt wypukłej skorupy i jest wykonana z medycznego tworzywa sztucznego akrylowego . Obecnie kilka protez ocznych jest wykonanych ze kriolitowego . Wariantem protezy oka jest bardzo cienka twarda skorupa znana jako skorupa twardówki , którą można nosić na uszkodzonym lub wypatroszonym oku. Twórcy protez ocznych są znani jako okularnicy . Proteza oka nie zapewnia widzenia; byłaby to wizualna proteza . Ktoś z protezą oka jest całkowicie ślepy po chorej stronie i ma jednooczne (jednostronne) widzenie .
Historia

Najwcześniejszym znanym dowodem użycia protezy oka jest kobieta znaleziona w Shahr-I Sokhta w Iranie, datowana na 2900–2800 pne. Ma półkulisty kształt i średnicę nieco ponad 2,5 cm (1 cal). Składa się z bardzo lekkiego materiału, prawdopodobnie pasty bitumicznej. Powierzchnia sztucznego oka pokryta jest cienką warstwą złota, z wygrawerowanym centralnym kołem (reprezentującym tęczówkę) i złotymi liniami przypominającymi promienie słoneczne. Po obu stronach oka wywiercone są malutkie dziurki, przez które złota nić mogłaby utrzymać gałkę oczną w miejscu. Ponieważ badania mikroskopowe wykazały, że oczodół miał wyraźne odciski złotej nici, gałka oczna musiała być noszona za jej życia. Poza tym wczesny tekst hebrajski wspomina o kobiecie, która nosiła sztuczne oko ze złota. Wiadomo, że kapłani rzymscy i egipscy wytwarzali sztuczne oczy już w V wieku pne, zbudowane z malowanej gliny przymocowanej do materiału i noszonej poza oczodołem.
Pierwsze sztuczne oczy w gnieździe były wykonane ze złota z kolorową emalią, później ewoluowały w kierunku używania szkła (stąd nazwa „szklane oko”) przez Wenecjan w drugiej połowie XVI wieku. Były to prymitywne, niewygodne i kruche, a metodologia produkcji pozostawała znana tylko Wenecjanom do końca XVIII wieku, kiedy to paryżanie przejęli rolę centrum sztucznego wytwarzania oczu. Ale centrum ponownie przeniosło się, tym razem do Niemiec, ze względu na ich doskonałe techniki dmuchania szkła. Wkrótce po wprowadzeniu sztuki szklarskiej do Stanów Zjednoczonych towary niemieckie stały się niedostępne z powodu II wojny światowej. W rezultacie Stany Zjednoczone zamiast tego wykonały sztuczne oczy z tworzywa akrylowego.
Produkcja nowoczesnych protez ocznych rozszerzyła się od zwykłego szkła do wielu różnych rodzajów materiałów. W Stanach Zjednoczonych większość niestandardowych protez oka jest wytwarzana przy użyciu PMMA (polimetakrylanu metylu) lub akrylu. W niektórych krajach, zwłaszcza w Niemczech, protezy są nadal najczęściej wykonywane ze szkła.
Granice realizmu
Chirurdzy okulistyczni zawsze pracowali razem, aby sztuczne oczy wyglądały bardziej realistycznie. Przez dziesięciolecia wszystkie wysiłki i inwestycje mające na celu poprawę wyglądu sztucznych oczu były tłumione przez bezruch źrenicy. Jedno rozwiązanie tego problemu zostało niedawno zademonstrowane w urządzeniu opartym na wyświetlaczu LCD, który symuluje rozmiar źrenicy w funkcji światła otoczenia.
Rodzaje implantów i budowa chemiczna
Istnieje wiele różnych typów implantów, a ich klasyfikacja obejmuje kształt (kulisty lub jajowaty), standardowy lub niestandardowy, porowaty lub nieporowaty, specyficzny skład chemiczny oraz obecność kołka lub słupka ruchliwości. Najbardziej podstawowym uproszczeniem może być podział typów implantów na dwie główne grupy: niezintegrowane (nieporowate) i zintegrowane (porowate).
Implanty niezintegrowane
Chociaż istnieją dowody na to, że implanty oczne istnieją od tysięcy lat, około 1976 roku pojawiły się nowoczesne niezintegrowane sferyczne implanty wewnątrzkonturowe (nie tylko szklane oczy). Implanty niezintegrowane nie zawierają unikalnego aparatu przyczepiającego się do mięśni zewnątrzgałkowych i nie pozwalają na wrastanie tkanki organicznej w ich substancję nieorganiczną. Takie implanty nie mają bezpośredniego połączenia z protezą oka. Zwykle implanty te są pokryte materiałem, który umożliwia unieruchomienie mięśni prostych zewnątrzgałkowych, takich jak twardówka dawcy lub gaza poliestrowa, która poprawia ruchomość implantu, ale nie pozwala na bezpośrednie mechaniczne sprzężenie między implantem a sztucznym okiem. Implanty niezintegrowane obejmują kulki akrylowe (PMMA), szklane i silikonowe.
Polimetakrylan metylu (PMMA) (akryl)
Polimetakrylan metylu (PMMA), powszechnie znany jako akryl, jest przezroczystym tworzywem termoplastycznym dostępnym do stosowania jako proteza oka, zastępcze soczewki wewnątrzgałkowe, gdy oryginalna soczewka została usunięta w leczeniu zaćmy i była historycznie stosowana jako twarde soczewki kontaktowe.
PMMA ma dobry stopień kompatybilności z tkanką ludzką, znacznie bardziej niż szkło. Chociaż w przeszłości do wykonania niezintegrowanych implantów używano różnych materiałów, jednym z preferowanych implantów jest polimetakrylan metylu.
Implanty zintegrowane (porowate)
Porowata natura zintegrowanych implantów umożliwia wrastanie włóknisto-naczyniowe w implant, a tym samym również wprowadzanie kołków lub słupków. Ponieważ uważa się, że bezpośrednie sprzężenie mechaniczne poprawia ruchliwość sztucznego oka, podjęto próby opracowania tak zwanych „zintegrowanych implantów”, które są bezpośrednio połączone ze sztucznym okiem. W przeszłości implanty bezpośrednio mocowane do protezy były nieskuteczne z powodu przewlekłego stanu zapalnego lub infekcji wynikającej z odsłonięcia nieporowatego materiału implantu. Doprowadziło to do opracowania quasi-zintegrowanych implantów ze specjalnie zaprojektowaną przednią powierzchnią, która rzekomo lepiej przenosiła ruchliwość implantu do sztucznego oka przez zamkniętą spojówkę i torebkę Tenona. W 1985 roku uznano, że problemy związane z implantami zintegrowanymi zostały w dużej mierze rozwiązane wraz z wprowadzeniem sferycznych implantów wykonanych z porowatego hydroksyapatytu wapnia. Materiał ten pozwala na wrastanie włóknisto-naczyniowe w ciągu kilku miesięcy. Porowate implanty enukleacyjne są obecnie wytwarzane z różnych materiałów, w tym naturalnych i syntetycznych hydroksyapatyt , tlenek glinu i polietylen .
Chirurg może zmienić kontur porowatych implantów przed wprowadzeniem, a także możliwa jest modyfikacja konturu in situ, choć czasami jest to trudne.
Hydroksyapatyt (HA)
Implanty hydroksyapatytowe są kuliste i wykonane w różnych rozmiarach iz różnych materiałów (koralowe/syntetyczne).
Od czasu ich wprowadzenia w 1989 r., kiedy implant wykonany z hydroksyapatytu uzyskał aprobatę Agencji ds. Żywności i Leków, sferyczne implanty hydroksyapatytowe zyskały powszechną popularność jako implant wyłuszczający i były w pewnym momencie najczęściej stosowanym implantem orbitalnym w Stanach Zjednoczonych. Porowata natura tego materiału pozwala na wrastanie naczyń włóknistych w implant i pozwala na wprowadzenie urządzenia sprzęgającego (PEG) przy zmniejszonym ryzyku zapalenia lub infekcji, związanym z wcześniejszymi typami odsłoniętych zintegrowanych implantów.
Hydroksyapatyt jest ograniczony do wstępnie uformowanych (podstawowych) kulek (do wyłuszczenia) lub granulek (do tworzenia defektów).
Jedną z głównych wad HA jest to, że musi być pokryty materiałem egzogennym, takim jak twardówka, politereftalan etylenu lub siatka wikrylowa (co ma tę wadę, że tworzy szorstki interfejs tkanki implantu, co może prowadzić do trudności technicznych w implantacji i późniejszej erozji implantu). pokrywającą tkankę, a końcowym etapem jest ekstruzja), ponieważ bezpośrednie szycie nie jest możliwe w przypadku przyczepu mięśnia. Pokrycie twardówki niesie ze sobą ryzyko przeniesienia infekcji, stanu zapalnego i odrzucenia.
Badanie z 2008 roku wykazało, że HA ma szybsze tempo fibrowaskularyzacji niż MEDPOR, implant z porowatego polietylenu o dużej gęstości, wytwarzany z liniowego polietylenu o dużej gęstości.
Porowaty polietylen (PP)
Rozwój chemii polimerów umożliwił wprowadzenie do chirurgii implantów oczodołowych nowszych materiałów biokompatybilnych, takich jak porowaty polietylen (PP). Implanty enukleacyjne z porowatego polietylenu są stosowane co najmniej od 1989 roku. Są one dostępne w dziesiątkach prefabrykowanych kulistych i niesferycznych kształtach oraz w różnych rozmiarach lub w zwykłych blokach do zindywidualizowanego dostosowania śródoperacyjnego. Materiał jest twardy, ale plastyczny i umożliwia bezpośrednie przyszycie mięśni do implantu bez owijania lub wykonywania dodatkowych czynności. Dodatkowo gładka powierzchnia jest mniej ścierna i drażniąca niż inne materiały używane do podobnych celów. Polietylen zostaje również unaczyniony, co umożliwia umieszczenie tytanowego słupka ruchomości, który łączy implant z protezą w taki sam sposób, w jaki kołek jest używany do implantów hydroksyapatytowych.
Wykazano, że PP ma dobre wyniki, aw 2004 roku był to najczęściej stosowany implant orbitalny w Stanach Zjednoczonych. Porowaty polietylen spełnia kilka kryteriów udanego implantu, w tym małą skłonność do migracji i odbudowy ubytku w sposób anatomiczny; jest łatwo dostępny, ekonomiczny i można go łatwo modyfikować lub dostosowywać do każdej wady. Implant PP nie wymaga pokrycia, dzięki czemu pozwala uniknąć niektórych problemów związanych z implantami hydroksyapatytowymi.
Bioceramiczny
Protezy bioceramiczne wykonane są z tlenku glinu ( Al
2 O
3 ). Tlenek glinu jest ceramicznym biomateriałem, który jest używany od ponad 35 lat w ortopedii i stomatologii do różnych zastosowań protetycznych ze względu na niskie tarcie, trwałość, stabilność i obojętność. Implanty oczne z tlenku glinu można uzyskać w kształcie kulistym i niekulistym (jajowatym) oraz w różnych rozmiarach do stosowania w zębodole anoftalmicznym. Otrzymał aprobatę US Food and Drug Administration w kwietniu 2000 roku i został zatwierdzony przez Health and Welfare w Kanadzie w lutym 2001 roku.
Wcześniej wykazano, że tlenek glinu jest bardziej biokompatybilny niż HA w badaniach hodowli komórkowych i sugerowano go jako standardowy materiał odniesienia, gdy wymagane są badania biokompatybilności w celu zbadania nowych produktów. Współczynnik narażenia związany wcześniej z implantem bioceramicznym (2%) był niższy niż w większości doniesień dotyczących implantu HA lub porowatego polietylenu (0% do 50%).
Stożkowy implant orbitalny (COI) i uniwersalny stożkowy implant orbitalny (MCOI)
Bezpieczną i skuteczną kulę (wciąż popularną i łatwą w użyciu) uzupełniono piramidą lub implantem COI. COI ma unikalne elementy konstrukcyjne, które zostały włączone do ogólnego stożkowego kształtu, w tym płaską powierzchnię przednią, lepszą projekcję i wstępnie uformowane kanały dla mięśni prostych. Igły do szwów Vicryl 5-0 można z niewielkimi trudnościami wprowadzić bezpośrednio przez implant w celu zawiązania na przedniej powierzchni. Ponadto ten implant ma lekko zagłębioną szczelinę dla mięśnia prostego górnego i występ do wypełnienia sklepienia górnego.
Najnowszy model [ wymaga aktualizacji ] to wielozadaniowy stożkowy implant oczodołowy (MCOI), który został zaprojektowany w celu rozwiązania problemów pooperacyjnej orbity okołoocznej, która jest narażona na ryzyko rozwoju nieprawidłowości zębodołu, w tym wytrzeszczu gałki ocznej, retrakcji górnej powieki, pogłębienia bruzdy górnej, przechylenia do tyłu gałki ocznej protezy i rozciąganie dolnej powieki po wypatroszeniu lub wyłuszczeniu. Ogólnie uważa się, że problemy te są drugorzędne w stosunku do niedoborów objętości orbitalnej, które są również rozwiązywane przez MCOI. Stożkowy kształt MCOI bardziej odpowiada anatomicznemu kształtowi orbity niż sferyczny implant. Szersza część przednia w połączeniu z węższą i dłuższą częścią tylną pozwala na pełniejsze i naturalne uzupełnienie utraconej objętości oczodołu. Ten kształt zmniejsza ryzyko deformacji bruzdy górnej i zwiększa objętość stożka mięśniowego. Za pomocą tych implantów mięśnie można umieścić w dowolnym miejscu wybranym przez chirurga. Jest to korzystne w przypadkach uszkodzonych lub utraconych mięśni po urazie, a pozostałe mięśnie są transponowane w celu poprawy motoryki pooperacyjnej. W oczekiwaniu na przyszłe umieszczenie kołków, dostępna jest spłaszczona powierzchnia o średnicy 6 mm (0,24 cala), która eliminuje potrzebę golenia płaskiej przedniej powierzchni przed umieszczeniem kołków.
Oba implanty (COI i MCOI) składają się z wzajemnie połączonych kanałów, które umożliwiają wrastanie tkanki łącznej gospodarza. Całkowite unaczynienie implantu zmniejsza ryzyko infekcji, wypchnięcia i innych powikłań związanych z niezintegrowanymi implantami. Obydwa implanty zapewniają doskonałą motorykę i kosmetykę pooperacyjną.
Implanty kołkowe (słupki ruchowe).
W przypadku implantów hydroksyapatytowych procedura wtórna może polegać na wprowadzeniu zewnętrznego, okrągłego kołka lub wkrętu do implantu. Proteza jest modyfikowana, aby pomieścić kołek, tworząc przegub kulowy: po zakończeniu wrastania włóknisto-naczyniowego można wywiercić mały otwór w przedniej powierzchni implantu. Po spojówce ten otwór może być wyposażony w kołek z zaokrągloną końcówką, który pasuje do odpowiedniego zagłębienia na tylnej powierzchni sztucznego oka. Kołek ten bezpośrednio przenosi ruchliwość implantu do sztucznego oka. Jednak kołek ruchliwości jest montowany tylko u mniejszości pacjentów. Może to częściowo wynikać z problemów związanych z umieszczeniem kołka, podczas gdy zakłada się, że implanty hydroksyapatytowe zapewniają lepszą ruchomość sztucznego oka nawet bez kołka.
Polietylen zostaje również unaczyniony, co umożliwia umieszczenie tytanowego słupka ruchomości, który łączy implant z protezą w taki sam sposób, w jaki kołek jest używany do implantów hydroksyapatytowych.
Ruch implantu
Ruch implantu i protezy to ważne aspekty ogólnego wyglądu kosmetycznego po wyłuszczeniu i są niezbędne do osiągnięcia idealnego celu, jakim jest stworzenie realistycznego oka, podobnego pod każdym względem do normalnego drugiego oka. Istnieje kilka teorii poprawiających ruch gałek ocznych, takich jak stosowanie integrującego materiału protetycznego, mocowanie implantu, pokrywanie implantu (np. tkanką twardówki) lub przyszywanie mięśni oka bezpośrednio do implantu protetycznego. Sprawność przenoszenia ruchu z implantu na protezę określa stopień ruchomości protezy. Ruch jest przenoszony z tradycyjnych nieporowatych implantów sferycznych poprzez napięcie powierzchniowe na styku spojówkowo-protetycznym oraz ruch sklepień. Quasi-zintegrowane implanty mają nieregularnie ukształtowane powierzchnie, które tworzą pośredni mechanizm sprzęgający między implantem a protezą, który nadaje protezie większy ruch. Oczekuje się, że bezpośrednia integracja implantu z protezą poprzez zewnętrzny mechanizm sprzęgający jeszcze bardziej poprawi ruchliwość.
Pomimo rozumowania stwierdzającego, że hydroksyapatytowe implanty oczodołu bez kołka ruchliwości zapewniłyby lepszą ruchliwość sztucznego oka, gdy stosowane są podobne techniki chirurgiczne, nieprzytwierdzone porowate (hydroksyapatytowe) implanty wyłuszczające i nieporowate (akrylowe) sferyczne implanty wyłuszczające pokryte twardówką dawcy dają porównywalną ruchliwość sztucznego oka . W dwóch badaniach nie stwierdzono różnic w maksymalnej amplitudzie między hydroksyapatytowymi a akrylowymi lub silikonowymi sferycznymi implantami wyłuszczającymi, co wskazuje, że sam materiał implantu może nie mieć wpływu na ruch implantu, o ile mięśnie są przyczepione bezpośrednio lub pośrednio do implantu, a implant nie jest osadzony. Ruchliwość niezintegrowanego sztucznego oka może być spowodowana co najmniej dwiema siłami:
- Siła tarcia między tylną powierzchnią sztucznego oka a spojówką osłaniającą implant może spowodować przesunięcie sztucznego oka. Ponieważ siła ta prawdopodobnie będzie w przybliżeniu równa we wszystkich kierunkach, spowodowałaby porównywalne poziome i pionowe amplitudy sztucznego oka. [ potrzebne źródło ]
- Sztuczne oko zwykle dobrze przylega do przestrzeni spojówkowej (prawdopodobnie nie w sklepieniu górnym). Dlatego każdy ruch sklepienia spojówkowego spowoduje podobny ruch sztucznego oka, natomiast brak ruchu sklepienia spojówkowego ograniczy jego ruchliwość.
Tradycyjnie uważano, że imbrykacja mięśni prostych nad niezintegrowanym implantem nadaje ruch implantowi i protezie. Podobnie jak przegub kulowy, gdy implant się porusza, proteza się porusza. Jednak ze względu na to, że tzw. kula i panewka są oddzielone warstwami torebki Tenona, mięśni imbrykowanych i spojówki, mechaniczna sprawność przenoszenia ruchu z implantu na protezę jest nieoptymalna. Co więcej, istnieje obawa, że imbrykacja mięśnia prostego nad niezintegrowanymi implantami może w rzeczywistości spowodować migrację implantu. Nowoczesna technika wyłuszczania mięśniowo-spojówkowego jest alternatywą dla imbrykacji mięśni.
Chociaż ogólnie przyjmuje się, że zintegrowanie protezy z porowatym implantem za pomocą kołka poprawia ruch protezy, w literaturze dostępnych jest niewiele dowodów dokumentujących stopień poprawy. I chociaż donoszono, że porowate implanty zapewniają lepszą ruchomość implantu, są one oczywiście droższe i inwazyjne, wymagają owinięcia, a następnie obrazowania w celu określenia unaczynienia i kołkowania w celu zapewnienia lepszego przenoszenia ruchu implantu na protezę, a także są podatne na odsłonięcie implantu.
Wiek i rozmiar implantu mogą również wpływać na ruchliwość, ponieważ w badaniu porównującym pacjentów z implantami hydroksyapatytowymi i pacjentami z implantami nieporowatymi ruch implantu wydawał się zmniejszać wraz z wiekiem w obu grupach. Badanie to wykazało również poprawę ruchu większych implantów niezależnie od materiału.
Zabieg chirurgiczny
Zasadniczo operacja obejmuje następujące kroki:
- Znieczulenie
- Perytomia spojówkowa
- Oddzielenie powięzi przedniej Tenona od twardówki
- Przeprowadź szwy przez mięśnie proste
- Mięśnie proste wyjęte z kuli ziemskiej
- Obracaj i podnoś kulę ziemską
- Otwórz torebkę Tenona, aby uwidocznić nerw wzrokowy
- Przypalić niezbędne naczynia krwionośne
- Podziel nerw
- Usuń oko
- Hemostazę uzyskuje się za pomocą kauteryzacji lub nacisku palca
- Włóż implant orbitalny.
- W razie potrzeby (hydroksyapatyt) należy wcześniej przykryć implant materiałem owijającym
- Przymocuj mięsień (jeśli to możliwe) bezpośrednio (PP) lub pośrednio (HA) do implantu.
- W razie potrzeby utwórz okienka w materiale do pakowania
- W przypadku implantów HA wywierć otwory o średnicy 1 mm jako miejsce wprowadzenia mięśnia
- Narysuj powięź Tenona nad implantem
- Zamknij twarz Tenona w jednej lub dwóch warstwach
- Zszyj spojówkę
- Włóż tymczasowy konformator oka do czasu otrzymania protezy (4–8 tygodni później)
- Po unaczynieniu implantu można wykonać opcjonalną procedurę wtórną polegającą na umieszczeniu kołka lub wkładu.
Również w znieczuleniu:
- Utworzyć nacięcie spojówkowe w miejscu wprowadzenia kołka
- Utwórz otwór w implancie, aby włożyć kołek lub słupek
- Zmodyfikuj protezę, aby otrzymać kołek/słupek.
Operację przeprowadza się w znieczuleniu ogólnym z dodatkiem dodatkowych środków znieczulających podspojówkowo i/lub pozagałkowo, w niektórych przypadkach wstrzykiwanych miejscowo. Poniżej znajduje się opis zabiegu chirurgicznego przeprowadzonego przez Custera i in. :
Perytomię spojówki wykonuje się na rąbku rogówki, zachowując jak najwięcej zdrowej tkanki. Powięź przedniego czopu jest oddzielona od twardówki. Tępe rozwarstwienie w czterech ćwiartkach między mięśniami prostymi oddziela głęboką powięź Tenona.
Szwy można przeciągnąć przez mięśnie proste przed ich wyjęciem z gałki ocznej. Niektórzy chirurdzy zszywają również jeden lub oba mięśnie skośne. Szwy trakcyjne lub zaciski można założyć na poziome wstawki mięśnia prostego, aby pomóc w obracaniu i unoszeniu gałki ocznej podczas późniejszego rozwarstwienia. Torebkę Tenona można otworzyć z tyłu, aby umożliwić wizualizację nerwu wzrokowego. Żyły wirowe i tylne naczynia rzęskowe można wypalić przed przecięciem nerwu i usunięciem oka. Alternatywnie nerw wzrokowy można zlokalizować za pomocą zacisku przed przecięciem. Hemostazę uzyskuje się za pomocą kauteryzacji lub nacisku palca.
Implant orbitalny jest wprowadzany w momencie wyłuszczenia. Implant o odpowiednim rozmiarze powinien zastąpić gałkę oczną i pozostawić wystarczającą ilość miejsca na protezę oka. Implanty wyłuszczające są dostępne w różnych rozmiarach, które można określić za pomocą implantów dopasowujących lub obliczyć, mierząc objętość gałki ocznej lub długość osiową przeciwległego oka.
W przeszłości sferyczne, nieporowate implanty umieszczano w przestrzeni wewnątrzkonnej, a mięśnie zewnątrzgałkowe pozostawiano nie przyczepione lub wiązano na implancie. Owinięcie tych implantów umożliwia przyczepienie mięśni do materiału pokrywającego, technika, która wydaje się poprawiać ruch implantu i zmniejszać częstość migracji implantu. Porowate implanty przed wprowadzeniem można nasączyć roztworem antybiotyku. Ponieważ krucha natura hydroksyapatytu uniemożliwia bezpośrednie przyszycie mięśni do implantu, implanty te są zwykle pokryte jakąś formą materiału owijającego. Mięśnie są mocowane do implantu w technice podobnej do stosowanej w przypadku kulistych, nieporowatych implantów. Mięśnie mogą być bezpośrednio przyszyte do porowatych implantów polietylenowych poprzez przeciągnięcie szwu przez materiał implantu lub przy użyciu implantu z wykonanymi tunelami szwów. Niektórzy chirurdzy owijają również porowate implanty polietylenowe, aby ułatwić mocowanie mięśni lub zmniejszyć ryzyko odsłonięcia implantu. Do pokrycia porowatych implantów stosowano różne materiały owijające, w tym poliglaktynę lub siatkę z kwasu poliglikolowego, tkanki heterologiczne (osierdzie bydlęce), homologiczne tkanki dawcy (twardówka, skóra właściwa) i tkanki autogenne (powięź szeroka, powięź skroniowa, mięsień ucha tylnego, pochwa mięśnia prostego brzucha).
W miejscach wprowadzenia mięśni gałki ocznej powstają fenestracje w materiale owijającym, co umożliwia kontakt przyczepionych mięśni z implantem i poprawia unaczynienie implantu. Wiercenie otworów o średnicy 1 mm w implancie w miejscach przyczepu mięśnia wykonuje się w celu ułatwienia unaczynienia implantów hydroksyapatytowych. Powięź Tenona jest naciągana na implant i zamykana w jednej lub dwóch warstwach. Następnie zszywa się spojówkę.
Tymczasowy konformer oczny jest zakładany po zakończeniu zabiegu i jest noszony do momentu założenia protezy przez 4 do 8 tygodni po operacji.
Planowa procedura wtórna jest wymagana w celu umieszczenia kołka lub słupka łączącego u tych pacjentów, którzy chcą poprawić ruchomość protezy. Procedura ta jest zwykle opóźniana o co najmniej 6 miesięcy po wyłuszczeniu, aby dać czas na unaczynienie implantu. Skany rezonansu magnetycznego wzmocnione technetem lub gadolinem nie są obecnie powszechnie stosowane, ale były wykorzystywane do potwierdzania unaczynienia przed wprowadzeniem kołka. W znieczuleniu miejscowym w miejscu wkłucia kołka wykonuje się nacięcie spojówkowe. W porowatym implancie tworzony jest otwór umożliwiający wprowadzenie kołka lub słupka. Proteza jest następnie modyfikowana w celu przyjęcia kołka lub słupka. Niektórzy chirurdzy umieszczali słupki łączące w porowatych implantach polietylenowych w czasie wyłuszczania. Wkład może się samoistnie odsłonić lub zostać uzewnętrzniony w późniejszej procedurze przez nacięcie spojówki.
Następstwa zabiegów chirurgicznych
Niezależnie od zabiegu, po zabiegu zawsze potrzebny jest rodzaj protezy ocznej. Chirurg wstawi tymczasową protezę pod koniec operacji, znaną jako oko zapasowe, i skieruje pacjenta do okulisty , który nie jest lekarzem, ale okulistą certyfikowanym przez American Society of Ocularists. Proces wykonania protezy oka lub oka na zamówienie rozpocznie się zwykle sześć tygodni po zabiegu chirurgicznym i zazwyczaj trwa do trzech wizyt przed ostatecznym dopasowaniem protezy. W większości przypadków pacjent będzie dopasowywany podczas pierwszej wizyty, powróci na ręczne malowanie protezy, a na końcu przymiarki końcowej. Metody stosowane do dopasowania, kształtowania i malowania protezy często różnią się w zależności od potrzeb okulisty i pacjenta.
Życie z protezą oczną wymaga opieki, ale często pacjenci, którzy mieli nieuleczalne choroby oczu, takie jak mikroftalmia , anoftalmia lub siatkówczak , dzięki protezom osiągają lepszą jakość życia. Pielęgnacja protezy oka, poza regularnym polerowaniem i wizytami kontrolnymi u okulisty, zwykle polega na utrzymywaniu wilgotności i czystości protezy.
Znani ludzie z protezami oczu
- Bhumibol Adulyadej – król Tajlandii; stracił oko w wypadku samochodowym w 1948 roku (prawe oko)
- Baz Bastien – kanadyjski hokeista, trener (prawe oko)
- Mokhtar Belmokhtar - algierski przemytnik, porywacz, handlarz bronią i terrorysta; stracił oko, źle obchodząc się z materiałami wybuchowymi (lewe oko)
- Sammy Davis Jr. – amerykański piosenkarz (lewe oko)
- Peter Falk – amerykański aktor (prawe oko)
- Tex Avery – wpływowy amerykański reżyser animacji (lewe oko)
- Ry Cooder - Słynny muzyk najbardziej znany ze swojej gry na gitarze slide. (lewe oko)
- Nick Griffin – lider BNP (lewe oko)
- Leo McKern – aktor (lewe oko)
- Carl Ouellet - kanadyjski zawodowy zapaśnik (prawe oko)
- Claus Schenk Graf von Stauffenberg - zawodowy oficer armii niemieckiej i przywódca ruchu oporu (lewe oko)
- Robert Thurman – pisarz (lewe oko)
- Mo Udall – polityk (prawe oko)
Linki zewnętrzne
- Mapa myśli: dostosowanie i adaptacja do utraty wzroku
- Osobiste historie o posiadaniu sztucznego oka
- Wykonywanie protez oka
- Historia sztucznych oczu
- Protetyka oka
- Informacje o protezach oczu dla optyków oczu
- FourDoc (krótki dokument online) o ostatnim wytwórcy szklanych oczu w Anglii.
- Jak powstają protezy oczu
- Amerykańska Akademia Protetyki Szczękowo-Twarzowej
- Wprowadzenie do protezy samosmarującej