Reakcja Doebnera-Millera
Doebnera -Millera to organiczna reakcja aniliny z α, β- nienasyconymi związkami karbonylowymi w celu utworzenia chinoliny .
Ta reakcja jest również znana jako synteza chinoliny Skraupa-Doebnera-Von Millera i nosi imię czeskiego chemika Zdenka Hansa Skraupa (1850–1910) oraz Niemców Oscara Döbnera (Doebnera) (1850–1907) i Wilhelma von Millera ( 1848-1899). Gdy α,β-nienasycony karbonylowy jest przygotowywany in situ z dwóch związków karbonylowych (poprzez kondensację aldolową ), reakcja jest znana jako metoda Beyera dla chinolin .
Reakcję katalizują kwasy Lewisa, takie jak tetrachlorek cyny i triflat skandu(III), oraz kwasy Brønsteda, takie jak kwas p -toluenosulfonowy , kwas nadchlorowy , amberlit i jod .
Mechanizm reakcji
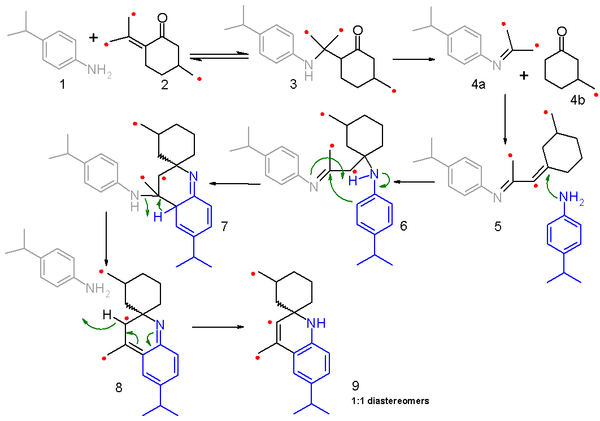
Mechanizm reakcji tej reakcji i związana z nią synteza Skraupa jest przedmiotem dyskusji. Badanie z 2006 roku proponuje mechanizm fragmentacji-rekombinacji oparty na izotopów węgla . W tym badaniu 4-izopropyloanilina 1 poddawana jest reakcji z mieszaniną (50:50) zwykłego pulegonu i izomeru 2 wzbogaconego w 13 C , a mechanizm reakcji przedstawiono na schemacie 2 z zaznaczonym węglem oznaczonym czerwoną kropką. Pierwszym etapem jest nukleofilowa addycja koniugatu aminy z enolem do aminy ketonu 3 w reakcji odwracalnej . Następnie ten związek pośredni ulega fragmentacji do iminy 4a i nasyconego cykloheksanonu 4b w nieodwracalnej reakcji i oba fragmenty rekombinują w reakcji kondensacji do skoniugowanej iminy 5 . W następnym etapie 5 reaguje z drugą cząsteczką aniliny w koniugacie nukleofilowym addycja do iminy 6 , a następnie addycja elektrofilowa i przeniesienie protonu prowadzi do 7 . eliminacja jednej cząsteczki aniliny przez 8 i reromatyzacja prowadzi do produktu końcowego 9 . Ponieważ protony α-aminowe nie są dostępne w tym modelowym związku, reakcja nie jest prowadzona do pełnoprawnej chinoliny.
Fragmentacja do 4a i 4b jest kluczem do tego mechanizmu, ponieważ wyjaśnia wyniki szyfrowania izotopów. W tej reakcji tylko połowa pulegonu ( 2 ) jest wyznakowana i po rekombinacji znakowany fragment iminy może reagować z innym znakowanym fragmentem ketonu lub fragmentem nieznakowanym i podobnie znakowany fragment ketonu może reagować ze znakowanym lub nieznakowanym fragmentem iminy. Otrzymany rozkład produktu potwierdza się za pomocą spektrometrii mas produktu końcowego 9.