Zakłócenia zwrotnicy
Interferencja crossover to termin używany w odniesieniu do nielosowego rozmieszczenia crossoverów względem siebie podczas mejozy . Termin ten przypisuje się Hermannowi Josephowi Mullerowi , który zauważył, że jedno skrzyżowanie „zakłóca zbieżne występowanie innego skrzyżowania w tej samej parze chromosomów, dlatego nazwałem to zjawisko„ interferencją ”.
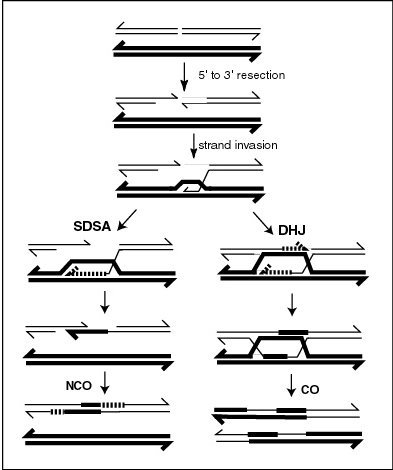
skrzyżowania mejotyczne (CO) są regulowane, aby zapewnić, że CO na tym samym chromosomie są rozmieszczone daleko od siebie (interferencja krzyżowania). W robaku nicieni Caenorhabditis elegans mejotyczne pęknięcia dwuniciowe (DSB) przewyższają liczbę CO. Zatem nie wszystkie DSB są naprawiane przez proces (procesy) rekombinacji prowadzące do CO. Białko RTEL-1 jest wymagane, aby zapobiec nadmiarowi mejotycznego CO. W tel-1 mejotyczna rekombinacja CO jest znacznie zwiększona i wydaje się, że nie występuje interferencja krzyżowa. RTEL1 prawdopodobnie działa poprzez promowanie wyżarzania nici zależnego od syntezy , co skutkuje rekombinantami bez krzyżowania (NCO) zamiast CO (patrz diagram). Zwykle około połowa wszystkich DSB jest przekształcana w podoficerów. Wydaje się, że RTEL-1 wymusza mejotyczną interferencję krzyżową, kierując naprawę niektórych DSB w stronę podoficerów, a nie CO.
U ludzi szybkość rekombinacji wzrasta wraz z wiekiem matki. Co więcej, wydaje się, że rozmieszczenie zdarzeń rekombinacji kobiet staje się coraz bardziej rozregulowane wraz z wiekiem matki, przy czym większa część zdarzeń występuje w bliższej odległości od siebie, niż można by się spodziewać w przypadku prostych modeli interferencji krzyżowej.
Wysoka ujemna interferencja
Bakteriofag T4
Wysoka interferencja ujemna (HNI), w przeciwieństwie do interferencji pozytywnej, odnosi się do powiązania zdarzeń rekombinacyjnych zwykle mierzonych na krótkich odległościach genomowych , zwykle w obrębie genu . Na tak krótkich odległościach występuje dodatnia korelacja (interferencja ujemna) zdarzeń rekombinacyjnych. Jak badano na bakteriofagach T4, korelacja ta jest tym większa, im krótszy jest odstęp między miejscami użytymi do wykrywania. HNI wynika z wielokrotnych wymian w krótkim regionie genomu podczas pojedynczego krycia. To, co jest liczone jako „pojedyncza wymiana” w krzyżówce genetycznej obejmującej tylko odległe markery, może w rzeczywistości być złożonym zdarzeniem, które jest rozmieszczone w skończonym regionie genomu. przełączanie między niciami matrycy DNA podczas syntezy DNA (patrz rysunek, szlak SDSA ), określane jako rekombinacja wyboru kopii, w celu wyjaśnienia dodatniej korelacji zdarzeń rekombinacji w obrębie genu. Wydaje się, że HNI wymaga dość precyzyjnej komplementarności zasad w regionach genomów rodzicielskich, w których występują powiązane zdarzenia rekombinacyjne.
HIV
Każda cząsteczka ludzkiego wirusa upośledzenia odporności ( HIV ) zawiera dwa jednoniciowe genomy RNA o pozytywnym sensie . Po zakażeniu komórki gospodarza DNA genomu jest tworzona przez odwrotną transkrypcję genomów RNA. Odwrotnej transkrypcji towarzyszy przełączanie matrycy między dwiema kopiami genomu RNA (rekombinacja wyboru kopii). W każdym cyklu replikacji występuje od 5 do 14 zdarzeń rekombinacji na genom. Ta rekombinacja wykazuje HNI. HNI jest najwyraźniej spowodowane przez skorelowane przełączniki szablonów podczas syntezy nici ujemnej DNA. Wydaje się, że rekombinacja przełączania szablonów jest niezbędna do utrzymania integralności genomu i jako mechanizm naprawczy do ratowania uszkodzonych genomów.
Linki zewnętrzne
-
 Media związane z interferencją genetyczną w Wikimedia Commons
Media związane z interferencją genetyczną w Wikimedia Commons