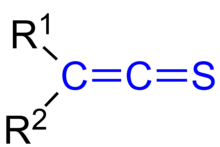tioketen
W chemii organicznej tioketeny są związkami siarkoorganicznymi analogicznymi do ketenów o ogólnym wzorze oznacza R2C =C=S , gdzie R alkil lub aryl . Macierzysty tioketen CH2 =C=S (etention) ma wzór . Jest to najprostszy tioketen. Tioketen jest stabilny jako gaz, ale podobnie jak większość tioketenów polimeryzuje podczas kondensacji.
Niektóre tiokeny są wytwarzane jako związki przejściowe podczas pirolizy 1,2,3 -tiadiazolu .
Izolowane tioketeny
Tioketeny można stabilizować za pomocą ochrony sterycznej lub efektów elektronicznych. Zatem di-tert-butylotioketen jest łatwy do wyizolowania i stabilny w powietrzu. Kilka przykładów scharakteryzowano za pomocą krystalografii rentgenowskiej . Odległość C=S wynosi 157 pm, a odległość C=C wynosi 124 pm, oba wiązania są odpowiednie do przypisania C=C=S. Fioletowy kolor charakterystyczny dla tioketenów wskazuje na małą lukę HOMO-LUMO . Związki te wytwarza się przez traktowanie chlorku kwasowego pięciosiarczkiem fosforu , jak opisano za pomocą następującego wyidealizowanego równania:
Przykładem elektronicznie stabilizowanego tioketenu jest bis(trifluorometylo)tioketen ( (CF 3 ) 2 C=C=S ).
Reakcje
Tioketeny są elektrofilowe. Dodają aminy, dając tioamidy:
- R 2 C=C=S + HNR' 2 → R 2 CH-C(S)-NR' 2
Z nadtlenokwasami wytwarzają S-tlenki tioketenu:
- R2C = C=S + R'CO3H → R2CH = C=S=O + R'CO2H
Tioketeny wiążą się z karbonylkami metali, tworząc addukty.
Związki pokrewne
- podsiarczek węgla ( S=C=C=C=S ).
Sugerowano, że tioketen może brać udział w procesach uszkadzania komórek.
-
^
Noslash;rkjær, Kim; Senning, Aleksander (1992). „Tio-, seleno- i telluroketeny”. Raporty siarki . 11 (2): 361–384. doi : 10.1080/01961779208046190 .
{{ cite journal }}: CS1 maint: wiele nazwisk: lista autorów ( link ) - ^ Otto-Albrecht Neuman (redaktor). Rompps Encyclopedia of Chemistry, Wydawnictwo Frank'sche, Stuttgart, 1983, 8. wydanie, s. 4242, ISBN 3-440-04513-7 .
- ^ ab Elam , UE; wysypka, FH; Dougherty, JT; Goodlett, VW; Brannock, KC (1968). „Di- tert -Butylotioketen”. Journal of Chemii Organicznej . 33 (7): 2738–2741. doi : 10.1021/jo01271a027 .
- ^ ab Schaumann , Ernst; Harto, Surya; Adiwidjaja, Gunadi (1979). „Kristall- und Molekülstruktur eines Ketens, eines Thioketens und eines Thioketen-S-oxids”. Chemische Berichte . 112 (7): 2698–2708. doi : 10.1002/cber.19791120738 .
- ^ Raasch, Maynard S. (1970). „Bis (trifluorometylo) tioketen. I. Synteza i reakcje cykloaddycji”. J.Org. chemia . 35 (10): 3470–3483. doi : 10.1021/jo00835a064 .
- Bibliografia _ Benecke, Jörg; Behrens, Ulrich (1989). „Übergangsmetall-heteroallen-kompleks” . Czasopismo chemii metaloorganicznej . 371 (2): 247–256. doi : 10.1016/0022-328x(89)88030-1 .
- Bibliografia _ Urban, Gudrun; Goersmann, Mikołaj; Anders, MW (1991). „Tworzenie tioketenu z dwusiarczków 2-nitrofenylu α-haloalkenylu: modele biologicznych reaktywnych związków pośrednich cytotoksycznych S-koniugatów”. J. Am. chemia soc . 113 (13): 5120–5122. doi : 10.1021/ja00013a090 .