Zapalenie jelita grubego-X
Zapalenie okrężnicy X , końskie zapalenie okrężnicy X lub nadostre toksemiczne zapalenie okrężnicy to ogólne określenie różnych śmiertelnych postaci ostrego lub nadostrego zapalenia okrężnicy występujących u koni , ale w szczególności piorunującego zapalenia okrężnicy , którego objawy kliniczne obejmują nagły początek ciężkiej biegunki, ból brzucha, wstrząs i odwodnienie . Śmierć jest powszechna, ze śmiertelnością od 90% do 100%, zwykle w mniej niż 24 godziny. Czynnikiem sprawczym może być Clostridium difficile , ale mogą go również wywołać inne patogeny jelitowe. Konie w stresie wydają się być bardziej podatne na rozwój zapalenia jelita grubego X i podobnie jak w przypadku rzekomobłoniastego zapalenia jelita grubego u ludzi, istnieje również związek z wcześniejszym stosowaniem antybiotyków. Natychmiastowe i agresywne leczenie może czasami uratować konia, ale nawet w takich przypadkach śmiertelność na poziomie 75% jest uważana za najlepszy scenariusz.
Objawy kliniczne
Colitis-X to termin używany w przypadkach zapalenia jelita grubego, w których nie można postawić ostatecznej diagnozy, a koń umiera. Objawy kliniczne obejmują nagłą, wodnistą biegunkę, której zwykle towarzyszą objawy wstrząsu hipowolemicznego i która zwykle prowadzi do śmierci w ciągu 3 do 48 godzin, zwykle w ciągu mniej niż 24 godzin. Inne objawy kliniczne obejmują tachykardię , przyspieszony oddech i słaby puls. Wyraźna depresja jest obecna. Wybuchowa biegunka rozwija się, powodując skrajne odwodnienie. Wstrząs hipowolemiczny i endotoksyczny objawia się wydłużeniem czasu powrotu naczyń włosowatych , przekrwieniem lub sinicą (purpurową) błoną śluzową i zimnymi kończynami. Chociaż początkowo może wystąpić gorączka , temperatura zwykle wraca do normy.
Objawy kliniczne są podobne do objawów innych chorób biegunkowych, w tym toksemii wywołanej przez Clostridium , końskiej gorączki Potomac , eksperymentalnego wstrząsu endotoksycznego i anafilaksji .
Powoduje
Do tej pory dokładny czynnik sprawczy nie został zweryfikowany, a różne źródła przypisują chorobę wirusom, pasożytom, bakteriom, stosowaniu antybiotyków i sulfonamidów oraz zatruciom metalami ciężkimi. Inne możliwe przyczyny to nadostra salmonelloza , zapalenie jelit spowodowane przez Clostridium i endotoksemię . Toksyny Clostridium difficile wyizolowane u koni mają genotyp podobny do obecnego ludzkiego „szczepu epidemicznego”, który jest powiązany z ludzką chorobą związaną z C. difficile o większym niż historyczna ciężkości. C. difficile może powodować rzekomobłoniaste zapalenie jelita grubego u ludzi, a u hospitalizowanych pacjentów, u których się rozwija, piorunujące zapalenie jelita grubego wywołane przez C. difficile jest istotną i coraz częstszą przyczyną śmierci.
Konie w stresie wydają się być bardziej podatne na rozwój zapalenia jelita grubego X. Początek choroby jest często ściśle związany z operacją lub transportem. Uważa się , że nadmiar białka i brak celulozy w diecie (dieta obfitująca w zboża i pozbawiona odpowiedniego siana lub podobnej paszy objętościowej) jest czynnikiem wyzwalającym namnażanie organizmów Clostridium . Podobny stan można zaobserwować po podaniu koniom tetracykliny lub linkomycyny . Czynniki te mogą być jednym z powodów, dla których stan ten często rozwija się u koni wyścigowych , ponieważ był odpowiedzialny za śmierć klaczki pełnej krwi angielskiej Landaluce , ogiera Quarter Horse Lightning Bar i jest jedną z teorii dotyczących nagłej śmierci zwycięzcy Kentucky Derby , Swale'a .
Związek ze stresem sugeruje, że stan ten może być spowodowany zmianami mikroflory jelita ślepego i okrężnicy, które zmniejszają liczbę bakterii beztlenowych, zwiększają liczbę bakterii jelitowych Gram-ujemnych i zmniejszają fermentację beztlenową rozpuszczalnych węglowodanów, powodując uszkodzenia do błony śluzowej jelita ślepego i okrężnicy oraz umożliwia zwiększoną absorpcję endotoksyn ze światła jelita.
Czynnikiem sprawczym może być Clostridium perfringens typu A, ale bakteria jest odzyskiwana tylko we wstępnych stadiach choroby.
Podejrzana toksyna może być również formą Clostridium difficile . W badaniu przeprowadzonym w 2009 roku na Uniwersytecie Arizony wykryto toksyny A i B C. difficile , wyizolowano dużą liczbę C. difficile , a charakterystyka genetyczna wykazała, że jest to północnoamerykańska elektroforeza żelowa w polu pulsacyjnym typu 1, rybotyp reakcji łańcuchowej polimerazy 027 i toksynotyp III. Obecne były geny toksyny binarnej, a negatywny regulator toksyny tcdC zawierał delecję 18 pz. U pojedynczego zwierzęcia badanego w tym przypadku zdiagnozowano nadostre zapalenie jelita grubego, ze zmianami i historią typową dla tych przypisywanych zapaleniu okrężnicy X.
Stosowanie antybiotyków może być również związane z niektórymi postaciami zapalenia jelita grubego-X. U ludzi C. difficile jest najpoważniejszą przyczyną biegunki związanej ze stosowaniem antybiotyków, często będącej wynikiem wyeliminowania normalnej flory jelitowej przez antybiotyki . W jednym badaniu z udziałem koni wywołano zapalenie okrężnicy po wstępnym leczeniu klindamycyną i linkomycyną , a następnie treścią jelitową koni, które padły z powodu naturalnie występującego idiopatycznego zapalenia okrężnicy. (Klasycznym działaniem niepożądanym klindamycyny u ludzi jest biegunka związana z C. difficile ). W eksperymencie leczone konie padły. Po sekcji zwłok Clostridium cadaveris była obecna i jest proponowana jako kolejny możliwy czynnik sprawczy w niektórych przypadkach śmiertelnego zapalenia jelita grubego.
Diagnoza
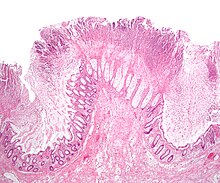
Podczas sekcji stwierdza się obrzęk i krwotok w ścianie jelita grubego i jelita ślepego , a treść jelit jest płynna i często zabarwiona krwią. W obrazie makroskopowym i mikroskopowym stwierdza się cechy rozsianego wykrzepiania wewnątrznaczyniowego, martwicę błony śluzowej okrężnicy oraz obecność dużej liczby bakterii w obumarłych częściach jelita. Zwykle PCV wynosi >65% nawet krótko po wystąpieniu objawów klinicznych. Leukogram waha się od normalnego do neutropenii ze zwyrodnieniowym przesunięciem w lewo. Występuje również kwasica metaboliczna i zaburzenia elektrolitowe. Występuje leukopenia, początkowo charakteryzująca się neutropenią, która może ewoluować w neutrofilię. Ponadto obserwuje się hemokoncentrację wraz ze wzrostem objętości upakowanych komórek; białka ogółem są początkowo zwiększone, ale zmieniają się do wartości niższej niż normalna. Najbardziej znaczącym odkryciem laboratoryjnym w zapaleniu jelita grubego X jest wzrost całkowitego stężenia kortyzolu w osoczu krwi. Histopatologicznie błona śluzowa jelita grubego jest krwotoczna, martwicza i pokryta wysiękiem włóknisto-krwotocznym, natomiast błona podśluzowa, osłona mięśniowa i miejscowe węzły chłonne są obrzęknięte.
Leczenie
Leczenie zapalenia jelita grubego-X zwykle nie ratuje konia. Rokowanie jest średnie lub złe, a śmiertelność wynosi od 90% do 100%. Dostępne są jednak metody leczenia, a jednym ze słynnych koni, które przeżyły zapalenie jelita grubego-X, był zwycięzca potrójnej korony Stanów Zjednoczonych Seattle Slew , który przeżył zapalenie jelita grubego-X w 1978 roku i zaczął ścigać się jako czterolatek. Aby przeciwdziałać ciężkiemu odwodnieniu, potrzebne są duże ilości płynów dożylnych i często konieczna jest wymiana elektrolitów. Meglumina fluniksyny (Banamine) może pomóc w blokowaniu skutków toksemii. Teoretycznie śmiertelność spada do 75%, jeśli leczenie jest szybkie i agresywne, w tym podawanie nie tylko płynów i elektrolitów, ale także osocza krwi, leków przeciwzapalnych i przeciwbólowych oraz antybiotyków. Zapobieganie odwodnieniu jest niezwykle ważne. Odżywianie jest również ważne. W celu wsparcia zestresowanego metabolizmu chorego konia można zastosować żywienie pozajelitowe lub normalne . Wreszcie, stosowanie probiotyków jest uważane za korzystne w przywracaniu normalnej flory jelitowej. Najczęściej stosowane w tym celu probiotyki to Lactobacillus i Bifidobacterium .