Niepożądana reakcja na lek
 | |
| Niepożądana reakcja na lek | |
|---|---|
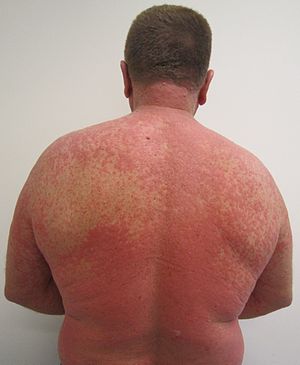
| Wysypka spowodowana reakcją na lek |
Niepożądana reakcja na lek ( ADR ) to szkodliwy, niezamierzony efekt spowodowany przyjmowaniem leków . Działania niepożądane mogą wystąpić po podaniu pojedynczej dawki lub przedłużonym podawaniu leku lub wynikać z połączenia dwóch lub więcej leków. Znaczenie tego terminu różni się od terminu „ skutek uboczny ”, ponieważ skutki uboczne mogą być zarówno korzystne, jak i szkodliwe. Badanie działań niepożądanych jest przedmiotem zainteresowania dziedziny znanej jako nadzór nad bezpieczeństwem farmakoterapii . Zdarzenie niepożądane ( AE ) odnosi się do każdego nieoczekiwanego i niewłaściwego zdarzenia w czasie stosowania leku, niezależnie od tego, czy jest ono związane z podawaniem leku, czy też nie. ADR jest szczególnym typem zdarzenia niepożądanego, w którym można wykazać związek przyczynowy. Działania niepożądane to tylko jeden rodzaj szkód związanych z lekami, ponieważ szkoda może być również spowodowana zaniechaniem przyjmowania wskazanych leków.
Klasyfikacja
Działania niepożądane można sklasyfikować np. według przyczyny i ciężkości.
Przyczyna
- Typ A: Zwiększone działanie farmakologiczne – zależne od dawki i przewidywalne Reakcje typu A, które stanowią około 80% działań niepożądanych leku, są
- zwykle konsekwencją pierwotnego działania farmakologicznego leku ( np . leku (np. nudności wywołane digoksyną ) i dlatego są przewidywalne. Są zależne od dawki i zwykle łagodne, chociaż mogą być poważne, a nawet śmiertelne (np. krwawienie wewnątrzczaszkowe po warfarynie). Takie reakcje są zwykle spowodowane niewłaściwym dawkowaniem, zwłaszcza gdy zaburzona jest eliminacja leku. Termin „skutki uboczne” jest często stosowany w odniesieniu do drobnych reakcji typu A.
- Typ B : Idiosynkratyczny
Typy A i B zostały zaproponowane w latach 70. XX wieku, a pozostałe typy zaproponowano później, gdy dwa pierwsze okazały się niewystarczające do sklasyfikowania ADR.
Powaga
Amerykańska Agencja ds. Żywności i Leków definiuje poważne zdarzenie niepożądane jako takie, którego wynik u pacjenta jest jednym z następujących:
- Śmierć
- Zagrażający życiu
- Hospitalizacja (początkowa lub przedłużona)
- Niepełnosprawność – znacząca, uporczywa lub trwała zmiana, upośledzenie, uszkodzenie lub zakłócenie funkcji/struktury ciała pacjenta, aktywności fizycznej lub jakości życia.
- Wrodzona nieprawidłowość
- Wymaga interwencji, aby zapobiec trwałemu upośledzeniu lub uszkodzeniu
Nasilenie to punkt na arbitralnej skali intensywności danego zdarzenia niepożądanego. Terminy „poważne” i „poważne”, stosowane do zdarzeń niepożądanych, są technicznie bardzo różne. Można je łatwo pomylić, ale nie można ich używać zamiennie, co wymaga ostrożności podczas użytkowania.
Ból głowy jest ciężki, jeśli powoduje intensywny ból. Istnieją skale, takie jak „wizualna skala analogowa”, które pomagają klinicystom ocenić nasilenie. Z drugiej strony, ból głowy zwykle nie jest poważny (ale może nim być w przypadku krwotoku podpajęczynówkowego, krwawienia podtwardówkowego, a nawet migrena może tymczasowo spełniać kryteria), chyba że spełnia również kryteria ciężkości wymienione powyżej.
Lokalizacja
Działania niepożądane mogą być miejscowe, tj. ograniczone do określonej lokalizacji, lub ogólnoustrojowe, gdy lek spowodował działania niepożądane w całym krążeniu ogólnoustrojowym .
Na przykład niektóre leki przeciwnadciśnieniowe do oczu powodują skutki ogólnoustrojowe, chociaż podaje się je miejscowo w postaci kropli do oczu , ponieważ część przedostaje się do krążenia ogólnoustrojowego.
Mechanizmy
Ponieważ badania lepiej wyjaśniają biochemię zażywania narkotyków, mniej ADR jest typu B, a więcej typu A. Typowe mechanizmy to:
- Nieprawidłowa farmakokinetyka z powodu
- czynniki genetyczne
- współistniejące stany chorobowe
-
synergiczne między nimi
- lek i choroba
- dwa leki
-
antagonizmu między obydwoma
- lek i choroba
- dwa leki
Nieprawidłowa farmakokinetyka
Stany chorobowe współistniejące
Różne choroby, zwłaszcza te, które powodują niewydolność nerek lub wątroby , mogą zmieniać metabolizm leków. Dostępne są zasoby opisujące zmiany w metabolizmie leków spowodowane stanami chorobowymi.
Narzędzia Odpowiedniości Leków dla Współwystępujących Warunków Zdrowotnych w Demencji ( MATCH-D ) ostrzegają, że osoby z demencją są bardziej narażone na wystąpienie działań niepożądanych i że jest mniej prawdopodobne, że będą w stanie wiarygodnie zgłaszać objawy.
Czynniki genetyczne
Nieprawidłowy metabolizm leku może być spowodowany dziedzicznymi czynnikami utleniania fazy I lub koniugacji fazy II. Farmakogenomika to nauka o dziedzicznych podstawach nieprawidłowych reakcji na leki.
Reakcje fazy I
Dziedziczenie nieprawidłowych alleli cytochromu P450 może zmienić metabolizm leków. Dostępne są tabele umożliwiające sprawdzenie interakcji lekowych w związku z interakcjami P450.
Dziedziczenie nieprawidłowej butyrylocholinoesterazy ( pseudocholinesterazy ) może wpływać na metabolizm leków, takich jak sukcynylocholina
Reakcje fazy II
Dziedziczenie nieprawidłowej N -acetylotransferazy , która sprzęgała niektóre leki w celu ułatwienia ich wydalania, może wpływać na metabolizm leków, takich jak izoniazyd , hydralazyna i prokainamid .
Dziedziczenie nieprawidłowej S -metylotransferazy tiopuryny może wpływać na metabolizm leków tiopurynowych , merkaptopuryny i azatiopryny .
Interakcje z innymi lekami
Ryzyko interakcji lekowych jest zwiększone w przypadku polipragmazji .
Wiązanie białek
Te interakcje są zwykle przejściowe i łagodne, aż do osiągnięcia nowego stanu stacjonarnego. Są to głównie leki bez znacznego metabolizmu pierwszego przejścia przez wątrobę. Głównymi białkami osocza wiążącymi leki są:
- albumina
- α1-kwaśna glikoproteina
- lipoproteiny
Niektóre interakcje leków z warfaryną wynikają ze zmian w wiązaniu białek.
Cytochrom P450
Pacjenci mają nieprawidłowy metabolizm przez cytochrom P450 z powodu dziedziczenia nieprawidłowych alleli lub interakcji lekowych. Dostępne są tabele umożliwiające sprawdzenie interakcji lekowych w związku z interakcjami P450.
Efekty synergiczne
Przykładem synergizmu są dwa leki, które wydłużają odstęp QT .
Ocena przyczynowości
Ocena związku przyczynowego służy do określenia prawdopodobieństwa, że lek spowodował podejrzewane działanie niepożądane. Istnieje wiele różnych metod oceny związku przyczynowego, w tym algorytm Naranjo , algorytm Venulet i kryteria oceny terminu przyczynowości WHO. Każda z nich ma zalety i wady związane z ich użyciem, a większość z nich wymaga pewnego poziomu oceny eksperta, aby zastosować. ADR nie powinien być oznaczony jako „pewny”, chyba że ADR ustąpi po zastosowaniu prowokacja-odstawienie-ponowna prowokacja (zatrzymanie i rozpoczęcie danego środka). Ważna jest chronologia wystąpienia podejrzewanego działania niepożądanego, ponieważ przyczyną może być inna substancja lub czynnik; współprzepisane leki i współistniejące choroby psychiczne mogą być czynnikami powodującymi ADR.
Przypisanie przyczynowości do konkretnego czynnika często okazuje się trudne, chyba że zdarzenie zostanie znalezione podczas badania klinicznego lub zostaną użyte duże bazy danych. Obie metody mają trudności i mogą być obarczone błędami. Nawet w badaniach klinicznych niektóre działania niepożądane mogą zostać pominięte, ponieważ do wykrycia tej niepożądanej reakcji na lek wymagana jest duża liczba badanych osób. Psychiatryczne działania niepożądane są często pomijane, ponieważ są one grupowane w kwestionariuszach stosowanych do oceny populacji.
Organy monitorujące
W wielu krajach istnieją oficjalne organy monitorujące bezpieczeństwo leków i reakcje na nie. Na poziomie międzynarodowym WHO prowadzi Centrum Monitorowania w Uppsali , a Unia Europejska prowadzi Europejską Agencję Leków (EMA). W Stanach Zjednoczonych za monitorowanie badań postmarketingowych odpowiada Agencja ds. Żywności i Leków (FDA ) . W Kanadzie za nadzór nad wprowadzanymi do obrotu produktami zdrowotnymi odpowiada Dyrekcja ds. Produktów Zdrowotnych wprowadzonych na rynek w Kanadzie. W Australii Therapeutic Goods Administration (TGA) prowadzi monitorowanie produktów terapeutycznych po wprowadzeniu ich do obrotu. W Wielkiej Brytanii system żółtej karty został ustanowiony w 1963 roku.
Epidemiologia
Badanie przeprowadzone przez Agencję Badań i Jakości Opieki Zdrowotnej (AHRQ) wykazało, że w 2011 roku środki uspokajające i nasenne były głównym źródłem niepożądanych zdarzeń związanych z lekami obserwowanych w warunkach szpitalnych. Około 2,8% wszystkich ADE obecnych przy przyjęciu i 4,4% ADE powstałych podczas pobytu w szpitalu było spowodowanych lekiem uspokajającym lub nasennym. Drugie badanie przeprowadzone przez AHRQ wykazało, że w 2011 roku najpowszechniej zidentyfikowanymi przyczynami działań niepożądanych związanych z lekami, które powstały podczas pobytu w szpitalu w USA, były sterydy, antybiotyki, opiaty/narkotyki i antykoagulanty. Pacjenci leczeni w miejskich szpitalach klinicznych mieli wyższy odsetek ADE związanych z antybiotykami i opiatami/narkotykami w porównaniu z pacjentami leczonymi w miejskich szpitalach niepedagogicznych. Osoby leczone w prywatnych szpitalach non-profit miały wyższy wskaźnik większości przyczyn ADE w porównaniu z pacjentami leczonymi w publicznych lub prywatnych szpitalach nastawionych na zysk.
MRH występuje często po wypisie ze szpitala u osób starszych, ale niespójności metodologiczne między badaniami i niedostatek danych na temat czynników ryzyka ograniczają jasne zrozumienie epidemiologii. Występował szeroki zakres częstości występowania, od 0,4% do 51,2% uczestników, a od 35% do 59% szkód można było zapobiec. Częstość występowania szkód związanych z lekami w ciągu 30 dni po wypisie wahała się od 167 do 500 zdarzeń na 1000 osób wypisanych (17–51% osób).
W Stanach Zjednoczonych kobiety miały wyższy wskaźnik ADE związanych z opiatami i narkotykami niż mężczyźni w 2011 r., Podczas gdy pacjenci płci męskiej mieli wyższy wskaźnik ADE przeciwzakrzepowych. Prawie 8 na 1000 dorosłych w wieku 65 lat lub starszych doświadczyło jednego z czterech najczęstszych ADE (steroidy, antybiotyki, opiaty/narkotyki i antykoagulanty) podczas hospitalizacji. Badanie wykazało, że u 48% pacjentów wystąpiła niepożądana reakcja na co najmniej jeden lek, a zaangażowanie farmaceuty pomaga wykryć niepożądane reakcje na lek.
W 2012 roku firma McKinsey & Company doszła do wniosku, że koszt 50-100 milionów możliwych do uniknięcia zdarzeń niepożądanych leków związanych z błędami wyniesie od 18 do 115 miliardów USD.
Zobacz też
- Rzekome problemy w procesie zatwierdzania leków
- Klasyfikacja skierowań farmakoterapeutycznych
- Problemy farmakoterapii
- EudraVigilance ( Unia Europejska )
- Historia farmacji
- Jatrogeneza
- Dawka śmiertelna
- Lista wycofanych leków
- Reakcja paradoksalna
- Polipragmazja
- Toksyczność
- Toksykologia
- Pismo medyczne w sprawie leków i środków terapeutycznych
- System żółtej kartki (Wielka Brytania)
Dalsza lektura
- Częstość występowania działań niepożądanych u pacjentów zakażonych wirusem niedoboru odporności u ludzi stosujących wysoce aktywną terapię przeciwretrowirusową PMC 3312730
Linki zewnętrzne