zapalenie wysp trzustkowych
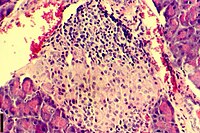 | |
| Insulitis | |
|---|---|
| Obraz histologiczny nacieku zapalnego wysp Langerhansa trzustki | |
| Wymowa | |
| Specjalność | Endokrynologia |
| Komplikacje | Może prowadzić do utraty funkcji komórek beta i może prowadzić do cukrzycy typu 1 |
| Powoduje | Naciek komórek odpornościowych w wysepkach Langerhansa |
| Kierownictwo | przeszczep komórek wysp trzustkowych |
| Częstotliwość | Występuje u 19% osób z T1D i 28% osób z T2D |
trzustkowych to zapalenie wysepek Langerhansa , zbioru tkanki wewnątrzwydzielniczej zlokalizowanej w trzustce , która pomaga regulować poziom glukozy i jest sklasyfikowane na podstawie swoistego naciekania komórek odpornościowych ( limfocytów T i B , makrofagów i komórek dendrytycznych ) w wysepkach trzustkowych. Langerhansa. Ta infiltracja komórek odpornościowych może spowodować zniszczenie komórek beta produkujących insulinę wysp trzustkowych, który odgrywa główną rolę w patogenezie, rozwoju choroby cukrzycy typu 1 i typu 2 . Zapalenie wysp trzustkowych występuje u 19% osób z cukrzycą typu 1 i 28% osób z cukrzycą typu 2 . Wiadomo, że czynniki genetyczne i środowiskowe przyczyniają się do inicjacji zapalenia wysp trzustkowych, jednak dokładny proces, który je wywołuje, nie jest znany. Zapalenie wysp trzustkowych jest często badane przy użyciu myszy z cukrzycą bez otyłości (NOD). model cukrzycy typu 1. Rodzina białek chemokin może odgrywać kluczową rolę w promowaniu nacieku leukocytów do trzustki przed zniszczeniem komórek beta trzustki.
Patofizjologia
Patogenezę zapalenia wysp trzustkowych można ocenić na podstawie progu liczby komórek CD3+ lub CD45+ otaczających lub naciekających wysepki Langerhansa, jednak można to zbadać jedynie za pomocą próbki tkanki trzustki. CD3+ i CD45+ (skupisko komórek różnicowania 3 i 45 dodatnich) to limfocyty. Badanie nieotyłych myszy z cukrzycą ujawniło korelację między postępem zapalenia wysp trzustkowych a ilością autoprzeciwciał insulinowych produkcji w krwioobiegu, jak również związek między pewnymi kombinacjami obecnych autoprzeciwciał a ryzykiem rozwoju cukrzycy typu 1 i zapalenia wysp trzustkowych.
Zapalenie wysp trzustkowych, które występuje u około 19% pacjentów z cukrzycą typu 1, najczęściej występuje w pierwszym roku po rozpoznaniu u pacjentów w wieku od 0 do 14 lat z częstością występowania wynoszącą 68% (32/47 badanych pacjentów). Częstość występowania zapalenia wysp trzustkowych wynosi 4% u młodych pacjentów z przewlekłą cukrzycą typu 1 (pacjenci, którzy chorują na tę chorobę od ponad roku). Tylko u 29% starszych pacjentów w wieku od 15 do 39 lat wykazano zmianę insulityczną w ciągu roku od rozpoznania. Dokładna przyczyna tej rozbieżności między grupami wiekowymi nie jest znana, jednak istnieje teoria, że dorośli mogą mieć inną lub mniej ciężką postać cukrzycy typu 1, która postępuje wolniej.
Istnieją 2 różne podklasyfikacje zapalenia wysp trzustkowych, zapalenia okołowyspowego i zapalenia wewnątrzwyspowego, które różnią się w zależności od lokalizacji nacieku komórek odpornościowych. W zapaleniu okołowyspowym naciek komórkowy występuje na obrzeżach wysepek, podczas gdy w zapaleniu wewnątrzwyspowym ma naciek komórkowy w miąższu, tkance funkcjonalnej wysepki. Często w zapaleniu okołowyspowym naciek komórkowy w koncentracji na 1 biegunie wysepki.
Diagnoza
Istnieje istotna korelacja między częstością występowania zapalenia wysp trzustkowych a komórkami CD45+, CD3+, CD4+ , CD8+ i CD20+ w obrębie zmiany zapalnej wysp trzustkowych , a w społeczności naukowej panuje powszechna zgoda co do tego, że zmiana w wysepkach Langerhansa może zostać zdiagnozowana jako zapalenie wysp trzustkowych, jeśli spełnia minimalny próg infiltracji co najmniej 3 wysepek, z których każda zawiera co najmniej 15 komórek CD45+. W jednym badaniu, którego celem było określenie częstości występowania osób z cukrzycą typu 2, które spełniły wymagania diagnostyczne zapalenia wysp trzustkowych, stwierdzono, że obecna definicja i wymagania dotyczące zapalenia wysp trzustkowych nie mogą być stosowane do „odróżnienia trzustek pobranych od osób z cukrzycą typu 1 od osób z cukrzycą typu 2”. cukrzyca” (Lundberg i in., 2017). W badaniu tym zaproponowano zmianę przyjętej definicji zapalenia wysp trzustkowych, tak aby pozytywna diagnoza występowała, gdy „≥ 15 komórek CD3+, a nie komórek CD45+, znajduje się w ≥ 3 wysepkach” (Lundberg i in., 2017), co zmniejszyło odsetek typu 2 chorych na cukrzycę spełniających kryteria zapalenia wysp trzustkowych od 82% do 28%.
Podstawowym wyzwaniem w badaniu patogenezy zapalenia wysp trzustkowych oraz cukrzycy typu 1 i 2 jest brak zgody co do definicji i warunków diagnostycznych zapalenia wysp trzustkowych. Ten brak konsensusu istnieje, ponieważ istnieje wiele różnych immunofenotypowania i progów nacieków komórkowych stosowanych do odróżnienia zapalenia wysp trzustkowych od innych stanów zapalnych, a ze względu na niewielką wielkość próby dostępnej do badania, istnieje wiele badań skupionych na wyraźniejszej identyfikacji cech zapalenia wysp trzustkowych .
Ze względu na to, że wysepki Langerhansa są małymi skupiskami komórek w trzustce, badanie i diagnozowanie zapalenia wysp trzustkowych jest trudne, ponieważ wymaga pobrania raportu patologicznego na próbkach tkanki wysepek Langerhansa od dawcy, a od 2014 r. było tylko badanie histopatologiczne dane z ~250 przypadków. Strategia badania wczesnego rozwoju cukrzycy typu 1 i prawdopodobnego rozwoju zapalenia wysp trzustkowych polega na wykonaniu badania krwi w celu zmierzenia poziomu autoprzeciwciał wysp trzustkowych w krążeniu danej osoby. Rozpoznanie zapalenia wysp trzustkowych może również nastąpić na podstawie obrazowania zmian zapalnych wysp trzustkowych za pomocą obrazowania radiologicznego lub obrazowania optycznego , jednak główna trudność w diagnozowaniu zapalenia wysp trzustkowych na podstawie obrazów wynika z trudności w wykryciu wysepek trzustkowych w tkance trzustki. Techniki obrazowania radiologicznego obejmują obrazowanie metodą rezonansu magnetycznego (MRI) , ultradźwięki i tomografię komputerową .
Leczenie
Terapia immunosupresyjna podawana na wczesnym etapie rozwoju zapalenia wysp trzustkowych
To leczenie byłoby skuteczne, gdyby zostało zastosowane na wczesnym etapie rozwoju zapalenia wysp trzustkowych. Gdyby zapalenie wysp trzustkowych i rozwój cukrzycy typu 1 udało się wykryć metodą nieinwazyjną przed rozległą utratą komórek beta wydzielających insulinę, zastosowanie leczenia immunosupresyjnego zapobiegłoby naciekowi komórek odpornościowych do wysepek Langerhansa. To zapobieganie zapaleniu wysp trzustkowych służyłoby również jako zapobieganie rozwojowi cukrzycy typu 1, ponieważ jeśli nie dochodzi do niszczenia komórek beta produkujących insulinę, organizm będzie w stanie wytworzyć wystarczający poziom glukozy.
Allogeniczny przeszczep komórek wysp trzustkowych
W tej procedurze chirurgicznej komórki wysp trzustkowych są uzyskiwane od dawców ze śmiercią mózgu (często wymaganych jest 2 dawców) i podawane w infuzji do wątroby pacjenta w celu zastąpienia zniszczonych wysepek u pacjenta. Pacjent rozpoczyna również terapię immunosupresyjną, aby zapobiec uszkodzeniu przeszczepionych komórek przez układ odpornościowy pacjenta. Przeszczep odbywa się w znieczuleniu miejscowym, a cewnik pod kontrolą obrazu jest wprowadzany przezskórnie do żyły wrotnej , naczynia krwionośnego, które transportuje krew do wątroby. Pierwsza odnotowana transplantacja miała miejsce w 1977 roku.
Procedura pokazuje krótkoterminowy sukces z pewnymi dowodami długoterminowego sukcesu. W przypadku powodzenia procedura ta skutkuje znaczną poprawą kontroli cukrzycy i zmniejszeniem hipoglikemii epizody, co wskazuje, że wszczepione komórki beta wysp trzustkowych produkujące insulinę skutecznie wytwarzają i wydzielają insulinę na wymaganym poziomie. W badaniu rejestrowym 112 pacjentów przeszczep wysp trzustkowych zakończył się niepowodzeniem u 13% pacjentów, a 76% pacjentów było zależnych od insuliny w ciągu 2 lat od zabiegu. Niski wskaźnik sukcesu przeszczepu może być spowodowany niewystarczającą liczbą wszczepionych komórek wysp trzustkowych, niepowodzeniem przeszczepu komórek wysp trzustkowych, uszkodzeniem komórek wysp trzustkowych w wątrobie, nieskuteczną immunosupresją i nawracającą cukrzycą autoimmunologiczną. Procedura ta może wiązać się z poważnymi powikłaniami, jednak większość procedur transplantacyjnych nie powoduje żadnych skutków ubocznych dla pacjentów. Istnieje również ryzyko wystąpienia działań niepożądanych wynikających z długotrwałego stosowania terapii immunosupresyjnej. Chociaż wskaźniki powodzenia tej procedury rosną od czasu jej pierwszego wykonania, procedura ta często nie jest oferowana ze względu na wysoki wskaźnik odrzucenia przez organizm pacjenta i długoterminowe ryzyko leczenia immunosupresyjnego.
Autologiczny przeszczep komórek wysp trzustkowych
Ta procedura chirurgiczna jest podobna do allogenicznego przeszczepu komórek wysp trzustkowych , z główną różnicą polegającą na tym, skąd pozyskiwane są wszczepione wyspy trzustkowe. W autologicznym przeszczepie komórek wysp trzustkowych komórki wysp trzustkowych uzyskuje się od pacjenta, podczas gdy w allogenicznym przeszczepie komórek wysp trzustkowych komórki wysp trzustkowych uzyskano od dawców.
Zabieg ten wykonywany jest wraz z pankreatektomią w znieczuleniu ogólnym . Najpierw wykonywana jest pankreatektomia, przy czym cała trzustka jest usuwana tylko w bardziej ekstremalnych przypadkach, takich jak wyniszczający ból spowodowany przewlekłym zapaleniem trzustki, następnie izolowane są żywe komórki wysp trzustkowych i wszczepiane do wątroby pacjenta przez żyłę wrotną za pomocą cewnika kierowanego obrazem. Ponieważ wszczepione komórki wysp trzustkowych pochodzą z organizmu pacjenta, nie ma odrzucenia immunologicznego i nie ma potrzeby leczenia immunosupresyjnego.
Ta procedura wykazuje krótkotrwały sukces w poprawie zarządzania poziomem cukru we krwi pacjenta, ale w dłuższej perspektywie większość pacjentów wymaga insulinoterapii. Powikłania wynikające z tej procedury wynikają przede wszystkim z wycięcia trzustki.
Historia
Zapalenie wysp trzustkowych zostało po raz pierwszy opisane w 1902 roku przez niemieckiego patologa Martina Benno Schmidta, a później nazwane zapaleniem wysp trzustkowych przez szwajcarskiego patologa Hannsa von Meyenburga w 1940 roku. -letnie dziecko z cukrzycą. Uważano, że zapalenie wysp trzustkowych jest rzadkim schorzeniem do 1928 roku, kiedy naukowcy Oliver Stansfield i Shields Warren odkryli korelację między zapaleniem wysp trzustkowych a wiekiem pacjentów w badaniu kilku młodych dzieci z cukrzycą, które zmarły wkrótce po rozpoznaniu cukrzycy. Młodzi pacjenci byli głównym celem ich badań, ponieważ dzieci mają „najlepsze przykłady czystej, niepowikłanej cukrzycy” (In't Veld, 2011) i mają mniej powikłań, które pojawiają się wraz z wiekiem. Oprócz powiązania zapalenia wysp trzustkowych z wiekiem, Stansfield i Warren odkryli korelację między zapaleniem wysp trzustkowych a nagłym początkiem (<1 roku) cukrzycy typu 1. Warren zauważył również, że zapalenie wysp trzustkowych nie zawsze występowało u pacjentów z cukrzycą, dochodząc do wniosku, że ponieważ zapalenie wysp trzustkowych nie występowało w prostych przypadkach cukrzycy, zapalenie wysp trzustkowych nie powodowało cukrzycy, było jedynie jej objawem.
W 1958 roku Philip LeCompte ponownie zbadał chorobę o ostrym początku i krótkim czasie trwania, badając 4 powiązane przypadki zapalenia wysp trzustkowych. LeCompte wysunął teorię, że zapalenie wysp trzustkowych było rzadką, ale znaczącą zmianą, która mogła być niedodiagnozowana, a naciek komórkowy mógł być spowodowany czynnikiem infekcyjnym, funkcjonalnym szczepem wysepek, reakcją na uszkodzenie ze źródła innego niż bakteryjne lub antygenem -reakcja przeciwciał W 1965 roku patolog Willy Gepts spekulował na temat możliwego pochodzenia immunologicznego zapalenia wysp trzustkowych, kiedy opublikował pierwszą analizę dotyczącą zapalenia wysp trzustkowych i cukrzycy młodzieńczej na stosunkowo dużej próbie, 22 pacjentów. Wszyscy 22 badani pacjenci zmarli w ciągu 6 miesięcy od postawienia diagnozy, a Gepts stwierdził obecność zapalenia wysp trzustkowych u 68% (15/22) pacjentów, co było istotne, ponieważ wykazywało znacznie wyższą częstość występowania niż wcześniej stwierdzono. W kolejnym badaniu Gepts stwierdził również wysoce zmienną redukcję masy komórek beta trzustki, średnio o około 10% mniejszą niż u osób kontrolnych bez cukrzycy, tendencję do występowania stanów zapalnych w wysepkach, które nadal miały immunoreaktywność insuliny, i dalsze dowody procesu autoimmunologicznego w pracy. Dalsze badania przeprowadzone w 1978 roku doprowadziły Geptsa do wniosku, że „zapalenie wysp trzustkowych jest reakcją immunologiczną typu opóźnionego, specyficznie skierowaną przeciwko komórkom beta” (In't Veld, 2011). Badania nad chorobami trzustki prowadzone od lat dwudziestych do siedemdziesiątych XX wieku ujawniły wiele rzeczy na temat zapalenia wysp trzustkowych, a w połączeniu z badaniami immunologicznymi i genetycznymi na pacjentach z cukrzycą typu 1 wskazały na związek między zapaleniem wysp trzustkowych a cukrzycą typu 1 oraz autoimmunologicznym podłożem cukrzycy typu 1.
