systemu Bethesdy
System Bethesda ( TBS ), oficjalnie nazywany The Bethesda System for Reporting Cervical Cytology , to system zgłaszania diagnoz cytologicznych szyjki macicy lub pochwy , używany do zgłaszania wyników cytologii . Został wprowadzony w 1988 roku i poprawiony w 1991, 2001 i 2014 roku. Nazwa pochodzi od lokalizacji ( Bethesda, Maryland ) konferencji sponsorowanej przez National Institutes of Health , która ustanowiła system.
Od 2010 roku istnieje również system Bethesda służący do cytopatologii guzków tarczycy , który nosi nazwę The Bethesda System for Reporting Thyroid Cytopatology (TBSRTC lub BSRTC). Podobnie jak TBS, powstał w wyniku konferencji sponsorowanej przez NIH i jest publikowany w wydaniach książkowych (obecnie Springer). Wzmianki o „systemie Bethesda” bez dalszych specyfikacji zwykle odnoszą się do układu szyjki macicy, chyba że kontekst dyskusji dotyczący tarczycy jest dorozumiany.
Szyjka macicy
Nieprawidłowe wyniki obejmują: [ potrzebne źródło ]
- Nietypowe komórki płaskonabłonkowe
- Nietypowe komórki płaskonabłonkowe o nieokreślonym znaczeniu (ASC-US)
- Nietypowe komórki płaskonabłonkowe – nie można wykluczyć HSIL (ASC-H)
- Zmiany śródnabłonkowe niskiego stopnia (LGSIL lub LSIL)
- Zmiany śródnabłonkowe dużego stopnia (HGSIL lub HSIL)
- Rak kolczystokomórkowy
- Nietypowe komórki gruczołowe niewymienione inaczej (AGC-NOS)
- Nietypowe komórki gruczołowe, podejrzane o AIS lub raka (AGC-nowotwór)
- Gruczolakorak in situ (AIS)
Wyniki są obliczane inaczej po badaniu cytologicznym szyjki macicy . [ potrzebne źródło ]
Nieprawidłowości komórek płaskonabłonkowych
LSIL: śródnabłonkowa zmiana płaskonabłonkowa niskiego stopnia

Zmiany śródnabłonkowe niskiego stopnia (LSIL lub LGSIL) wskazują na możliwą dysplazję szyjki macicy . LSIL zwykle wskazuje na łagodną dysplazję (CIN 1), najprawdopodobniej spowodowaną wirusem brodawczaka ludzkiego . Zwykle diagnozuje się go po badaniu cytologicznym . [ potrzebne źródło ]
CIN 1 jest najczęstszą i najbardziej łagodną postacią śródnabłonkowej neoplazji szyjki macicy i zwykle ustępuje samoistnie w ciągu dwóch lat. Z tego powodu wynikami LSIL można zarządzać za pomocą prostej filozofii „obserwuj i czekaj”. Jednakże, ponieważ istnieje 12-16% szans na progresję do cięższej dysplazji, lekarz może chcieć bardziej agresywnie śledzić wyniki, wykonując kolposkopię z biopsją . Jeśli dysplazja postępuje, konieczne może być leczenie. Leczenie obejmuje usunięcie dotkniętej tkanki, co można osiągnąć za pomocą LEEP , kriochirurgii , biopsji stożkowej lub ablacji laserowej. [ potrzebne źródło ]
HSIL: śródnabłonkowa zmiana płaskonabłonkowa dużego stopnia

Śródnabłonkowa zmiana śródnabłonkowa dużego stopnia (HSIL lub HGSIL) wskazuje na umiarkowaną lub ciężką śródnabłonkową neoplazję szyjki macicy lub raka in situ . Zwykle diagnozuje się go po badaniu Pap . W niektórych przypadkach te zmiany mogą prowadzić do inwazyjnego raka szyjki macicy , jeśli nie są odpowiednio przestrzegane. [ potrzebne źródło ]
HSIL nie oznacza obecności raka. Spośród wszystkich kobiet z wynikami HSIL 2% lub mniej miało w tym czasie inwazyjnego raka szyjki macicy, jednak około 20% bez leczenia rozwinęłoby się w inwazyjnego raka szyjki macicy. Aby zwalczyć tę progresję, po HSIL zwykle następuje natychmiastowa kolposkopia z biopsją w celu pobrania próbki lub usunięcia tkanki dysplastycznej. Ta tkanka jest wysyłana do patologicznych w celu przypisania klasyfikacji histologicznej , która jest bardziej definitywna niż wynik wymazu cytologicznego (który jest odkryciem cytologicznym ). HSIL ogólnie odpowiada klasyfikacji histologicznej CIN 2 lub 3 . [ potrzebne źródło ]
Leczenie HSIL polega na usunięciu lub zniszczeniu dotkniętych komórek, zwykle przez LEEP . Inne metody obejmują krioterapię , kauteryzację lub ablację laserową, ale żadnej nie wykonuje się u kobiet w ciąży z obawy przed przerwaniem ciąży. Każda z tych procedur ma 85% szans na wyleczenie problemu.
Nieprawidłowości komórek gruczołowych
Rak gruczołowy

Gruczolakorak może powstać z szyjki macicy, endometrium i miejsc pozamacicznych. [ potrzebne źródło ]
AGC
AGC, dawniej AGUS, to termin określający atypowe komórki gruczołowe o nieokreślonym znaczeniu . Zmieniono nazwę AGC, aby uniknąć pomyłki z ASCUS.
Leczeniem AGC jest kolposkopia z biopsją endometrium lub bez niej .
Guzki tarczycy
Bethesda System for Reporting Thyroid Cytopatology to system używany do zgłaszania, czy próbka cytologiczna tarczycy jest łagodna czy złośliwa w cytologii aspiracyjnej cienkoigłowej (FNAC). Można go podzielić na sześć kategorii:
| Kategoria | Opis | Ryzyko nowotworu złośliwego | Rekomendacje |
|---|---|---|---|
| I | Niediagnostyczny/niezadowalający | - | Powtórzenie FNAC pod kontrolą USG za ponad 3 miesiące |
| II | Łagodne (komórki koloidalne i pęcherzykowe) | 0 - 3% | Obserwacja kliniczna |
| III | Atypia o nieokreślonym znaczeniu/zmiana pęcherzykowa o nieokreślonym znaczeniu (komórki pęcherzykowe lub limfoidalne o nietypowych cechach) | 5 - 15% | Powtarzanie FNAC |
| IV | Guzek pęcherzykowy/podejrzany guzek pęcherzykowy (stłoczenie komórek, mikropęcherzyki, rozproszone izolowane komórki, niewielka ilość koloidu) | 15 - 30% | Lobektomia chirurgiczna |
| V | Podejrzany o złośliwość | 60 - 75% | Lobektomia chirurgiczna lub prawie całkowita tyreoidektomia |
| VI | Złośliwy | 97 - 99% | Prawie całkowite wycięcie tarczycy |
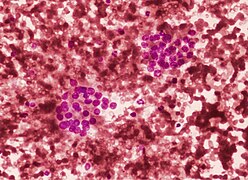
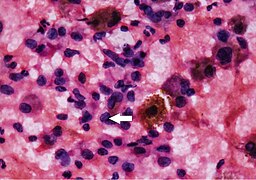
Cytopatologia podejrzana w kierunku nowotworu z komórek Hürthle'a (kategoria Bethesda IV, raczej niż hiperplazja komórek Hürthle'a), barwienie cytologiczne.
Powtórzenie FNAC jest zalecane dla Kategorii I, następnie obserwacja kliniczna Kategorii II, powtórna FNAC Kategorii III i lobektomia Kategorii IV, prawie całkowita tyreoidektomia/lobektomia Kategorii V i prawie całkowita tyreoidektomia Kategorii VI. Ryzyko złośliwości w złośliwym raporcie FNAC wynosi 93,7%, podczas gdy w przypadku podejrzanego raportu FNAC wynosi 18,9%.
Zobacz też
Linki zewnętrzne
- ASCP: Atlas witryn internetowych systemu Bethesda
- Warsztat Bethesdy 2001
- Bongiovanni, Massimo; Spitale, Aleksandra; Faquin, William C.; Mazzucchelli, Luca; Baloch, Zubair W. (2012). „System Bethesda do zgłaszania cytopatologii tarczycy: metaanaliza” . Acta Cytologica . 56 (4): 333–339. doi : 10.1159/000339959 . PMID 22846422 . S2CID 14143335 . Źródło 24 listopada 2022 r .

![Cytopathology suspicious for Hürthle cell neoplasm (Bethesda category IV, rather than Hürthle cell hyperplasia), Pap stain.[14]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/65/Cytopathology_suspicious_for_H%C3%BCrthle_cell_neoplasm%2C_annotated.png/436px-Cytopathology_suspicious_for_H%C3%BCrthle_cell_neoplasm%2C_annotated.png)