Allilowanie karbonylu
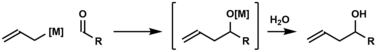
W chemii organicznej allilowanie karbonylem opisuje metody dodawania anionu allilowego do aldehydu lub ketonu w celu wytworzenia alkoholu homoallilowego. Allilowanie karbonylu zostało po raz pierwszy opisane w 1876 roku przez Aleksandra Zajcewa i wykorzystywało odczynnik allilocynkowy.
Wersje enancjoselektywne
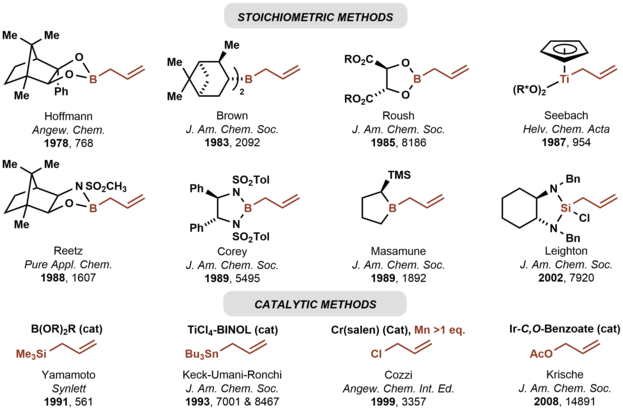
W 1978 roku Hoffmann opisał pierwsze asymetryczne allilowanie karbonylu przy użyciu chiralnego odczynnika allilometalicznego, alliloboranu pochodzącego z kamfory . Takie metody wykorzystują wstępnie uformowane odczynniki z metalami allilowymi. Podejście to jest dobrze rozwinięte przy użyciu boranów allilowych
(13)
Jak ilustruje allilowanie Kecka, katalityczne enancjoselektywne addycje achiralnych odczynników allilowo-metalicznych do związków karbonylowych są również możliwe dzięki dodatkom organostannanów .
Odczynniki boronianu allilu i boranu allilu zostały również opracowane do enancjoselektywnego dodawania karbonyli - w tej klasie reakcji odczynnik allilu boru zapewnia kontrolę stereochemiczną
(13)
Kataliza
W 1991 roku Yamamoto ujawnił pierwszą katalityczną enancjoselektywną metodę allilowania karbonylu, w której zastosowano chiralny borowy kwas-katalizator Lewisa w połączeniu z allilotrimetylosilanem . Następnie zastosowano wiele innych katalitycznych enancjoselektywnych metod allilowania karbonylu. Katalityczne warianty reakcji Nozaki-Hiyama-Kishi stanowią alternatywną metodę asymetrycznego allilowania karbonylu, ale wymagane są stechiometryczne reduktory metaliczne.
Podczas gdy wyżej wymienione asymetryczne allilowanie karbonylowe opiera się na wstępnie uformowanych odczynnikach allilometalicznych, allilowanie Krische wykorzystuje octan allilu do enancjoselektywnego allilowania karbonylu. Wybrane metody asymetrycznego allilowania karbonylu podsumowano poniżej.
Użyj w całkowitej syntezie
Allilowanie karbonylu zostało wykorzystane w syntezie naturalnych produktów poliketydowych i innych utlenionych cząsteczek z ciągłym układem stereocentrów. Na przykład allilostannanowanie aldehydu pochodzącego z treozy daje makrolid antasskomycynę B, która strukturalnie przypomina FK506 i rapamycynę i jest silnym środkiem wiążącym FKBP12. Allilowanie Krischego zastosowano do przygotowania poliketydu (+) -SCH 351448, makrodiolidowego jonoforu zawierającego 14 centrów stereogenicznych.
Starsza literatura pierwotna
- Brązowy, Herbert C.; Jadhav, Prabhakar K. (kwiecień 1983). „Tworzenie asymetrycznego wiązania węgiel-węgiel poprzez β-allilodiizopinokamfeyloboran. Prosta synteza drugorzędowych alkoholi homoallilowych o doskonałych czystościach enancjomerycznych” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 105 (7): 2092–2093. doi : 10.1021/ja00345a085 . ISSN 0002-7863 .
- Hayashi, Tamio; Konishi, Mitsuo; Kumada, Makoto (1982-09-01). „Optycznie czynne allilosilany. 2. Wysoka stereoselektywność w reakcji asymetrycznej z aldehydami wytwarzającymi alkohole homoallilowe”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 104 (18): 4963–4965. doi : 10.1021/ja00382a046 .
- Roush, William R.; Walts, Alan E.; Hoong, Lee K. (1985-12-01). „Diastereo- i enancjoselektywne reakcje addycji aldehydów estrów 2-allilo-1,3,2-dioksaborolano-4,5-dikarboksylowych, użyteczna klasa alliloboronianów modyfikowanych estrem winianowym”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 107 (26): 8186–8190. doi : 10.1021/ja00312a062 .
- Brązowy, Herbert C.; Jadhav, Prabhakar K. (kwiecień 1983). „Tworzenie asymetrycznego wiązania węgiel-węgiel poprzez β-allilodiizopinokamfeyloboran. Prosta synteza drugorzędowych alkoholi homoallilowych o doskonałych czystościach enancjomerycznych” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 105 (7): 2092–2093. doi : 10.1021/ja00345a085 . ISSN 0002-7863 .
- Kinnaird, James WA; Ng, Pui Yee; Kubota, Katsumi; Wang, Xiaolun; Leighton, James L. (2002-07-01). „Napięte silacykle w syntezie organicznej: nowy odczynnik do enancjoselektywnej allilacji aldehydów” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 124 (27): 7920–7921. doi : 10.1021/ja0264908 . ISSN 0002-7863 . PMID 12095334 .
- Krótki, Robert P .; Masamune, Satoru (marzec 1989). „Asymetryczne allilborowanie z B-allilo-2- (trimetylosililo) borolanem” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 111 (5): 1892–1894. doi : 10.1021/ja00187a061 . ISSN 0002-7863 .
- Corey, EJ; Yu, Chan Mo; Kim, Sung Soo (lipiec 1989). „Praktyczna i wydajna metoda enancjoselektywnego allilowania aldehydów” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 111 (14): 5495–5496. doi : 10.1021/ja00196a082 . ISSN 0002-7863 .
- ^ Tak, Miguel; González-Gómez, José C.; Foubelo, Franciszek (2011). „Katalityczne enancjoselektywne allilowanie związków karbonylowych i imin”. Recenzje chemiczne . 111 (12): 7774–7854. doi : 10.1021/cr1004474 . PMID 21923136 .
- Bibliografia _ Sajcew, Aleksander (1877). „Synthese des Allylodimethylcarbinols” . Justus Liebigs Annalen der Chemie . 185 (2–3): 151–169. doi : 10.1002/jlac.18771850204 . ISSN 1099-0690 .
- ^ Herold, Tomasz; Hoffmann, Reinhard W. (1978-10-01). „Enancjoselektywna synteza alkoholi homoallilowych poprzez chiralne estry alliloboronowe”. Angewandte Chemie International Edition w języku angielskim . 17 (10): 768–769. doi : 10.1002/anie.197807682 .
- ^ Hoffmann, Reinhard W.; Herold, Thomas (1981-01-01). „Stereoselektive Synthese von Alkoholen, VII1) Optisch aktive Homoallylalkohole durch Addition chiraler Boronsäureester an Aldehyde”. Chemische Berichte . 114 (1): 375–383. doi : 10.1002/cber.19811140139 .
- ^ a b Dania, SE; Almstead, NG we współczesnej chemii karbonylowej ; Otera, J., wyd.; Wiley-VCH: Weinheim, 2000; Rozdział 10.
- ^ ab Keck, Gary E.; Tarbet, Kenneth H.; Geraci, Leo S. (1993-09-01). „Katalityczne asymetryczne allilowanie aldehydów”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 115 (18): 8467–8468. doi : 10.1021/ja00071a074 .
- ^ Dania, Scott E.; Fu, Jiping (2003-08-01). „Katalityczna enancjoselektywna addycja allilowych odczynników metaloorganicznych do aldehydów i ketonów” . Recenzje chemiczne . 103 (8): 2763–2794. doi : 10.1021/cr020050h . ISSN 0009-2665 . PMID 12914480 .
- Bibliografia _ Mouri, Makoto; Yamamoto, Hisashi (1991-01-01). „Asymetryczne allilowanie aldehydów katalizowane chiralnie (acyloksy) boranem”. Synlett . 1991 (8): 561–562. doi : 10.1055/s-1991-20797 .
- ^ Costa, Anna Luisa; Piazza, Maria Julia; Tagliavini, Emilio; Trombini, Claudio; Umani-Ronchi, Achille (1993-07-01). „Katalityczna asymetryczna synteza alkoholi homoallilowych”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 115 (15): 7001–7002. doi : 10.1021/ja00068a079 .
- ^ Hargaden, Grainne C.; Guiry, Patrick J. (2007-11-05). „Rozwój asymetrycznej reakcji Nozakiego – Hiyamy – Kishiego”. Zaawansowana synteza i kataliza . 349 (16): 2407–2424. doi : 10.1002/adsc.200700324 .
- ^ Kim, w Su; Ngai, Ming-Yu; Krische, Michael J. (2008-11-05). „Enancjoselektywne allilowanie karbonylu katalizowane irydem z poziomu utlenienia alkoholu lub aldehydu poprzez przenoszenie wodorowego sprzęgania octanu allilu: odejście od chiralnie modyfikowanych odczynników allilowych z metalami w dodatku karbonylu” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 130 (44): 14891–14899. doi : 10.1021/ja805722e . ISSN 0002-7863 . PMC 2890235 . PMID 18841896 .
- ^ Brytania, Dominik EA; Griffiths-Jones, Charlotte M.; Linder, Michael R.; Smith, Martin D.; McCusker, Katarzyna; Barlow, Jaqueline S.; Akiyama, Ryo; Yasuda, Kosuke; Ley, Steven V. (2005). „Całkowita synteza Antascomicyny B” . Angewandte Chemie wydanie międzynarodowe . 44 (18): 2732–2737. doi : 10.1002/anie.200500174 . ISSN 1521-3773 . PMID 15806607 .
- ^ Wang, gang; Krische, Michael J. (2016-07-06). „Całkowita synteza (+) -SCH 351448: wydajność dzięki chemoselektywności i gospodarce redoks napędzanej katalizą metali” . Dziennik Amerykańskiego Towarzystwa Chemicznego . 138 (26): 8088–8091. doi : 10.1021/jacs.6b04917 . ISSN 0002-7863 . PMC 4935581 . PMID 27337561 .