Kompleks allilowy metali przejściowych
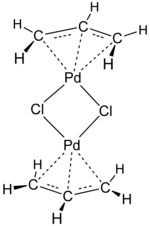
Kompleksy allilowe metali przejściowych to kompleksy koordynacyjne z allilem i jego pochodnymi jako ligandami . Allil jest rodnikiem o łączności CH 2 CHCH 2 , chociaż jako ligand jest zwykle postrzegany jako anion allilowy CH 2 = CH-CH 2 − , który jest zwykle opisywany jako dwie równoważne struktury rezonansowe.
Przykłady
Ligand allilowy jest powszechnie spotykany w chemii metaloorganicznej . Najczęściej ligandy allilowe wiążą się z metalami za pośrednictwem wszystkich trzech atomów węgla, w trybie wiązania η3 . Grupa η 3 -allilowa jest klasyfikowana jako ligand typu LX w schemacie klasyfikacji ligandów Green LXZ , służąc jako 3e – donor przy użyciu liczenia elektronów neutralnych i 4e – donor przy użyciu liczenia elektronów jonowych. Bardziej powszechne są kompleksy z ligandami allilowymi i innymi. Przykłady obejmują (η3 - allil)Mn(CO) 4 i CpPd(allil) .
Kompleksy homoleptyczne
- bis(allilo)nikiel
- bis(allilo)pallad
- bis(allilo)platyna
- tris(allilo)chrom
- tris(allilo)rod
- tris(allilo)iryd
Metody syntetyczne
Kompleksy allilowe są często generowane przez utleniające dodanie halogenków allilowych do kompleksów metali o niskiej wartościowości. Ta droga jest używana do przygotowania (allilu) 2 Ni 2 Cl 2 :
- 2 Ni(CO) 4 + 2 ClCH 2 CH=CH 2 → Ni 2 (μ-Cl) 2 (η 3 -C 3 H 5 ) 2 + 8 CO
Podobna addycja utleniająca obejmuje reakcję bromku allilu z diironononakarbonylem . Utleniającą drogę addycji zastosowano również w przypadku kompleksów allilowych Mo (II):
- Mo(CO) 3 (pirydyna) 3 + BrCH 2 CH=CH 2 → Mo(CO) 2 (Cl)(C 3 H 5 )(pirydyna) 2
Inne metody syntezy polegają na dodaniu nukleofili do kompleksów η 4 -dienowych i absorpcji wodorków z kompleksów alkenowych. Wreszcie ligandy allilowe są wytwarzane w reakcjach metatezy soli , zaczynając od bromku allilomagnezu lub pokrewnych odczynników allilolitowych.
Chelatujące kompleksy bis(allilowe).
1,3- Dieny, takie jak butadien i izopren , dimeryzują w sferach koordynacyjnych niektórych metali, tworząc chelatujące kompleksy bis(allilowe). Takie kompleksy powstają również w wyniku otwarcia pierścienia diwinylocyklobutanu. Chelatujące kompleksy bis (allilowe) są produktami pośrednimi w katalizowanej metalem dimeryzacji butadienu z wytworzeniem winylocykloheksenu i cyklookta-1,5-dienu .
Sigma-ligandy allilowe
kompleksy z ligandami η 1 -allilowymi (klasyfikowanymi jako ligandy typu X). Jednym z przykładów jest CpFe(CO) 2 (η 1 -C 3 H 5 ), w którym tylko grupa metylenowa jest przyłączona do centrum Fe (tj. ma łączność [Fe]–CH 2 –CH=CH 2 ). Podobnie jak w przypadku wielu innych kompleksów η 1 -allilowych, monohaptyczność ligandu allilowego w tym gatunku jest wymuszona przez regułę 18 elektronów , ponieważ CpFe(CO) 2 (η 1 -C 3 H 5 ) jest już kompleksem 18-elektronowym, podczas gdy ligand η3 - allilowy dawałby liczbę elektronów równą 20 i naruszałby regułę 18-elektronową . Takie kompleksy mogą przekształcić się w pochodne η 3 -allilu poprzez dysocjację obojętnego (dwuelektronowego) liganda L. Dla CpFe(CO) 2 (η 1 -C 3 H 5 ) dysocjacja L = CO zachodzi w warunkach fotochemicznych:
- CpFe(CO) 2 (η 1 -C 3 H 5 ) → CpFe(CO)(η 3 -C 3 H 5 ) + CO
kompleksy benzylowe
Ligandy benzylowe i allilowe często wykazują podobne właściwości chemiczne. Ligandy benzylowe zwykle przyjmują tryby wiązania η 1 lub η 3 . Reakcje wzajemnej konwersji są analogiczne do reakcji η 1 - lub η 3 -ligandów allilowych:
- CpFe(CO) 2 (η 1 -CH 2 Ph) → CpFe(CO)(η 3 -CH 2 Ph) + CO
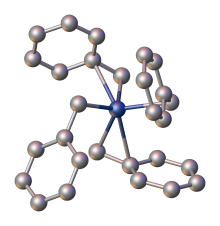
We wszystkich trybach wiązania benzylowy atom węgla jest silniej związany z metalem, na co wskazują odległości wiązań MC, które różnią się o ok. 0,2 Å w kompleksach z wiązaniami η 3 . Krystalografia rentgenowska wykazała, że ligandy benzylowe w tetrabenzylocyrkonie są bardzo elastyczne. Jeden polimorf ma cztery ligandy η2 - benzylowe, podczas gdy inny polimorf ma dwa ligandy η1- i dwa ligandy η2 -benzylowe .
Aplikacje
Pod względem zastosowań popularnym kompleksem allilowym jest chlorek allilopalladu . Ligandy allilowe są podatne na addycję nukleofilową , co może być przydatne w syntezie organicznej .
- ^ a b c d O'Brien, S .; Fishwick, M.; McDermott, B.; Wallbridge, MGH; Wright, GA (1972). „Izoleptyczne pochodne allilowe różnych metali”. Syntezy nieorganiczne . Syntezy nieorganiczne. Tom. 13. s. 73–79. doi : 10.1002/9780470132449.ch14 . ISBN 9780470132449 .
- ^ a b c Kevin D. John; Judith L. Eglin; Kenneth V. Salazar; R. Thomas Baker; Alfreda P. Sattelbergera (2014). Tris(Allilo)Iryd i -Rod . Syntezy nieorganiczne. Tom. 36. str. 165. doi : 10.1002/9781118744994.ch32 . ISBN 9781118744994 .
- ^ Martin F. Semmelhack i Paul M. Helquist (1988). „Reakcja halogenków arylu z halogenkami π-allilniklu: metallilobenzen” . Syntezy Organiczne . ; Tom zbiorowy , obj. 6, str. 722
-
^
Craig R. Smith, Aibin Zhang, Daniel J. Mans, TV Rajanbabu (2008). „(R) -3-metylo-3-fenylo-1-penten poprzez katalityczne asymetryczne hydrowinylowanie” . Org. Syntezator . 85 : 248–266. doi : 10.15227/orgsyn.085.0248 . PMC 2723857 . PMID 19672483 .
{{ cite journal }}: CS1 maint: używa parametru autorów ( link ) - ^ Putnik, Karol F.; Welter, James J.; Stucky, Galen D.; d'Aniello, MJ; Sosiński, BA; Kirner, JF; Muetterties, EL (1978). „Skupiska metali w katalizie. 15. Badanie strukturalne i chemiczne kompleksu metali dwujądrowych, heksakarbonylobis (.eta.3-2-propenylo) diiron (Fe-Fe)”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 100 (13): 4107–4116. doi : 10.1021/ja00481a020 .
- ^ Pearson, Anthony J.; Schoffers, Elke (1997). „Trikarbonyltris (pirydyno) molibden: wygodny odczynnik do przygotowania kompleksów (π-allilowo) molibdenowych”. metaloorganiczne . 16 (24): 5365–5367. doi : 10.1021/om970473n .
- Bibliografia _ Sakate, Yumiko; Komine, Nobuyuki; Komiya, Sanshiro; Wang, Xian-qi; Bennett, Martin A. (2011). „Stechiometryczne regio- i stereoselektywne utleniające reakcje sprzęgania sprzężonych dienów z rutenem (0). Mechanistyczny wgląd w pochodzenie selektywności”. metaloorganiczne . 30 (4): 768–777. doi : 10.1021/om100956f .
- ^ Ryba, RW; Giering, WP; Marten, D.; Rosenblum, M. (1976-01-27). „Termiczne i fotochemiczne interkonwersje izomerycznych kompleksów monokarbonylo-η5-cyklopentadienylo (η3-allilo) żelaza” . Dziennik Chemii metaloorganicznej . 105 (1): 101–118. doi : 10.1016/S0022-328X(00)91977-6 . ISSN 0022-328X .
- ^ ab Rong , Yi; Al-Harbi, Ahmed; Parkin, Gerard (2012). „Wysoce zmienne kąty wiązań Zr – CH 2 –Ph w tetrabenzylocyrkonie: analiza trybów koordynacji liganda benzylowego”. metaloorganiczne . 31 stron = 8208–8217 (23): 8208–8217. doi : 10.1021/om300820b .
- ^ Trost, Barry M.; Czabaniuk, Lara C. (2014). „Struktura i reaktywność późnych kompleksów metali przejściowych η 3 -benzylowych”. Angew. chemia Int. wyd . 53 (11): 2826–2851. doi : 10.1002/anie.201305972 . PMID 24554487 .
- Bibliografia _ Yoshida, T.; Otsuka, S. „Kompleksy (η 3 -allilo)palladu(II)” Inorganic Syntheses , 1990, tom 28, strony 342-345. ISBN 0-471-52619-3
- ^ Hartwig, JF Organotransition Metal Chemistry, od wiązania do katalizy; Książki naukowe uniwersyteckie: Nowy Jork, 2010. ISBN 189138953X
