Kompleks okso metalu przejściowego
Kompleks okso metalu przejściowego to kompleks koordynacyjny zawierający ligand okso . Formalnie O 2- , ligand okso może być związany z jednym lub kilkoma centrami metali, tj. może istnieć jako terminal lub (najczęściej) jako ligandy mostkowe (ryc. 1). Ligandy okso stabilizują wysokie stopnie utlenienia metalu. Występują również w kilku metaloproteinach , na przykład w kofaktorach molibdenu i wielu enzymach zawierających żelazo. Jednym z najwcześniejszych syntetycznych związków zawierających ligand okso jest nadżelazian potasu (K 2 FeO 4 ), który prawdopodobnie został przygotowany przez Georga E. Stahla w 1702 roku.
Reaktywność
Olation i reakcje kwasowo-zasadowe

Powszechną reakcją, jaką wykazują związki metal-okso, jest olacja , proces kondensacji, który przekształca tlenki o niskiej masie cząsteczkowej w polimery z wiązaniami MOM. Olation często zaczyna się od deprotonowania kompleksu metal-hydroksy. Jest podstawą mineralizacji i wytrącania tlenków metali. W przypadku tlenków metali d0, V V , Nb V , Ta V , Mo VI i W VI proces olacji daje polioksometalany , dużą klasę cząsteczkowych tlenków metali.
Transfer atomu tlenu
Kompleksy metali okso są produktami pośrednimi w wielu reakcjach utleniania katalizowanych metalami . Przeniesienie atomu tlenu jest powszechną reakcją o szczególnym znaczeniu w chemii organicznej i biochemii . Niektóre metalo-okso są zdolne do przenoszenia swojego ligandu okso na podłoża organiczne. Jednym z takich przykładów tego typu reaktywności jest enzym z nadrodziny oksotransferazy molibdenowej .
W katalizie utleniania wody oksokompleksy metali są produktami pośrednimi w konwersji wody do O 2 .
Abstrakcja atomu wodoru
Metale przejściowe-okso są również zdolne do abstrakcji silnych wiązań C – H, N – H i O – H. Cytochrom P450 zawiera wysokowartościowe żelazo-okso, które jest zdolne do odrywania atomów wodoru od silnych wiązań C-H.
Tlenki molekularne
Do najdłużej znanych i najczęściej stosowanych związków okso należą środki utleniające, takie jak nadmanganian potasu (KMnO 4 ) i tetratlenek osmu (OsO 4 ). Związki takie jak te są szeroko stosowane do przekształcania alkenów w wicynalne diole i alkoholi w ketony lub kwasy karboksylowe. Bardziej selektywne lub łagodniejsze odczynniki utleniające obejmują chlorochromian pirydyniowy (PCC) i dichromian pirydyniowy (PDC). Gatunki metali okso są zdolne do katalitycznego, w tym asymetrycznego utleniania różnego rodzaju. Niektóre kompleksy metal-okso sprzyjają aktywacji wiązania CH , przekształcając węglowodory w alkohole.
 00 Dobór molekularnych tlenków metali. Od lewej chlorek wanadylu (d ), oksokarbonyl wolframu (d 2 ), nadmanganian (d ), [ReO 2 (pirydyna) 4 ] + (d 2 ), uproszczony widok związku I (stan cytochromu P450 , d 4 ) i Ir(O)(mesityl) 3 (d4 ) .
00 Dobór molekularnych tlenków metali. Od lewej chlorek wanadylu (d ), oksokarbonyl wolframu (d 2 ), nadmanganian (d ), [ReO 2 (pirydyna) 4 ] + (d 2 ), uproszczony widok związku I (stan cytochromu P450 , d 4 ) i Ir(O)(mesityl) 3 (d4 ) .
Metaloenzymy
Gatunki żelaza(IV)-okso

Związki żelaza (IV) -okso są półproduktami w wielu biologicznych utlenianiach:
- Hydroksylazy zależne od alfa-ketoglutaranu aktywują O 2 poprzez oksydacyjną dekarboksylację ketoglutaranu , tworząc centra Fe(IV)=O, tj. ferryl , które hydroksylują różne substraty węglowodorowe.
- Enzymy cytochromu P450 wykorzystują kofaktor hemowy , wprowadzają tlen żelazowy do nasyconych wiązań C-H, epoksydują olefiny i utleniają grupy aromatyczne.
- Monooksygenaza metanu (MMO) utlenia metan do metanolu poprzez przeniesienie atomu tlenu z związku pośredniego żelazo-okso w jego niehemowym centrum diżelazowym. Wiele wysiłku wkłada się w odtworzenie reakcji z syntetycznymi katalizatorami.
Molibden/wolfram oxo

Ligand okso (lub analogiczny ligand sulfidowy) jest prawie wszechobecny w chemii molibdenu i wolframu, pojawiając się w rudach zawierających te pierwiastki, w całej ich chemii syntetycznej, a także w ich roli biologicznej (oprócz azotazy). Ogólnie przyjmuje się , że biologicznie transportowanymi gatunkami i punktem wyjścia dla biosyntezy są oksometalany MoO 4-2 lub WO 4-2 . Wszystkie enzymy Mo/W, z wyjątkiem azotazy , są związane z jedną lub więcej molibdopteryną zespół protetyczny. Centra Mo/W generalnie przechodzą między stanami sześciowartościowymi (M(VI)) i czterowartościowymi (M(IV)). Chociaż istnieją pewne różnice między tymi enzymami, przedstawiciele wszystkich trzech rodzin obejmują transfer atomów tlenu między centrum Mo/W a substratem. Reprezentatywne reakcje z każdej z trzech klas strukturalnych to:
- Oksydaza siarczynowa : SO 3 −2 + H 2 O → SO 4 −2 + 2 H + + 2 e −
- Reduktaza DMSO : H 3 CS(O) CH 3 ( DMSO ) + 2 H + + 2 e − → H 3 CSCH 3 ( DMS ) + H 2 O
- Aldehydowa oksydoreduktaza ferredoksyny : RCHO + H 2 O → RCO 2 H + 2 H + + 2 e -
Na rysunku pokazano trzy różne klasy kofaktorów molibdenu. Biologiczne wykorzystanie wolframu odzwierciedla zastosowanie molibdenu.
Kompleks wydzielający tlen
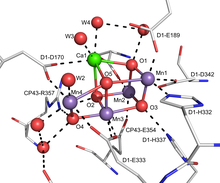
Miejscem aktywnym kompleksu wydzielającego tlen (OEC) fotoukładu II (PSII) jest centrum Mn 4 O 5 Ca z kilkoma mostkowymi ligandami okso, które uczestniczą w utlenianiu wody do tlenu cząsteczkowego. Proponuje się, aby OEC wykorzystywał końcowy produkt pośredni okso jako część reakcji utleniania wody. Kompleks ten jest odpowiedzialny za produkcję prawie całego tlenu cząsteczkowego na Ziemi. To kluczowe ogniwo w obiegu tlenu jest niezbędne dla większości bioróżnorodności obecnej na Ziemi.
„Ściana okso”

Termin „ściana okso” jest teorią używaną do opisania faktu, że nie są znane żadne końcowe kompleksy okso dla centrów metalowych o symetrii oktaedrycznej i liczbie d-elektronów powyżej 5.
Związki okso dla triad wanadu do żelaza ( grupy 3-8) są dobrze znane, podczas gdy końcowe związki okso dla metali w triadach kobaltu do cynku (grupy 9-12) są rzadkie i niezmiennie zawierają metale o liczbach koordynacyjnych niższych niż 6. To trend utrzymuje się dla innych wiązań wielokrotnych metal-ligand. Zgłoszone wyjątki od tej reguły zostały wycofane.
Oksokompleks irydu Ir(O)(mesityl) 3 może wydawać się wyjątkiem od ściany okso, ale tak nie jest, ponieważ kompleks nie jest oktaedryczny. Symetria trygonalna zmienia kolejność metalowych orbitali d poniżej zdegenerowanej pary MO π *. W potrójnie symetrycznych kompleksach wielokrotne wiązanie MO jest dozwolone dla aż 7 d-elektronów.
Terminalne ligandy okso są również raczej rzadkie w przypadku triady tytanu, zwłaszcza cyrkonu i hafnu, i są nieznane w przypadku metali z grupy 3 (skand, itr i lantan).