Kompleksy pirydynowe metali przejściowych
Kompleksy pirydyny metali przejściowych obejmują wiele kompleksów koordynacyjnych , które zawierają pirydynę jako ligand. Większość przykładów to mieszane kompleksy ligandów. Wiadomo również, że wiele wariantów pirydyny koordynuje jony metali, takie jak metylopirydyny, chinoliny i bardziej złożone pierścienie.
Klejenie
Z pKa 5,25 dla sprzężonego kwasu, pirydyna jest około 15 razy mniej zasadowa niż imidazol. Pirydyna jest słabym ligandem akceptora pi. Trendy odległości MN dla kompleksów typu [MCl 2 (py) 4 ] 2+ ujawniają antykorelację z liczbą d-elektronów. Znanych jest niewiele kompleksów pirydyn z metalami o niskiej wartościowości. Rola pirydyny jako zasady Lewisa rozciąga się również na chemię głównych grup. Przykłady obejmują kompleks tritlenku siarki z pirydyną SO3 ( py) i addukt pirydyny z boranem, BH3py .
Klasyfikacja kompleksów metal-pirydyna
Znanych jest wiele kompleksów pirydynowych metali. Ze względu na geometrię kompleksy te można podzielić na oktaedryczne, czworościenne, liniowe itp.
Kompleksy ośmiościenne
Ze względu na stosunkowo szeroki kąt CNC, atomy 2,6-wodoru zakłócają tworzenie kompleksów [M(py) 6 ] z . Znanych jest kilka oktaedrycznych homoleptycznych kompleksów pirydynowych. Te złożone kationy znajdują się w solach [Ru(py) 6 ]Fe 4 (CO) 13 i [Ru(py) 6 ](BF 4 ) 2 . Niektóre związki o stechiometrii M(py) 6 (ClO 4 ) 2 zostały przeformułowane jako [M(py) 4 (ClO 4 ) 2 ] . (py) 2
Powszechną rodziną kompleksów pirydynowych są kompleksy typu [MCl2 ( py) 4 ] n+ . Ligandy chlorkowe są wzajemnie trans w tych kompleksach.
| formuła | CAS RN | kluczowe właściwości | Przygotowanie | |
|---|---|---|---|---|
| TiCl2 ( pirydyna) 4 | 131618-68-3 |
niebieski, triplet d Ti-N = 2,27 Å, d Ti-Cl = 2,50 Å (thf solwat) |
TiCl 3 (thf) 3 + KC 8 + py | |
| VCl 2 (pirydyna) 4 | 15225-42-0 | fioletowy | VCI3 + Zn + py | |
| CrCl2 ( pirydyna) 4 | 51266-53-6 |
zielony d Cr-Cl = 2,80 Å d Co-Cl = 2,16 Å |
CrCI2 + py | |
| MnCl 2 (pirydyna) 4 | 14638-48-3 | 1.383 | ||
| FeCl2 ( pirydyna) 4 | 15138-92-8 |
żółty d Fe-Cl = 2,43 Å |
FeCl 2 + py | |
| CoCl2 ( pirydyna) 4 | 13985-87-0 |
niebieski d Co-Cl = 2,44 Å |
CoCl2 + py | |
| [CoCl2 ( pirydyna) 4 ]Cl | 27883-34-7 |
zielony (heksahydrat) d Co-Cl = 2,25 Å, d Co-N = 1,98 Å jako [CoCl 3 (py)] - sól |
CoCl 2 (pirydyna) 4 + Cl 2 | |
| NiCl 2 (pirydyna) 4 | 14076-99-4 |
niebieski d Ni-Cl = 2,44 Å |
NiCl 2 + py | |
| NbCl2 ( pirydyna) 4 | 168701-43-7 | d Nb-N = 2,22 A, d Nb-Cl = 2,51 A | NbCl 4 (thf) 2 + KC 8 + py | |
| [MoCl 2 py) 4 ] Br 3 | Br 3 − sól |
żółty d Mo-Cl = 2,41 A, d Mo-N = 2,20 A |
||
| TcCl2 py ) 4 | 172140-87-3 |
fioletowy d Tc-Cl = 2,41 Å, d Tc-N = 2,10 Å |
TcCl 4 py 2 + Zn + py | |
| RuCl2 ( pirydyna) 4 | 16997-43-6 |
czerwono-pomarańczowy d Ru-N = 2,08 Å, d Ru-Cl = 2,40 Å |
RuCl3 ( H2O ) x + py | |
| [RhCI2 ( pirydyna) 4 ] + | 14077-30-6 (Cl - sól) | żółty | RhCl3 (H2O ) 3 + py + kat. reduktor | |
| OsCl 2 (pirydyna) 4 | 137822-02-7 |
brązowy d Os-Cl = 2,40 Å, d Os-N = 2,068 Å |
K3OsCI6 + py + (CH2OH ) 2 / 140 ° C | |
| [IrCl2 ( pirydyna) 4 ] + |
żółty 1,35 Å (chlorek . heksahydrat) |
Trihalogenki tris(pirydyny), tj. [MCl 3 (py) 3 ] (M = Ti, Cr, Rh Ir), są kolejną dużą klasą kompleksów M-Cl-py.
Kompleksy czterech współrzędnych

Kompleksy o czterech współrzędnych obejmują pochodne czworościenne i kwadratowe. Przykłady homoleptycznych czworościennych kompleksów obejmują [M(py) 4 ] n+ dla Mn + = Cu + , M = Ni2 + , Ag + i Ag2 + . Przykłady homoleptycznych kwadratowych planarnych kompleksów obejmują kationy d8 [ M(py) 4 ] n+ dla Mn + = Pd2 + , Pt2 + , Au3 + .
Ni(ClO 4 ) 2 (3-pikolina) 2 można wyodrębnić w dwóch izomerach: żółtym, diamagnetycznym kwadratowym płaskim lub niebieskim, paramagnetycznym czworościennym.
Mn(II) i Co(II) tworzą kompleksy zarówno tetraedryczny MCl 2 py 2, jak i oktaedryczny MCl 2 py 4 , w zależności od warunków:
- MCl 2 py 2 + 2 py → MCl 2 py 4
Zespoły dwu- i trójrzędowe
Istnieje wiele przykładów dla [Au(py) 2 ] + . [Ag(py) 3 ] + i [Cu(py) 2 ] + są również poprzedzone.
kompleksy pi
Mod koordynacyjny η 6 , jaki występuje w kompleksach benzenowych η 6 , obserwuje się tylko w pochodnych obciążonych sterycznie , które blokują centrum azotu.
- Pikoliny
Wiele podstawionych pirydyn działa jako ligandy metali przejściowych. Najlepiej zbadane są pochodne monometylowe, pikoliny (2-, 3- i 4-pikolina). 2-Pikoliny mają steryczną przeszkodę w koordynacji.
- 2,2'-bipi
0 Sprzężenie dwóch pierścieni pirydynowych w ich pozycjach 2 daje 2,2'-bipirydynę , szeroko badany dwukleszczowy ligand. Widocznych jest wiele różnic między kompleksami pirydyny i bipirydyny. Znanych jest wiele kompleksów [M(bipy) 3 ] z , podczas gdy analogiczne kompleksy [M(py) 6 ] z są rzadkie i pozornie nietrwałe. Bipirydyna jest redoks- niewinnym ligandem , co ilustruje istnienie kompleksów, takich jak [Cr(bipy) 3 ] . Analogi pirydynowe takich kompleksów są nieznane. Kompleksy dichlorowe [MCl 2 (bipy) 2 ] n+ mają tendencję do cis, czego przykładem jest RuCl2 ( bipy) 2 . Natomiast kompleksy [MCl2 ( py) 4 ] n+ są zawsze trans.
- imidazole
Imidazole obejmują inną główną serię ligandów N-heterocyklicznych. W przeciwieństwie do pirydyn, pochodne imidazolu są z natury powszechnymi ligandami.
Zastosowania i występowanie
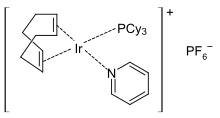
Katalizator Crabtree , popularny katalizator uwodornień, to kompleks pirydyny.
Chociaż kompleksy metali przejściowych z pirydyną mają niewiele praktycznych zastosowań, są szeroko stosowanymi syntetycznymi prekursorami. Wiele z nich jest bezwodnych, rozpuszczalnych w rozpuszczalnikach niepolarnych i podatnych na alkilowanie litoorganicznymi i odczynnikami Grignarda . Tak więc CoCl2 ( py)4 okazał się bardzo przydatny w chemii kobaltu organicznego , a NiCl2 ( py) 4 w chemii niklu organicznego .
- ^ Shin, Yeung-gyo K.; Szalda, David J.; Brunszwik, Bruce S.; Creutz, Carol; Sutin, Norman (1997). „Struktury elektroniczne i molekularne kompleksów pentaaminorutenu, pirydyny i benzoonitrylu jako funkcja stanu utlenienia”. Chemia nieorganiczna . 36 (14): 3190–3197. doi : 10.1021/ic9700967 . PMID 11669976 .
- ^ a b c d Długie, Gary J.; Clarke, Peter J. (1978). „Struktury krystaliczne i molekularne monohydratu trans -tetrakis (pirydyny) dichlorożelaza (II), -niklu (II) i -kobaltu (II) oraz monohydratu trans- tetrakis (pirydyny) dichlorożelaza (II)”. Chemia nieorganiczna . 17 (6): 1394–1401. doi : 10.1021/ic50184a002 .
- ^ Templeton, Joseph L. (1979). „Heksakis (pirydyna) ruten (II) tetrafluoroboran. Struktura cząsteczkowa i właściwości spektroskopowe”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 101 (17): 4906–4917. doi : 10.1021/ja00511a020 .
- ^ Lichtenberg, Kryspin; Adelhardt Mario; Wörle, Michael; Büttner, Torsten; Meyer, Karsten; Grützmacher, Hansjörg (2015). „Mono- i dwujądrowe neutralne i kationowe związki żelaza (II) wspierane przez ligand amidynato-diolefinowy: charakterystyka i zastosowanie katalityczne”. metaloorganiczne . 34 (12): 3079–3089. doi : 10.1021/acs.organomet.5b00395 .
- ^ Sołdatow, Dmitrij V.; Ripmeester, John A. (1998). „Heksapirydynowe związki addycyjne soli metali (II) (nadchlorany niklu i magnezu, azotan magnezu): ich supramolekularny charakter i koordynacja anionowa kationu metalu [1]”. chemia supramolekularna . 9 (3): 175–181. doi : 10.1080/10610279808034984 .
- ^ ab Araya , Miguel A.; Bawełna, F. Albert; Matonic, John H.; Murillo, Carlos A. (1995). „Wydajny proces redukcji prowadzący do tytanu (II) i niobu (II): przygotowanie i charakterystyka strukturalna związków trans -MCl 2 (py) 4 , M = Ti, Nb i Mn”. Chemia nieorganiczna . 34 (22): 5424–5428. doi : 10.1021/ic00126a009 .
- ^ Wijeratne, Gayan B.; Zolnhofer, Eva M.; Fortier, Skye; Grant, Lauren N.; Carroll, Patrick J.; Chen, Chun-Hsing; Meyer, Karsten; Krzystek J.; Ożarowski, Andrzej; Jackson, Tymoteusz A.; Mindiola, Daniel J.; Telser, Jozue (2015). „Struktura elektronowa i reaktywność dobrze zdefiniowanego kompleksu jednojądrzastego Ti (II)” . Chemia nieorganiczna . 54 (21): 10380–10397. doi : 10.1021/acs.inorgchem.5b01796 . PMID 26451744 .
- Bibliografia _ Krüger, C. (1973). „Tetrapirydynodichlorowanad (II)” . Kryształ. Struktura. Kom . 2 : 421.
- ^ Obrzęk, Jilles JH; Stauthamer, Walter; Van Bolhuis, Fre; Gambarotta, Sandro; Smeets, Wilberth JJ; Spek, Anthony L. (1990). „Nowe kompleksy aminowe wanadu (II): łatwe wejście w chemię dwuwartościowego wanadu. Synteza i charakterystyka jednojądrzastego L 4 VCl 2 [L = amina, pirydyna]: struktury rentgenowskie trans - (TMEDA) 2 VCl 2 [ TMEDA = N,N,N',N'-Tetrametyloetylenodiamina] i trans -Mz 2 V(py) 2 [Mz = oC 6 H 4 CH 2N (CH3 ) 2 , py = pirydyna]". Inorganic Chemistry . 29 (7): 1302-1306. doi : 10.1021/ic00332a003 .
- ^ Bawełna, F. Albert; Daniels, Lee M.; Feng, Xuejun; Maloney, David J.; Murillo, Carlos A.; Zúñiga, Luis A. (1995). „Eksperymentalne i teoretyczne badanie cząsteczki Paradygmatu Jahna-Tellera, all-trans-CrCl 2 (H 2 O) 2 (pirydyna) 2 i pokrewnego trans -CrCl 2 (pirydyna) 4 · aceton”. Inorganica Chimica Acta . 235 (1–2): 21–28. doi : 10.1016/0020-1693(95)90041-4 .
- Bibliografia _ Li, Jinyu; Wu, Zhongzhi; Zou, Jianzhong; Xu, Zheng; Ty, Xiaozeng; Dong, Zhengchao (1993). „Synteza i struktura kryształu rentgenowskiego kompleksu kobaltu o mieszanej wartościowości, Co 2 Cl 5 (py) 5 ”. Wielościan . 12 (18): 2261–2264. doi : 10.1016/S0277-5387(00)88265-0 .
- ^ Glerup, Jørgen; Schäffer, Claus Erik; Springborg, Johan (1978). „Synteza soli trans -dichloro- i trans -difluorotetrakis (pirydyno) kobaltu (III)” . Acta Chemica Scandinavica . 32a : 673–674. doi : 10.3891/acta.chem.scand.32a-0673 .
- Bibliografia _ Liban, I.; Brenčič, JV (1996). „Trójbromek trans-dichlorotetrakis (pirydyno-N) molibdenu (III)” . Acta Crystallographica Sekcja C Komunikacja w strukturze kryształu . 52 (9): 2155–2157. doi : 10.1107/S0108270196005628 .
- Bibliografia _ Burrell, Anthony K.; Bryan, Jeffrey C. (1996). „Kompleksy technetu (III), technetu (II) i technetu (I) z ligandami pirydynowymi. Czy koordynacja pirydyny może stabilizować stany niskiego utlenienia technetu?”. Chemia nieorganiczna . 35 (2): 335–341. doi : 10.1021/ic950291q . PMID 11666213 .
- Bibliografia _ Lau, TC (1994). „ trans -dichlorotetrapirydynoruten(II)”. Acta Crystallographica Sekcja C Komunikacja w strukturze kryształu . 50 (9): 1406–1407. doi : 10.1107/S0108270194002088 . hdl : 10722/69086 .
- Bibliografia _ Wilkinson, GW (1967). „Trans -dichlorotetra (pirydyna) sole rodu (III)”. trans -dichlorotetra(pirydyno)rodu(III) . Syntezy nieorganiczne. Tom. 10. s. 64–67. doi : 10.1002/9780470132418.ch11 . ISBN 9780470132418 .
- Bibliografia _ Preetz, W. (1997). "Darstellung, Kristallstrukturen, Schwingungsspektren und Normalkoordinatenanalysen der trans -Dihalogeno-tetrakis-Pyridin-Osmium(II)-Komplexe trans -[OsX 2 Py 4 ], X = F, Cl, Br, I". Zeitschrift für anorganische und allgemeine Chemie . 623 (1–6): 501–508. doi : 10.1002/zaac.19976230179 .
- Bibliografia _ Mitchell, Simon H.; Williams, Peter A.; Vagg, Robert S. (1984). „Struktura postaci niskotemperaturowej trans - [Ir (pirydyna) 4 Cl 2 ] Cl . 6H 2 O”. Dziennik chemii koordynacyjnej . 13 (4): 325–330. doi : 10.1080/00958978408073886 .
- ^ Acharya, KR; Tavale, SS; Guru Row, TN (1984). „Struktura meru -Trichlorotris (pirydyno) rodu (III), [RhCl 3 (C 5 H 5 N) 3 ]”. Acta Crystallographica Sekcja C Komunikacja w strukturze kryształu . 40 (8): 1327–1328. doi : 10.1107/S0108270184007848 .
- ^ JC Collins, WW Hess (1972). „Aldehydy z pierwszorzędowych alkoholi przez utlenianie tritlenkiem chromu: heptanal”. Syntezy Organiczne . 52 : 5. doi : 10.15227/orgsyn.052.0005 .
- ^ Horwat, Gordan; Portada, Tomisław; Stilinović, Władimir; Tomišić, Vladislav (2007). „Heksafluoridofosforan tetrapirydynomiedzi (I) (V)” . Acta Crystallographica Sekcja E . 63 (6): m1734. doi : 10.1107/S1600536807024051 .
- Bibliografia _ Wadsten, T.; Borbély-Kuszmann, A. (1986). „Charakterystyka [Ni(py) 4 ]Cl 2 i jego rozkładu termicznego”. Dziennik analizy termicznej . 31 (4): 845–852. doi : 10.1007/BF01913555 . S2CID 93538201 .
- Bibliografia _ Oskarsson, Ake; Lund, PA; Shen, Quang; Weidlein, Johan; Spiridonow, wiceprezes; Pasmo, TG (1982). „Struktura krystaliczna nadchloranu tetrapirydyny miedzi (I) i nadchloranu tetrapirydyny srebra (I) w temperaturze 260 K” . Acta Chemica Scandinavica . 36a : 605–610. doi : 10.3891/acta.chem.scand.36a-0605 .
- ^ Kauffman, George B.; Houghten, Richard A.; Likens, Robert E.; Posson, Philip L.; Ray, RK (2007) [1998]. „Tetrakis (pirydyna) srebro (2+) nadtlenodisiarczan” . Syntezy nieorganiczne . Syntezy nieorganiczne. Tom. 32. s. 177–181. doi : 10.1002/9780470132630.ch30 . ISBN 9780470132630 .
- Bibliografia _ Georgiou, Dayne C.; Wilson, David JD; Dutton, Jason L. (2014). „Reakcje [PhI (pirydyna) 2] 2+ z modelowymi parami redoks Pd i Pt II / IV”. Chemia nieorganiczna . 53 (3): 1690-1698. doi : 10.1021/ic402836d . PMID 24409820 .
- Bibliografia _ Hingerty, BE; Busing, WR (1989). „Struktura trihydratu chlorku tetrakis (pirydyny) platyny (II): nieograniczone anizotropowe udoskonalanie metodą najmniejszych kwadratów atomów wodoru i innych niż atomy wodoru na podstawie połączonych danych dyfrakcji rentgenowskiej i neutronowej”. Acta Crystallographica Sekcja C Komunikacja w strukturze kryształu . 45 : 26–30. doi : 10.1107/S0108270188009515 .
- ^ abc Corbo , Robert; Ryan, Gemma F.; Haghighatbin, Mohammad A.; Hogan, Conor F.; Wilson, David JD; Hulett, Mark D.; Barnard, Peter J.; Dutton, Jason L. (2016). „Dostęp do macierzystego trikationu tetrakisu (pirydyny) złota (III), łatwe tworzenie rzadkich końcowych wodorotlenków Au (III) i wstępne badania właściwości biologicznych”. Chemia nieorganiczna . 55 (6): 2830–2839. doi : 10.1021/acs.inorgchem.5b02667 . PMID 26930516 .
- ^ a b Vallarino, LM; Wzgórze, MY; Quagliano, JV (1965). „Związki koordynacyjne soli niklu (II) z podstawionymi pirydynami. Kompleksy 2-, 3- i 4-metylopirydyny”. Chemia nieorganiczna . 4 (11): 1598–1604. doi : 10.1021/ic50033a014 .
- Bibliografia _ Uruska, I. (1966). „Względna stabilność kompleksów ośmiościennych i czworościennych w roztworze. I. Kompleksy chloropirydynowe dwuwartościowych metali przejściowych”. Chemia nieorganiczna . 5 (2): 256–264. doi : 10.1021/ic50036a022 .
- Bibliografia _ Lu, Canzhong; Zhuang, Honghui (2002). „Synteza hydrotermalna i struktury trzech nowych kompleksów miedzi: [{Cu(2,2 ′ -bipy}2(β-Mo 8 O 26 )], [{Cu(py) 3 }2{Cu(py) 2 }2 (α-Mo8O26 ) ] i [Cu(py) 2 ]4[(SO4 ) Mo12O36 ] ". Journal of the Chemical Society, Dalton Transactions (14): 2879-2884. doi : 10.1039 / b111480h .
- ^ Elschenbroich, C. (2008). Organometallchemie (wyd. 6). Vieweg & Teubner. s. 524–525. ISBN 978-3-8351-0167-8 .
- Bibliografia _ Janssen, Femke FBJ; Budzelaar, Peter HM (2010). „(Py) 2 Co(CH 2 SiMe 3 ) 2 jako łatwo dostępne źródło „CoR 2 ” ”. metaloorganiczne . 29 (8): 1897–1908. doi : 10.1021/om901045s .
- ^ Chirik, Paweł J. (2015). „Uwodornianie alkenów katalizowane żelazem i kobaltem: kataliza z ligandami zarówno aktywnymi redoks, jak i silnymi polami” . Rachunki badań chemicznych . 48 (6): 1687-1695. doi : 10.1021/acs.accounts.5b00134 . PMID 26042837 .
- ^ Campora, Juan; Del Mar Conejo, Maria; Mereiter, Kurt; Palma, Pilar; Perez, Carmen; Reyes, Manuel L.; Ruiz, Caridad (2003). „Synteza dialkilowych, diarylowych i metalacyklicznych kompleksów Ni i Pd zawierających pirydynę, α-diiminy i inne ligandy azotowe”. Czasopismo chemii metaloorganicznej . 683 : 220–239. doi : 10.1016/S0022-328X(03)00691-0 .