Terapia deprywacji androgenów
| Terapia deprywacji androgenów | |
|---|---|
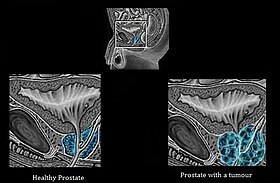 Różnice między zdrową prostatą a prostatą z guzem
| |
| Inne nazwy | Terapia supresyjna androgenów |
| Specjalność | onkologia |
Terapia deprywacji androgenów ( ADT ), zwana także terapią supresji androgenów , jest terapią antyhormonalną , której głównym zastosowaniem jest leczenie raka prostaty . Komórki raka prostaty zwykle wymagają hormonów androgenowych , takich jak testosteron . ADT zmniejsza poziom hormonów androgenowych za pomocą leków lub operacji , aby zapobiec wzrostowi komórek raka prostaty. Podejścia farmaceutyczne obejmują antyandrogeny i kastrację chemiczną .
W kilku badaniach stwierdzono, że ADT wykazało korzyści u pacjentów z chorobą przerzutową oraz jako uzupełnienie radioterapii u pacjentów z miejscowo zaawansowaną chorobą, a także z niekorzystną chorobą zlokalizowaną pośredniego lub wysokiego ryzyka. Jednak u pacjentów z rakiem gruczołu krokowego niskiego ryzyka ADT nie wykazało przewagi w zakresie przeżycia i znacznych szkód, takich jak impotencja, cukrzyca i utrata masy kostnej.
Terapia może również eliminować komórki nowotworowe poprzez indukowanie starzenia wywołanego deprywacją androgenów . Obniżenie poziomu androgenów lub powstrzymanie ich przed dostaniem się do komórek raka prostaty często powoduje, że rak prostaty kurczy się lub rośnie wolniej przez pewien czas. Leczenie to musi być jednak połączone z radioterapią (RT), ponieważ sama ADT nie eliminuje nowotworu ; po prostu zmniejsza jego agresywność.
typy
Metoda oparta na chirurgii
- Orchiektomia (kastracja chirurgiczna)
- Polega na usunięciu jąder , narządu, w którym syntetyzowane są androgeny , pacjentowi z chorobą nowotworową. Jest to najbardziej radykalny zabieg na zakończenie produkcji androgenów. Ponadto jest najłatwiejszy i najtańszy. Główną wadą jest to, że kastracja chirurgiczna jest metodą stałą.
Metody oparte na lekach
- W syntezie testosteronu pośredniczy łańcuch procesów rozpoczynających się w mózgu. Kiedy organizm wykryje niski poziom testosteronu, podwzgórze zaczyna produkować LHRH . LHRH aktywuje syntezę LH (hormonu luteinizującego) w przysadce mózgowej. LH indukuje syntezę testosteronu w jądrach. Istnieją dwa różne leki, agoniści i antagoniści LHRH , które obniżają ilość testosteronu wytwarzanego przez jądra. Działają poprzez hamowanie powstawania LH w przysadce mózgowej. Agoniści LHRH powodują nagły wzrost poziomu testosteronu, po którym następuje ogromny spadek, proces zwany zaostrzeniem , podczas gdy antagoniści LHRH bezpośrednio zmniejszają ilość testosteronu. Do agonistów i antagonistów LHRH stosowanych w terapii deprywacji androgenów należą leuprorelina (leuprolid) , goserelina , tryptorelina , histrelina , buserelina i degareliks .
- Leki te są wstrzykiwane pod skórę, uzyskując taki sam efekt jak kastracja chirurgiczna . Kastracja chemiczna może być lepsza od kastracji chirurgicznej [ potrzebne źródło ] , ponieważ utrzymuje jądra w stanie nienaruszonym.
- Terapia antyandrogenowa
- Nadnercza odkryto jako kolejny ośrodek produkcji androgenów nawet po procesie kastracji. Dlatego opracowano leczenie uzupełniające, które wykorzystuje antyandrogeny do blokowania zdolności organizmu do wykorzystywania jakichkolwiek androgenów. Komórki prostaty zawierają receptor androgenowy (AR), który stymulowany przez androgeny, takie jak testosteron, wspomaga wzrost i utrzymuje różnicowanie prostaty. Te sygnały prowzrostowe mogą być jednak problematyczne, gdy występują w komórce nowotworowej. Antyandrogeny mogą wnikać do komórek i zapobiegać wiązaniu testosteronu z białkami receptora, ze względu na ich większe powinowactwo do receptora androgenowego.
- Głównymi antyandrogenami są octan cyproteronu , flutamid , nilutamid , bikalutamid i enzalutamid , które są podawane w postaci tabletek doustnych. Ostatnio opracowano
- nowe antyandrogeny ukierunkowane na syntezę testosteronu ( octan abirateronu i sewiteron ) lub translokację jądrową AR ( enzalutamid , apalutamid i darolutamid ), jak również terapie skojarzone ( galeteron ) i mogą one lepiej oddziaływać na komórki reagujące na androgeny w połączeniu z ADT. Ale one również mogą odgrywać negatywną, niekorzystną rolę w rozwoju CRPC .
Wpływ na seksualność mężczyzn
Wydaje się, że normalna męska seksualność zależy od bardzo specyficznych i skomplikowanych schematów hormonalnych, które nie są do końca zrozumiałe. Jedno z badań sugeruje, że ADT może zmieniać równowagę hormonalną niezbędną do męskiej aktywności seksualnej. Wraz z wiekiem mężczyzn poziom testosteronu spada o około 1% rocznie po 30 roku życia; jednak ważne jest, aby ustalić, czy niski poziom testosteronu jest spowodowany normalnym starzeniem się, czy też chorobą, taką jak hipogonadyzm. Testosteron odgrywa znaczącą rolę w funkcjonowaniu seksualnym; dlatego naturalnie spadający poziom testosteronu może prowadzić do ograniczenia normalnego funkcjonowania seksualnego. Dalsze spadki poziomu testosteronu w surowicy mogą mieć negatywny wpływ na prawidłowe funkcje seksualne, prowadząc do pogorszenia jakości życia.
Zaburzenia erekcji nie są rzadkością po radykalnej prostatektomii, a mężczyźni, którzy dodatkowo przechodzą ADT, prawdopodobnie wykażą dalszy spadek zdolności do angażowania się w stosunek penetrujący, a także chęć do tego. Badanie dotyczące różnic w stosowaniu GnRH-A (i środka tłumiącego androgeny) lub orchiektomii wskazuje na różnice w zainteresowaniu seksualnym, doświadczaniu erekcji i częstości uczestnictwa w aktywności seksualnej. Mężczyźni deklarujący brak zainteresowania seksem wzrosli z 27,6% do 63,6% po orchiektomii iz 31,7% do 58,0% po GnRH-A; liczba mężczyzn, którzy nie doznali erekcji, wzrosła z 35,0% do 78,6%; i mężczyzn, którzy nie deklarowali podejmowania aktywności seksualnej, wzrósł z 47,9% do 82,8% po orchiektomii i z 45,0% do 80,2%. Badanie to sugeruje, że GnRH-A i orchiektomia miały podobny wpływ na funkcjonowanie seksualne. Błędne koło, w którym obniżenie poziomu testosteronu prowadzi do zmniejszenia aktywności seksualnej, co z kolei powoduje dalszy spadek zarówno wolnego, jak i całkowitego poziomu testosteronu. Pokazuje to znaczenie androgenów dla utrzymania struktur i funkcji seksualnych.
Niekorzystne skutki
Chociaż ukierunkowanie na oś androgenów ma wyraźną korzyść terapeutyczną, jego skuteczność jest tymczasowa, ponieważ komórki nowotworu prostaty przystosowują się, aby przetrwać i rosnąć. Wykazano, że usunięcie androgenów aktywuje przejście nabłonkowo-mezenchymalne (EMT), transdyferencjację neuroendokrynną (NEtD) i programy genowe podobne do komórek macierzystych raka .
- EMT ma ustalone role w promowaniu fenotypów biologicznych związanych z progresją nowotworu (migracja / inwazja, przeżycie komórek nowotworowych, właściwości podobne do komórek macierzystych raka, odporność na promieniowanie i chemioterapię) w wielu ludzkich typach raka.
- NEtD w raku gruczołu krokowego wiąże się z opornością na leczenie, przerzutami trzewnymi i agresywną chorobą.
- Fenotypy komórek macierzystych raka są związane z nawrotami choroby, przerzutami i przeżyciem komórek w krążeniu jako krążące komórki nowotworowe .
Zatem aktywacja tych programów poprzez hamowanie osi androgenów zapewnia mechanizm, dzięki któremu komórki nowotworowe mogą przystosować się, aby promować nawrót i postęp choroby.
Orchiektomia, analogi LHRH i antagoniści LHRH mogą powodować podobne skutki uboczne ze względu na zmiany poziomu hormonów płciowych (testosteronu).
Dla pacjentów i ich partnerów opracowano program rozpoznawania i radzenia sobie z bardziej uciążliwymi skutkami ubocznymi terapii deprywacji androgenów. Jeden program opiera się na książce z 2014 r. „Terapia deprywacji androgenów: niezbędny przewodnik dla pacjentów z rakiem prostaty i ich bliskich”, która została zatwierdzona przez Kanadyjskie Stowarzyszenie Urologiczne.
Ostatnie badania wykazały, że ADT może zwiększać ryzyko choroby Alzheimera lub demencji. Wzrost ryzyka może być związany z czasem trwania ADT. Podczas gdy niektóre badania donoszą o spadku niektórych obszarów funkcji poznawczych, takich jak zdolności przestrzenne , uwaga i pamięć werbalna , związane z ADT, dowody jako całość pozostają sprzeczne. Przydatne interwencje zapobiegawcze mogą obejmować między innymi interakcje społeczne , ćwiczenia fizyczne i „ dietę śródziemnomorską ”. Istnieje dodatkowe niewielkie ryzyko wystąpienia zaburzeń rytmu serca.
