przejście G1/S

Przejście G1/S jest etapem cyklu komórkowego na granicy między fazą G1 , w której komórka rośnie, a fazą S , podczas której następuje replikacja DNA. Jest zarządzany przez punkty kontrolne cyklu komórkowego, aby zapewnić integralność cyklu komórkowego, a kolejna faza S może zostać wstrzymana w odpowiedzi na nieprawidłowo lub częściowo replikowane DNA. Podczas tego przejścia komórka podejmuje decyzje o stanie w stanie spoczynku (wpisz G0 ), różnicowaniu , naprawiać DNA lub rozmnażać się w oparciu o sygnały środowiskowe i sygnały wejściowe sygnałów molekularnych. Przejście G1/S następuje późno w G1, a brak lub niewłaściwe zastosowanie tego wysoce regulowanego punktu kontrolnego może prowadzić do transformacji komórkowej i stanów chorobowych, takich jak rak
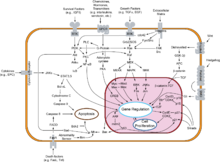
Podczas tego przejścia dimer cykliny D -Cdk4/6 G1 fosforyluje siatkówczaka, uwalniając czynnik transkrypcyjny E2F , który następnie napędza przejście z fazy G1 do fazy S. Przejście G1/S jest silnie regulowane przez czynnik transkrypcyjny p53 w celu zatrzymania cyklu komórkowego w przypadku uszkodzenia DNA.
Jest to „punkt bez powrotu”, poza którym komórka jest zobowiązana do podziału; u drożdży nazywa się to START, aw wielokomórkowych eukariotach jest to punkt restrykcyjny (punkt R). Jeśli komórka przejdzie przez przejście G1 / S, komórka będzie kontynuować cykl komórkowy niezależnie od nadchodzących czynników mitogennych z powodu dodatniej pętli sprzężenia zwrotnego transkrypcji G1-S. Dodatnie pętle sprzężenia zwrotnego obejmują cykliny G1 i akumulację E2F.
Przegląd cyklu komórkowego
Cykl komórkowy to proces, w którym uporządkowany zestaw zdarzeń prowadzi do wzrostu i podziału na dwie komórki potomne. Cykl komórkowy jest cyklem, a nie procesem liniowym, ponieważ dwie wytworzone komórki potomne powtarzają cykl. Proces ten obejmuje dwie główne fazy, interfazę , w której komórka rośnie i syntetyzuje kopię swojego DNA, oraz fazę mitotyczną (M), podczas której komórka oddziela swoje DNA i dzieli się na dwie nowe komórki potomne. Interfaza jest dalej dzielona na G1 (GAP 1), fazę S (synteza), fazę G2 (GAP 2) i faza mitotyczna (M), która z kolei dzieli się na mitozę i cytokinezę . Po cytokinezie, w fazie G1, komórki monitorują środowisko pod kątem potencjalnych czynników wzrostu, powiększają się i po osiągnięciu wielkości progowej (rRNA i ogólna zawartość białka charakterystyczna dla danego typu komórek) rozpoczynają progresję przez fazę S. Podczas fazy S komórka duplikuje również centrosom lub centrum organizujące mikrotubule , co ma kluczowe znaczenie dla rozdziału DNA w fazie M. Po całkowitej syntezie swojego DNA komórka wchodzi w fazę G2, w której kontynuuje wzrost przygotowując się do mitozy. Po interfazie komórka przechodzi w mitozę, obejmującą cztery podetapy: profazę , anafazę , metafazę i telofazę . W mitozie DNA kondensuje w chromosomy , które są ustawione w jednej linii i oddzielone przez wrzeciono mitotyczne . Po oddzieleniu duplikatu DNA na przeciwległych końcach komórki, cytoplazmie komórki jest dzielona na dwie części podczas cytokinezy, w wyniku czego powstają dwie komórki potomne.
Regulacja cyklu komórkowego
Podobnie jak w przypadku większości procesów zachodzących w organizmie, cykl komórkowy jest silnie regulowany, aby zapobiec syntezie zmutowanych komórek i niekontrolowanemu podziałowi komórek, który prowadzi do powstania guza . System kontroli cyklu komórkowego jest na biochemii , tak że białka czynnika promującego mitozę (MPF) kontrolują przejście z jednej fazy do drugiej w oparciu o serię punktów kontrolnych. MPF jest dimerem białkowym składającym się z cykliny i kinazy cyklinozależnej (Cdk), seryny i treoniny kinazy , które łączą się w różnych punktach cyklu, aby kontrolować postęp komórek w całym cyklu. Kiedy cyklina wiąże się z Cdk, Cdk zostaje aktywowany i fosforyluje serynę i treoninę na innych białkach, powodując aktywację i degradację innych białek, umożliwiając komórce przejście przez cykl komórkowy.
G 1 /przejście
W połowie do późnej fazy G1 cyklina D związana z Cdk4/6 aktywuje ekspresję składników fazy S cyklina- Cdk ; jednak komórka nie chce, aby cykliny fazy S stały się aktywne w G1 . Dlatego obecny jest inhibitor, białko Slc-1, które oddziałuje z dimerem, tak że dimer cyklina-Cdk fazy S pozostaje nieaktywny, dopóki komórka nie będzie gotowa do przejścia do fazy S. Gdy komórka urosła i jest gotowa do syntezy DNA, G 1 cyklina-Cdks fosforylują inhibitor cykliny fazy S sygnalizujący ubikwitynację, co powoduje dodanie grup do inhibitora. Ubikwitynacja inhibitora sygnalizuje SCF / proteasomowi degradację inhibitora, uwalniając i umożliwiając aktywację cykliny-Cdk fazy S i przejście komórki do fazy S. Będąc w fazie S, cyklina-Cdks fosforyluje kilka czynników w kompleksie replikacyjnym, promując replikację DNA, powodując odpadanie białek hamujących z kompleksów replikacyjnych lub poprzez aktywację składników kompleksu replikacyjnego w celu wywołania inicjacji replikacji DNA.
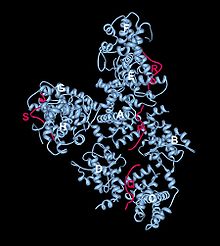
Białko siatkówczaka (pRB) i przejście G1/S
Inny dimer obecny w połowie G1 składa się z białka siatkówczaka ( pRB ) i czynnika transkrypcyjnego E2F . Kiedy pRb jest związany z E2F, E2F jest nieaktywne. Gdy cyklina D jest syntetyzowana i aktywuje Cdk4/6, cyklina-Cdk celuje w białko Rb w celu fosforylacji. Po fosforylacji pRb zmienia konformację, tak że E2F jest uwalniany i aktywowany, wiążąc się z górnymi regionami genów, inicjując ekspresję. W szczególności E2F kieruje ekspresją innych cyklin, w tym cykliny E i A , oraz genów niezbędnych do replikacji DNA. Cyklina E albo fosforyluje więcej pRb, aby dalej aktywować E2F i promować ekspresję większej ilości cykliny E, albo ma zdolność do zwiększania ekspresji samej siebie. Cyklina E oddziałuje również z Cdk2, kierując cyklem komórkowym, aby przejść z fazy G1 do fazy S.
Rola siatkówczaka w powstawaniu nowotworów
Retinoblastoma (Rb) to nowotwór oka spowodowany zmutowanym białkiem pRb. Kiedy pRb jest zmutowane, staje się niefunkcjonalne i nie jest w stanie hamować ekspresji czynnika transkrypcyjnego E2F . Dlatego E2F jest zawsze aktywny i napędza cykl komórkowy, aby przejść od fazy G1 do fazy S. W rezultacie wzrost i podział komórek jest nieuregulowany, co powoduje guza w oku.
Punkty kontrolne cyklu komórkowego
Aby zapewnić prawidłowy podział komórek, cykl komórkowy wykorzystuje liczne punkty kontrolne do monitorowania progresji komórek i zatrzymywania cyklu, gdy procesy idą nie tak. Te punkty kontrolne obejmują cztery punkty kontrolne uszkodzeń DNA , jeden niereplikowany punkt kontrolny DNA na końcu G2, jeden punkt kontrolny zespołu wrzeciona w mitozie i punkt kontrolny segregacji chromosomów podczas mitozy.
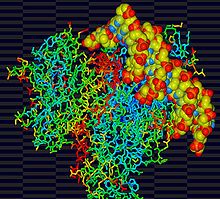
p53 jako regulator
Pomiędzy fazą G1 a fazą S występują trzy punkty kontrolne uszkodzenia DNA, aby zapewnić prawidłowy wzrost i syntezę DNA przed podziałem komórki. Uszkodzone DNA w fazie G1, przed wejściem w fazę S oraz w fazie S powoduje ekspresję ATM/R . Białko ATM/R następnie stabilizuje i aktywuje czynnik transkrypcyjny p53 , dzięki czemu może wiązać się z górnymi regionami genów, indukując ekspresję białek, w tym p21CIP. p21CIP wiąże się i hamuje każdą cyklinę-cdk obecną w cyklu komórkowym, zatrzymując cykl do czasu naprawienia uszkodzeń DNA.
Dodatkowe procesy w punktach kontrolnych uszkodzeń DNA
Spośród czterech punktów kontrolnych uszkodzeń DNA, dwa mają dodatkowy proces monitorowania uszkodzeń DNA inny niż aktywacja p53. Przed wejściem w fazę S i podczas fazy S, ATM/R aktywuje również Chk1/2, która hamuje Cdc25A , białko odpowiedzialne za aktywację dimerów cyklina-Cdk. Bez aktywacji dimeru cykliny komórka nie może przejść przez cykl. Te dwa punkty kontrolne mają dodatkowe procesy regulacji, ponieważ replikacja uszkodzonego DNA w fazie S może być szkodliwa dla komórki i, co ważniejsze, dla organizmu.