Alfa-mannozydoza
 | |
| Alfa-mannozydoza | |
|---|---|
| Alfa-mannozydoza ma autosomalny recesywny wzór dziedziczenia Rycina 1 | |
| Specjalność |
Endokrynologia |
Alfa-mannozydoza jest lizosomalnym zaburzeniem spichrzeniowym , po raz pierwszy opisanym przez szwedzkiego lekarza Okermana w 1967 roku. U ludzi wiadomo, że jest spowodowana autosomalną recesywną mutacją genetyczną w genie MAN2B1, zlokalizowanym na chromosomie 19, wpływającym na produkcję enzymu alfa- D-mannozydazy, powodując jej niedobór. W konsekwencji, jeśli oboje rodzice są nosicielami, przy każdej ciąży istnieje 25% szans, że wadliwy gen od obojga rodziców zostanie odziedziczony i u dziecka rozwinie się choroba. Istnieją dwie szanse na trzy, że zdrowe rodzeństwo będzie nosicielami (ryc. 1). U zwierząt gospodarskich alfa-mannozydoza jest spowodowana przewlekłym zatruciem swainsoniną z locoweed .
Objawy
Alfa-mannozydoza jest wieloukładową, postępującą chorobą trwającą całe życie, prowadzącą do pogorszenia funkcji nerwowo-mięśniowych i szkieletowych na przestrzeni dziesięcioleci. Czas pojawienia się objawów koreluje z ciężkością choroby. Początek najcięższej postaci choroby występuje w pierwszych miesiącach życia i obejmuje nieprawidłowości szkieletowe oraz niepełnosprawność intelektualną , z szybkim postępem prowadzącym do śmierci z powodu pierwotnego zajęcia ośrodkowego układu nerwowego lub miopatii . Jednak większość noworodków z lizosomalnymi zaburzeniami spichrzeniowymi jest bezobjawowa i rzadko poważnie dotknięta. Opóźnia to rozpoznanie, zwłaszcza że łagodniejsze formy choroby obejmują jedynie łagodną lub umiarkowaną niepełnosprawność intelektualną, która postępuje stopniowo w dzieciństwie lub w okresie dojrzewania.
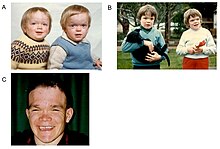
Pierwsza dekada życia charakteryzuje się rozwojem upośledzenia słuchu, opóźnieniem psychoruchowym, nawracającymi infekcjami, zwłaszcza górnych dróg oddechowych, infekcjami płuc oraz ostrymi/surowiczymi infekcjami ucha środkowego. Mogą wystąpić istotne zmiany w wielu rysach twarzy, takie jak: odstające czoło; spłaszczony grzbiet nosa; mały nos; szerokie usta; i szeroko rozstawionych zębów. Osłabienie mięśni lub nieprawidłowości kręgosłupa mogą wystąpić z powodu gromadzenia się materiałów magazynujących w mięśniach.
Patofizjologia
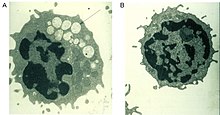
Wadliwy enzym alfa-mannozydaza, który normalnie pomaga rozkładać cukry złożone pochodzące z glikoprotein w lizosomie , powoduje postępującą akumulację lizosomalną oligosacharydów bogatych w mannozę we wszystkich tkankach, co prowadzi do upośledzenia funkcji komórkowych i apoptozy (ryc. 2). Całkowity brak funkcjonalności tego enzymu prowadzi do śmierci we wczesnym dzieciństwie z powodu pogorszenia stanu ośrodkowego układu nerwowego . Enzymy o niskiej aktywności resztkowej prowadzą do łagodniejszej postaci choroby, z objawami takimi jak upośledzenie słuchu, upośledzenie funkcji poznawczych, podatność na infekcje bakteryjne i deformacje szkieletu. Przebieg choroby jest postępujący.
W zależności od ciężkości choroby alfa-mannozydozę podzielono na trzy proponowane podtypy, w zależności od ciężkości i wieku zachorowania.
- Typ 1: Łagodna postać, rozpoznawana po ukończeniu dziesięciu lat, bez nieprawidłowości szkieletowych, problemów z mięśniami (miopatia) i powolnym postępem
- Typ 2: Umiarkowana postać, rozpoznana przed ukończeniem 10 roku życia, z obecnością nieprawidłowości szkieletowych, miopatią i powolnym postępem. Jest to najczęstsza forma
- Typ 3: ciężka postać, prowadząca do przedwczesnej śmierci z powodu postępującego zajęcia ośrodkowego układu nerwowego
Jednak biorąc pod uwagę różnorodność udokumentowanych mutacji oraz szeroki zakres i nasilenie objawów, choroba jest klinicznie uważana za kontinuum.
Diagnoza
Alfa-mannozydoza jest schorzeniem postępującym, a jej obecność należy podejrzewać u pacjentów z zaburzeniami poznawczymi, zmianami szkieletowymi (np. obrzęk stawów, skrzywienie kręgosłupa), niedosłuchem i nawracającymi infekcjami. Chociaż dzieci z tą chorobą często rodzą się pozornie normalne, ich stan pogarsza się wraz z wiekiem. Alfa-mannozydoza może wpływać na jakość życia pacjenta na wiele sposobów, w tym na jego zdolność do niezależnego życia, kontaktów towarzyskich lub znalezienia zatrudnienia.
Ogólnie rzecz biorąc, fenotypy pacjentów z alfa-mannozydozą nie są wyraźnie rozróżnialne, co sprawia, że przewidywanie przebiegu klinicznego dla indywidualnego pacjenta jest trudne. Pacjenci mogą zgłaszać się do lekarzy, pielęgniarek lub pielęgniarek środowiskowych na różnych etapach progresji iz różnymi ad hoc , co utrudnia powiązanie z podejrzeniem rozpoznania alfa-mannozydozy. Główne objawy można również podzielić z objawami innych lizosomalnych zaburzeń spichrzeniowych, takich jak mukopolisacharydoza .
Biorąc pod uwagę postępujący charakter choroby, im wcześniej zostanie postawiona właściwa diagnoza, tym lepiej. Schorzenie jest często diagnozowane i leczone z wykorzystaniem podejścia multidyscyplinarnego, z udziałem pediatrów, ortopedów, okulistów, otologów, neurologów, immunologów, neurochirurgów i fizjoterapeutów.
Podejrzenie alfa-mannozydozy stawia się na podstawie identyfikacji charakterystycznych objawów wieloobjawowej prezentacji, dokładnej oceny klinicznej, szczegółowego wywiadu pacjenta oraz wyników testów diagnostycznych opisanych poniżej:
A. Oligosacharydy w moczu
Można przeprowadzić wstępne badanie w celu zmierzenia stężenia oligosacharydów bogatych w mannozę w moczu. Podwyższone wydalanie z moczem oligosacharydów bogatych w mannozę jest sugestią, ale nie diagnostyczną choroby.
B. Aktywność kwaśnej alfa-mannozydazy
Diagnozę potwierdza się, mierząc resztkową aktywność alfa-mannozydazy w leukocytach lub innych komórkach jądrzastych za pomocą testu fluorometrycznego. Jest to najbardziej wiarygodna metoda diagnostyczna, obok badań genetycznych.
C. Testy genetyczne
Identyfikację mutacji powodujących chorobę uzyskuje się za pomocą DNA z komórek krwi obwodowej, poprzez amplifikację reakcji łańcuchowej polimerazy (PCR) wszystkich 24 eksonów MAN2B1, a następnie sekwencjonowanie DNA.
Leczenie
Nie ma lekarstwa na wrodzoną alfa-mannozydozę i ogólnie podejście do leczenia jest proaktywne, mające na celu zapobieganie pojawiającym się powikłaniom. Po pełnym badaniu fizykalnym lekarze powinni skupić się na znanych powikłaniach alfa-mannozydozy, takich jak wodogłowie, zapalenie ucha środkowego, utrata słuchu, próchnica zębów, objawy stawowe, kifoskolioza i stan psychiczny. Leczenie często ogranicza się do zmniejszania lub kontrolowania objawów choroby, na przykład za pomocą leków kontrolujących napady padaczkowe, aparatów słuchowych poprawiających ubytek słuchu oraz rutynowej fizjoterapii wspomagającej ból i osłabienie mięśni. W niektórych przypadkach wózek inwalidzki może być odpowiedni, jeśli upośledzenie mięśni lub kręgosłupa unieruchamia osobę dotkniętą chorobą.
Przeszczep krwiotwórczych komórek macierzystych (HSCT) może być opcją terapeutyczną dla niektórych pacjentów, jednak profil ryzyka i korzyści jest korzystniejszy u młodszych pacjentów, dlatego zapewnienie wczesnej diagnozy ma kluczowe znaczenie, aby była to opłacalna opcja. Uzasadnieniem jest to, że komórki dawcy produkujące enzymy ponownie zaludniają tkankę gospodarza i przenoszą enzym do pobliskich komórek gospodarza z niedoborem enzymu. Pomimo wczesnych doniesień przeciwnych, możliwe korzyści z HSCT należy porównać z ogólnym ryzykiem zachorowalności i śmiertelności związanej z zabiegiem. Korzyści są większe u młodszych pacjentów, zanim rozwiną się powikłania, a powikłania związane z przeszczepem są częstsze i cięższe u starszych pacjentów.
Enzymatyczna terapia zastępcza (ERT) jest alternatywą terapeutyczną w wielu lizosomalnych chorobach spichrzeniowych. Ogólna zasada ERT polega na tym, że rekombinacyjnie wersja niedoboru enzymu jest wprowadzana do krwioobiegu, skąd jest internalizowana przez komórki i dociera do lizosomów poprzez wychwyt za pośrednictwem receptora mannozo-6-fosforanu, zastępując w ten sposób brakujący endogenny enzym . ERT jest zatwierdzony do użytku w Unii Europejskiej.
Rokowanie
Długoterminowa prognoza stanu jest zła. Ogólnie rzecz biorąc, przez dziesięciolecia następuje powolny postęp zmian nerwowo-mięśniowych i kostnych. Mogą również występować problemy behawioralne lub zaburzenia psychiczne. Oczekiwana długość życia w alfa-mannozydozie jest bardzo zmienna. Osoby z wczesnym początkiem ciężkiej choroby często nie przeżywają poza dzieciństwem, podczas gdy osoby z łagodniejszymi zaburzeniami mogą dobrze przeżyć dorosłe życie.
Niezależne życie będzie trudne, a pacjenci z alfa-mannozydozą mogą zostać odizolowani społecznie, aw późnych stadiach choroby mogą poruszać się na wózku inwalidzkim, ponieważ nie będą już mogli samodzielnie chodzić. Może to mieć negatywny wpływ na jakość życia opiekunów i członków rodziny.
Epidemiologia
Światowa częstość występowania alfa-mannozydozy nie jest dokładnie znana. Jednak wiele raportów z różnych krajów szacuje, że występuje u około jednego na milion dzieci urodzonych na całym świecie. Mannozydoza występuje we wszystkich grupach etnicznych w Europie, Ameryce, Afryce i Azji.
Dalsza lektura
- Wpis GeneReviews/NCBI/NIH/UW na temat alfa-mannozydozy
- Wpisy OMIM dotyczące alfa-mannozydozy
- Alfa-mannozydoza typu 1 w Biurze Chorób Rzadkich NIH
- Alfa-mannozydoza typu 2 w Biurze Chorób Rzadkich NIH