Powierzchnia postrema
| Area postrema | |
|---|---|
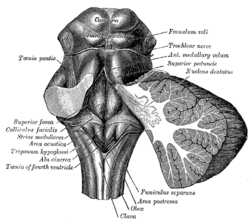 Romboidalny dół. (Obszar postrema oznaczony na dole pośrodku.)
| |
 Opis widoku z tyłu ogonowego pnia mózgu człowieka (Obszar postrema to nr 8)
| |
| Szczegóły | |
| Część | Rdzeń |
| Identyfikatory | |
| akronim(y) | AP |
| Siatka | D031608 |
| NeuroNazwy | 772 |
| Identyfikator NeuroLexa | birnlex_2636 |
| TA98 | A14.1.04.258 |
| TA2 | 6009 |
| FMA | 72607 |
| Anatomiczne warunki neuroanatomii | |
Obszar postrema , sparowana struktura w rdzeniu przedłużonym pnia mózgu , jest narządem okołokomorowym posiadającym przepuszczalne naczynia włosowate i neurony czuciowe , które umożliwiają mu podwójną rolę w wykrywaniu krążących przekaźników chemicznych we krwi i przekształcaniu ich w sygnały i sieci nerwowe . Jego położenie w sąsiedztwie obustronnych jąder przewodu samotnego i rola jako przetwornika czuciowego pozwalają mu na integrację krwi z mózgiem funkcje autonomiczne . Takie role obszaru postrema obejmują wykrywanie krążących hormonów zaangażowanych w wymioty , pragnienie , głód i kontrolę ciśnienia krwi .
Struktura
Obszar postrema to sparowana wypukłość znajdująca się na dolno-tylnej granicy komory czwartej . Wyspecjalizowane komórki wyściółki znajdują się w obszarze postrema. Komórki te różnią się nieznacznie od większości komórek wyściółczaków (ependymocytów), tworząc jednokomórkową nabłonkową wyściółkę komór i kanału środkowego . Obszar postrema jest oddzielony od trójkąta nerwu błędnego przez funiculus separans , cienki półprzezroczysty grzbiet. Trójkąt nerwu błędnego pokrywa grzbietowe jądro nerwu błędnego i znajduje się na ogonowym końcu romboidalny dół lub „podłoga” czwartej komory. Obszar postrema znajduje się tuż przed obex , dolnym wierzchołkiem dna komory ogonowej. Zarówno funiculus separans, jak i area postrema mają podobną grubą warstwę tanycytów zawierającą wyściółkę. Ependyma i tanycyty mogą uczestniczyć w transporcie neurochemikaliów do iz płynu mózgowo-rdzeniowego z jego komórek lub sąsiednich neuronów, gleju lub naczyń. Ependyma i tanycyty mogą również uczestniczyć w chemorecepcji.
Obszar postrema jest uważany za narząd okołokomorowy ze względu na jego bliskość do układu komorowego . W morfologicznym wykazano , że naczynia włosowate obszaru postrema w podregionie brzusznym obszaru postrema są stosunkowo nieprzepuszczalne, podobnie jak naczynia włosowate mózgu, podczas gdy naczynia włosowate obszaru postrema przyśrodkowego i grzbietowego mają cechy mikroskopowe o wysokiej przepuszczalności, cechę zwaną sinusoidalną . Subregionalna gęstość naczyń włosowatych obszaru postrema była najwyższa w pobliżu interfejsu komorowego i była prawie dwukrotnie większa niż gęstość naczyń włosowatych sąsiedniego pojedynczego jądra (SN) i grzbietowego jądra motorycznego nerwu błędnego . Bariera tanycytów częściowo kompensuje wysoką przepuszczalność naczyń włosowatych w obszarze postrema.
Fizjologiczne subregionalne badania obszaru postrema wykazały, że jego objętość krwi jest stosunkowo duża, a przepływ krwi i czas przejścia dla markerów krwi są stosunkowo wolne, co wzmacnia zdolność wykrywania krążących związków, takich jak hormony lub przekaźniki.

Znajomości
Obszar postrema łączy się z pojedynczym jądrem lub jądrem tractus solitarii (NTS) i innymi autonomicznymi ośrodkami kontroli w pniu mózgu . Jest pobudzany przez trzewne impulsy doprowadzające (współczulny i błędny) pochodzące z przewodu pokarmowego i innych obwodowych stref wyzwalających oraz czynniki humoralne . Obszar postrema tworzy część grzbietowego kompleksu nerwu błędnego, który jest krytycznym miejscem zakończenia aferentnych włókien nerwowych nerwu błędnego , wraz z grzbietowym jądrem motorycznym nerwu błędnego i NTS.
Nudności są najprawdopodobniej wywoływane przez stymulację obszaru postrema poprzez jego połączenie z NTS, co może służyć jako początek szlaku wywołującego wymioty w odpowiedzi na różne bodźce wymiotne . Jednak ta struktura nie odgrywa kluczowej roli w nudnościach wywołanych aktywacją włókien nerwu błędnego lub ruchem, a jej funkcja w wymiotach wywołanych promieniowaniem pozostaje niejasna.
Ponieważ obszar postrema i wyspecjalizowany region NTS mają przepuszczalne naczynia włosowate , peptydy i inne sygnały hormonalne we krwi mają bezpośredni dostęp do neuronów obszarów mózgu, które odgrywają istotną rolę w autonomicznej kontroli organizmu. W rezultacie obszar postrema jest uważany za miejsce integracji różnych sygnałów fizjologicznych we krwi, gdy wchodzą one do ośrodkowego układu nerwowego .
Funkcjonować
Chemorecepcja
Obszar postrema, jeden z narządów okołokomorowych , wykrywa toksyny we krwi i działa jako ośrodek wywołujący wymioty. Obszar postrema jest krytycznym centrum integracji homeostatycznej dla sygnałów humoralnych i nerwowych dzięki swojej funkcji jako strefa wyzwalająca chemoreceptor dla wymiotów w odpowiedzi na leki wymiotne . Jest to gęsto unaczyniona struktura z subregionalnymi specjalizacjami naczyń włosowatych zapewniających wysoką przepuszczalność dla krążących sygnałów krwi, umożliwiając jej wykrywanie różnych przekaźników chemicznych we krwi i płyn mózgowo-rdzeniowy . Wydaje się, że przepływ krwi w naczyniach włosowatych jest wyjątkowo powolny w obszarze postrema, co wydłuża czas kontaktu hormonów przenoszonych przez krew z receptorami neuronalnymi zaangażowanymi w regulację ciśnienia krwi, płynów ustrojowych i reakcji wymiotnych.
Regulacja autonomiczna
Fenestrowane sinusoidalne naczynia włosowate obszaru postrema i wyspecjalizowany region NTS sprawiają, że ten konkretny region rdzenia jest krytyczny w autonomicznej kontroli różnych układów fizjologicznych, w tym układu sercowo-naczyniowego oraz układów kontrolujących odżywianie i metabolizm. Angiotensyna II powoduje zależny od dawki wzrost ciśnienia tętniczego krwi bez powodowania znacznych zmian częstości akcji serca , w czym pośredniczy obszar postrema.
Znaczenie kliniczne
Szkoda
Uszkodzenie obszaru postrema, spowodowane głównie uszkodzeniem lub ablacją , uniemożliwia normalne funkcjonowanie obszaru postrema. Ta ablacja jest zwykle wykonywana chirurgicznie i ma na celu odkrycie dokładnego wpływu obszaru postrema na resztę ciała. Ponieważ obszar postrema działa jako punkt wejścia do mózgu dla informacji z neuronów czuciowych w żołądku, jelitach, wątrobie, nerkach, sercu i innych narządach wewnętrznych różne odruchy fizjologiczne polegają na przekazywaniu informacji przez obszar postrema. Obszar postrema działa bezpośrednio monitorując stan chemiczny organizmu. Uszkodzenia obszaru postrema są czasami określane jako „centralna wagotomia”, ponieważ eliminują zdolność mózgu do monitorowania stanu fizjologicznego organizmu poprzez nerw błędny. Zmiany te służą zatem zapobieganiu wykryciu trucizn, aw konsekwencji zapobieganiu uruchamianiu naturalnych mechanizmów obronnych organizmu. W jednym przykładzie eksperymenty przeprowadzone przez Bernsteina i in. na szczurach wskazywały, że obszar postrema zmian uniemożliwiał wykrycie chlorek litu , który w wysokich stężeniach może stać się toksyczny. Ponieważ szczury nie były w stanie wykryć substancji chemicznej, nie były w stanie zastosować procedury psychologicznej znanej jako niechęć do smaku kondycjonowanie, powodując ciągłe połykanie przez szczura roztworu sacharyny sparowanej z litem. Odkrycia te wskazują, że szczury z obszarowymi uszkodzeniami postrema nie nabywają normalnej warunkowej awersji smakowej, gdy jako bodziec bezwarunkowy stosuje się chlorek litu. Oprócz prostych awersji smakowych, szczury z obszarowymi zmianami postrema nie wykazywały innych reakcji behawioralnych i fizjologicznych związanych z wprowadzeniem toksyny i obecnych w grupie kontrolnej, takich jak położenie się na brzuchu, opóźnione opróżnianie żołądka i hipotermia. Takie eksperymenty podkreślają znaczenie obszaru postrema nie tylko w identyfikacji substancji toksycznych w organizmie, ale także w wielu fizycznych reakcjach na toksynę.
Wpływ dopaminy
Obszar postrema również odgrywa znaczącą rolę w dyskusji na temat choroby Parkinsona . Leki leczące chorobę Parkinsona za pomocą dopaminy mają silny wpływ na obszar postrema. Leki te stymulują przekazywanie dopaminy i próbują normalizować funkcje motoryczne dotknięte chorobą Parkinsona. Działa to, ponieważ komórki nerwowe, w szczególności w zwojach podstawy , który odgrywa kluczową rolę w regulacji ruchu i jest głównym miejscem patologii choroby Parkinsona, wykorzystują dopaminę jako neuroprzekaźnik i są aktywowane przez leki, które zwiększają stężenie dopaminy lub działają stymulująco na receptory dopaminy. Dopamina może również stymulować obszar postrema, ponieważ ta część mózgu zawiera dużą gęstość receptorów dopaminy. Obszar postrema jest bardzo wrażliwy na zmiany toksyczności krwi i wyczuwa obecność trujących lub niebezpiecznych substancji we krwi. Jako mechanizm obronny obszar postrema wywołuje wymioty, aby zapobiec dalszemu zatruciu. Duża gęstość receptorów dopaminy w obszarze postrema czyni go bardzo wrażliwym na leki zwiększające dopaminę. Stymulacja receptorów dopaminy w obszarze postrema aktywuje te ośrodki wymiotne w mózgu; dlatego nudności są jednym z najczęstszych skutków ubocznych leki przeciw parkinsonizmowi .
Historia
Obszar postrema został po raz pierwszy nazwany i zlokalizowany w ogólnej anatomii mózgu przez Magnusa Gustafa Retziusa , szwedzkiego anatoma, antropologa i profesora histologii . W 1896 roku opublikował dwutomową monografię na temat ogólnej anatomii ludzkiego mózgu, w której wspomniano o obszarze postrema. [ potrzebne źródło ] W 1975 roku opublikowano dowody na istnienie neuronów w obszarze postrema kilku gatunków ssaków.
Naukowcy coraz bardziej interesowali się badaniami wymiotów w latach pięćdziesiątych XX wieku, być może częściowo ze względu na zwiększoną świadomość społeczeństwa na temat choroby popromiennej , stanu, w którym wielu pacjentów wymiotujących po ekspozycji na promieniowanie zmarło. Badania wykazały istnienie dwóch obszarów w mózgu związanych z wymiotami: jeden, chemosensor wymiotów bez funkcji koordynacyjnej, zlokalizowany w czwartej komorze i drugi, koordynator wymiotów bez funkcji chemosensorycznej, zlokalizowany w bocznej formacji siateczkowatej rdzeń przedłużony. [ potrzebne źródło ]
W 1953 roku Borison i Wang ustalili, że obszar chemosensora działa jak strefa wyzwalania wymiotów w pniu mózgu, którą nazwali strefą wyzwalania chemoreceptorów (CTZ) dla wymiotów. Wykorzystując koty i psy jako organizmy modelowe, odkryli, że usunięcie tej strefy spustowej z mózgu pozwoliło na zapobieganie wymiotom u zwierząt bezpośrednio po wstrzyknięciu pewnych substancji chemicznych do krwi, wykazując istnienie związku między strefą wyzwalającą a akt wymiotów. CTZ zlokalizowano anatomicznie w obszarze postrema rdzenia przedłużonego. Obszar postrema został anatomicznie zidentyfikowany i nazwany prawie 60 lat wcześniej, ale jego funkcja pozostawała nieznana, dopóki nie potwierdzono później jego roli w wymiotach.
Obecne badania
Badania nad funkcjami obszaru postrema są kontynuowane do dziś na całym świecie. Poza rolą, jaką odgrywa w wymiotach, intensywnie badaną przez naukowców z połowy XX wieku, aktywność obszaru postrema została ściśle powiązana z innymi funkcjami autonomicznymi, takimi jak regulacja przyjmowania pokarmu, homeostaza płynów ustrojowych i regulacja układu sercowo-naczyniowego, poprzez badania behawioralne i badania elektrofizjologiczne . W 2007 roku w Japonii prowadzono badania nad mechanizmem pobudliwości neuronów area postrema przez zewnątrzkomórkowy ATP. Zacisk napięcia techniki rejestrowania całych komórek zastosowano na skrawkach mózgu szczura. Wyniki pokazały, że większość odpowiedzi na ATP ma charakter pobudzający i że pośredniczą w nich określone purinoceptory P2 znajdujące się w obszarze postrema. Rola obszaru postrema w awersji i preferencjach uwarunkowanych smakiem była badana w 2001 roku przez naukowców z Brooklyn College na City University of New York . W eksperymencie przetestowano wpływ uszkodzeń obszaru postrema u szczurów na ich zdolność uczenia się warunkowanej smakiem awersji do smaków w połączeniu z toksycznymi lekami, co rzeczywiście wykazało, że uszkodzenia obszaru postrema prowadzą do upośledzenia uczenia się niechęci do smaku. Badanie z 2009 roku śledziło rozwój obszaru postrema, wykorzystując model małpy makaka, próbując zidentyfikować i scharakteryzować przekaźnictwo nerwowe w tym regionie, a także rozwiązać wybitne niezgodności w badaniach. Naukowcy ci stwierdzili w kulminacji, że poprzednie badania sugerują noradrenalinę i/lub dopamina powoduje fluorescencję CA w obszarze postrema macaque-CA, co oznacza katecholaminergiczny lub pochodzący z aminy i funkcjonujący jako neuroprzekaźnik lub hormon lub jedno i drugie. W badaniu znaleziono jednak dowody na wydzielanie neuroprzekaźników zamiast uwalniania w pęcherzykach. Ponadto ich odkrycia wykazały, że GABA jest głównym neuroprzekaźnikiem w obszarze postrema, a nie glutaminianem . Trwające badania wciąż ujawniają rozbieżności między różnymi modelami badań szczurów, kotów, a teraz makaków.
Potencjalne zabiegi
Badanie przeprowadzone w Japonii w 2002 roku testowało lek, który może być przydatny w ograniczaniu reakcji wymiotnej na leki zwiększające stężenie dopaminy. W badaniu zbadano wymioty wywołane morfiną u fretek, wyjaśniając, że ekspozycja na morfinę wyzwalała uwalnianie dopaminy w rdzeniu przedłużonym iw obszarze postrema poprzez aktywację receptorów opiatowych, co z kolei powodowało wymioty u fretek. Jednak wstępne leczenie 6-hydroksydopaminą, neurotoksyną dopaminergiczną, znacznie zmniejszyło liczbę epizodów wymiotnych u fretek po ekspozycji na morfinę. Ta neurotoksyna obniża poziom dopaminy, noradrenaliny i kwasu homowanilowego, metabolitu dopaminy, i wiadomo, że niszczy neurony noradrenergiczne i dopaminergiczne. Tutaj 6-hydroksydopaminę wstrzyknięto bezpośrednio do rdzenia przedłużonego, ale nie w inne części mózgu. To badanie pokazuje, w jaki sposób można manipulować szlakiem dopaminergicznym w rdzeniu przedłużonym w celu zmniejszenia mdlących skutków ubocznych związanych z tak wieloma lekami zwiększającymi dopaminę.
Kontynuacja badań patologicznych
Obszar postrema jest również wskazany w leczeniu insuliną cukrzycy typu 1 i typu 2. Szczególny mechanizm działania leku pramlintyd działa głównie na obszar postrema i powoduje zmniejszenie wydzielania glukagonu , co z kolei spowalnia opróżnianie żołądka i efekt sytości. To ukierunkowanie na obszar postrema pozwala na poprawę glikemii bez powodowania przyrostu masy ciała. Ponieważ lek działa na obszar postrema, dawki należy miareczkować powoli, aby uniknąć wywołania nudności u pacjenta.
Nadal trwają również badania mające na celu określenie wpływu ablacji obszaru postrema na nadciśnienie tętnicze i czynność układu sercowo-naczyniowego. Na przykład badania na szczurach i królikach wskazują, że angiotensyny II jest znoszone przez uszkodzenie obszaru postrema. Mechanizm tej reakcji fizjologicznej wciąż nie jest w pełni poznany, ale zdolność obszaru postrema do regulacji czynności układu krążenia stanowi bardzo interesujący kierunek dla neuroendokrynologii.