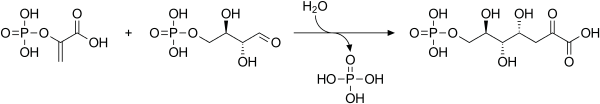7-fosforan kwasu 3-deoksy- D -arabino-heptulozonowego

Projekcja Fischera DAHP
|
|
| nazw | |
|---|---|
|
Preferowana nazwa IUPAC
(4R , 5S , 6R ) -4,5,6-Trihydroksy-2-okso-7-(fosfonooksy)heptanowy |
|
| Inne nazwy fosforan kwasu 3-dezoksy - D - heptulozonowego 3-dezoksy- D - arabino -heptulozonian-7-fosforan DAHP 7-fosfo-2-dehydro-3-deoksy- D - arabino - heptonian |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
|
Identyfikator klienta PubChem
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 7 H 13 O 10 P | |
| Masa cząsteczkowa | 288,145 g·mol -1 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
7-fosforan kwasu 3-deoksy - D - arabino -heptulozonowego ( DAHP ) to 7-węglowy kwas ulonowy . Związek ten bierze udział w szlaku biosyntezy kwasu szikimowego i jest półproduktem w produkcji aminokwasów aromatycznych .
Fosfenolopirogronian i erytrozo-4-fosforan reagują, tworząc 3-dezoksy- D - arabino -heptulosonano-7-fosforan (DAHP), w reakcji katalizowanej przez enzym syntazę DAHP .
DAHP jest następnie przekształcany w 3-dehydrochinian (DHQ) w reakcji katalizowanej przez syntazę DHQ . Chociaż ta reakcja wymaga dinukleotydu nikotynoamidoadeninowego (NAD) jako kofaktora, mechanizm enzymatyczny go regeneruje, co skutkuje całkowitym zużyciem NAD.
-
 Biosynteza chinianu katalizowana przez syntazę 3-dehydrochinanu.
Biosynteza chinianu katalizowana przez syntazę 3-dehydrochinanu.
Mechanizm zamykania pierścienia jest złożony, ale obejmuje kondensację aldolową przy C-2 i C-7.
Inżynieria metaboliczna poprawiła produkcję DAHP przez Escherichia coli . Pierwszy etap, kondensacja 7-fosforanu kwasu 3-dezoksy- D - arabino -heptulozonowego (DAHP) z PEP/E4P, wykorzystuje trzy izoenzymy AroF, AroG i AroH. Każdy z nich ma swoją syntezę regulowaną odpowiednio z tyrozyny, fenyloalaniny i tryptofanu. Wszystkie te izoenzymy mają zdolność regulowania syntezy DAHP metodą hamowania ze sprzężeniem zwrotnym. Działa to w komórce poprzez monitorowanie stężenia każdego z trzech aminokwasów aromatycznych. Kiedy któregokolwiek z nich jest za dużo, ten będzie allosterycznie kontrolował syntetazę DAHP, „wyłączając ją”. Po wyłączeniu pierwszego etapu wspólnego szlaku synteza trzech aminokwasów nie może przebiegać. Reszta enzymów znajduje się na wspólnej ścieżce (konwersja DAHP do choryzmatu).
-
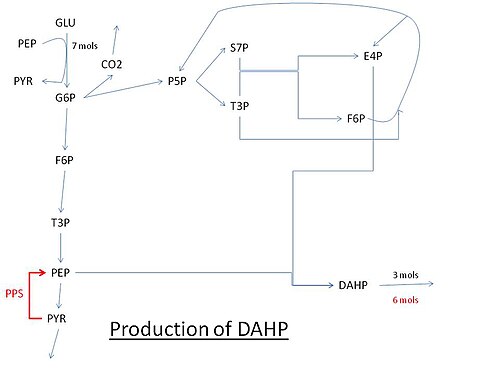 Droga do produkcji DAHP przy użyciu glukozy . Skróty: GLU: glukoza, G6P: glukozo-6-fosforan, PEP: fosfoenolopirogronian, PYR: pirogronian, F6P: fruktozo-6-fosforan, P5P: pentozo-5-fosforan (ryboza lub 5-fosforan ksylulozy) T3P: aldehyd 3-fosforanowy, S7P : 7-fosforan sedoheptulozy , E4P: 4-fosforan erytrozy, PPS: syntaza PEP .
Droga do produkcji DAHP przy użyciu glukozy . Skróty: GLU: glukoza, G6P: glukozo-6-fosforan, PEP: fosfoenolopirogronian, PYR: pirogronian, F6P: fruktozo-6-fosforan, P5P: pentozo-5-fosforan (ryboza lub 5-fosforan ksylulozy) T3P: aldehyd 3-fosforanowy, S7P : 7-fosforan sedoheptulozy , E4P: 4-fosforan erytrozy, PPS: syntaza PEP .
Linki zewnętrzne
- Webby, Celia J.; Piekarz, Heather M.; Lott, J. Shaun; Baker, Edward N.; Parker, Emily J. (2005). „Struktura syntazy 3-dezoksy D - arabino -heptulosonianu 7-fosforanu z Mycobacterium tuberculosis ujawnia wspólne rusztowanie katalityczne i pochodzenie dla enzymów typu I i II”. Journal of Molecular Biology . 354 (4): 927–39. doi : 10.1016/j.jmb.2005.09.093 . PMID 16288916 .