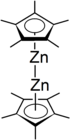dekametylodizynkocen
|
|
|||
| Identyfikatory | |||
|---|---|---|---|
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
|
Identyfikator klienta PubChem
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 20 H 30 Zn 2 | |||
| Masa cząsteczkowa | 401,22 g·mol -1 | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Dekametylodizinkocen jest związkiem cynkoorganicznym o wzorze [Zn 2 (η 5 –C 5 Me 5 ) 2 ]. Jest to pierwszy i nietypowy przykład związku z wiązaniem Zn-Zn. Dekametylodizinkocen jest bezbarwną krystaliczną substancją stałą , która w obecności tlenu spala się samorzutnie i reaguje z wodą. Jest stabilny w temperaturze pokojowej i szczególnie rozpuszczalny w eterze dietylowym , benzenie , pentanie lub tetrahydrofuranie .
Synteza
Zdolność metali do tworzenia heterojądrowych lub homojądrowych wiązań metal-metal zmienia się w całym układzie okresowym pierwiastków . Wśród pierwiastków z grupy 12 rtęć z łatwością tworzy jednostki [MM] 2+ , podczas gdy pierwiastki kadm i cynk stanowią mniej przykładów takich związków. Dekametylodizinkocen został opisany w 2004 roku przez Carmona i współpracowników jako nieoczekiwany produkt reakcji pomiędzy dekametylozinkocenem (Zn(C 5Me 5 ) 2 ) i dietylocynkiem (ZnEt 2 ).
- 2 (η 5 -C 5 Me 5 ) 2 Zn + Et 2 Zn → (η 5 -C 5 Me 5 ) 2 Zn 2 + 2 (η 5 -C 5 Me 5 )ZnEt + węglowodór(y)
Analogiczna reakcja cynkocenu (Zn(C 5 H 5 ) 2 ) z dietylocynkiem daje (η 5 -C 5 H 5 )ZnEt. Dlatego stabilizujący wpływ grup metylowych na pierścienie cyklopentadienylowe ma ogromne znaczenie w tworzeniu dekametydyzynkocenu. Szczególne znaczenie ma zastosowanie ZnEt 2 jako reagenta .
Ważny jest prekursor cynkoorganiczny. Difenylocynk (Zn(C 6 H 5 ) 2 ), pomimo mniejszej rozpuszczalności, może być stosowany zamiast ZnEt 2 . Z drugiej strony ZnMe 2 daje tylko związek półkanapkowy [(η 5 -C 5 Me 5 )ZnMe].
Zarówno (η 5 -C 5 Me 5 )ZnEt, jak i dekametylodizinkocen powstają w reakcji pomiędzy Zn(η 5 -C 5 Me 5 ) 2 i ZnEt 2 . Względne ilości zależą od warunków reakcji, które można zoptymalizować, aby faworyzować jedno lub drugie. tę reakcję prowadzi się w pentanie w temperaturze -40°C, jedynym produktem jest ( η5- C5Me5 ) ZnEt. I odwrotnie, jeśli reakcję prowadzi się w eterze dietylowym w temperaturze -10°C, głównym produktem jest ( Zn2 (η5 - C5Me5 ) 2 ) .
Nieprzewidywalność syntezy
Powstawanie dekametylodizincocenu jest jednak raczej nieprzewidywalne. Kilka powtórzeń tej reakcji (w warunkach sprzyjających powstawaniu dekametylodizinkocenu) w niewytłumaczalny sposób doprowadziło do powstania jedynie kompleksu półkanapkowego (η 5 -C 5 Me 5 )ZnEt. Powstawanie produktów (η 5 -C 5 Me 5 )ZnEt i Zn 2 (η 5 -C 5 Me 5 ) 2 zachodzi poprzez oddzielne, konkurencyjne ścieżki reakcji, a zatem te dwa produkty nie ulegają wzajemnej przemianie, gdy są pozostawione do przereagowania wydłużone okresy czasu.
Uważa się, że tworzenie kompleksu półkanapkowego zachodzi poprzez związki pośrednie z mostkami hydrokarbylowymi . Mechanizm reakcji jest jednak niepewny. Wcześniej wysunięto hipotezę, że powstanie dekametylodizinkocenu nastąpiło w wyniku rozkładu dietylocynku, którego produkty rozkładu miałyby zdolność redukowania dekametylozinkocenu do dekametylodizinkocenu. Jednak obecnie uważa się, że tworzenie dekametylodizinkocenu zachodzi w reakcji rodnikowej obejmującej połączenie dwóch rodników (η 5 -C 5 Me 5 )Zn • .
W nowej, bardziej wydajnej i bardziej ogólnej drodze do dekametylodizinkocenu, wodorek potasu jest stosowany do redukcji dekametylozinkocenu do dekametylodizinkocenu. Inne środki redukujące, takie jak K , Na lub CaH2 , mogą być również stosowane w redukcji dekametylocynkocenu do dekametylodizinkocenu.
Kompleks ten nie reaguje z zasadami Lewisa , takimi jak PMe 3 , PPh 3 , NEt 3 lub pirydyna , ani nie reaguje z H 2 , CO 2 lub CO. Związek ten wydaje się być nieskończenie trwały w temperaturze pokojowej (jednak przechowywanie w temperaturze -20 ° C) i sublimuje w pobliżu 70 ° C.
Struktura
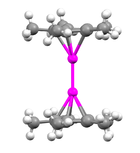
W celu określenia struktury dekametylodizinkocenu zastosowano różne metody, w tym dyfrakcję rentgenowską , 1H NMR i spektrometrię mas . Za pomocą metod dyfrakcji rentgenowskiej stwierdzono, że atomy cynku są umieszczone pomiędzy dwoma równoległymi pierścieniami C5Me5, których płaszczyzny są prostopadłe do osi wiązania metal- metal . Odległość między dwiema płaszczyznami pierścienia wynosi około 6,40 Å. Pierścienie C 5 Me 5 są w zaćmionej konformacji z podstawnikami metylowymi wygiętymi lekko na zewnątrz (z dala od centralnych atomów metalu) pod kątem od 3 do 6 stopni.
W jednojądrzastych metalocenach zginanie podstawników przyłączonych do pierścieni służy zapobieganiu zawady sterycznej ; jednakże promień grupy metylowej wynosi tylko 2,0 Å i dlatego zagięcie w dekametylodizincocenie nie służy temu celowi, ponieważ odległość między dwoma pierścieniami jest znacznie większa niż ta wartość. Uważa się, że w przypadku dekametylodizinkocenu wygięcie grup metylowych przyłączonych do ligandów cyklopentadienylowych jest preferencyjne, ponieważ koncentruje gęstość elektronową z dala od centralnych, dodatnio naładowanych atomów metalu. Odległość między każdym atomem Zn a środkiem przyłączonego do niego pierścienia cyklopentadienylu wynosi około 2,04 Å, a odległości Zn-C (pierścień) wahają się od 2,27 do 2,30 Å. Odległość wiązania Zn-Zn wynosi 2,305 Å, co wskazuje na dość silne wiązanie między dwoma atomami cynku. Można to porównać ze znaną długością wiązania [Hg-Hg] 2+ wynoszącą od 2,5 do 2,7 Å. Postawiono hipotezę dwóch odrębnych typów struktur dimetalocenów, w tym struktury współosiowej (która jest strukturą dekametylodizynkocenu) i struktury prostopadłej, w której oś wiązania metal-metal jest równoległa do płaszczyzny ligandów cyklopentadienylu (co przewiduje się być struktura dla dikuprocenów). Związek, o którym mowa w tym artykule, jest zasadniczo liniowy z kątami wiązań Zn-Zn wynoszącymi około 177°:
Brak ligandów mostkujących
1H NMR i spektrometrii masowej były przydatne w udowodnieniu, że dekametylodizynkocen nie zawiera ligandów mostkujących. To badanie jest ważne, biorąc pod uwagę, że kompleks, który wcześniej zakładano, że jest Co2 ( η5 - C5Me5 ) 2 , został później znaleziony przy użyciu 1H NMR i danych spektrometrii mas, co potwierdziły trzy wodory mostkowe. 1H NMR dekametylodizynkocenu pokazuje tylko jeden sygnał przy δ 2,02 z powodu wodorów przyłączonych do grup metylowych ligandów cyklopentadienylowych .
Struktura elektronowa i charakterystyka wiązania
Dekametylodizinkocen ma akumulację gęstości elektronowej między dwoma atomami cynku, co wskazuje na wiązanie. To wiązanie ma przewidywaną energię dysocjacji 62 kcal·mol -1 i jest w przybliżeniu tak silne jak wiązania metal- halogenek . Analiza NBO (Natural Bond Order) wykazała, że wiązanie sigma występuje między orbitalami 4s centralnych atomów metalu z zajętością orbitali wiążących wynoszącą 1,9445,9 Za pomocą analizy fragmentów orbitali molekularnych (FMOA) stwierdzono, że istnieje jeden główny orbital molekularny który bierze udział w wiązaniu Zn-Zn z około 88% charakterem wiązania skoncentrowanym między atomami Zn.