Spektroskopia magnetycznego rezonansu jądrowego
Spektroskopia magnetycznego rezonansu jądrowego , najczęściej znana jako spektroskopia NMR lub spektroskopia rezonansu magnetycznego ( MRS ), jest techniką spektroskopową służącą do obserwacji lokalnych pól magnetycznych wokół jąder atomowych . Próbkę umieszcza się w polu magnetycznym, a sygnał NMR jest wytwarzany przez wzbudzenie próbki jądra falami radiowymi do jądrowego rezonansu magnetycznego , który jest wykrywany za pomocą czułych odbiorników radiowych. Wewnątrzcząsteczkowe pole magnetyczne wokół atomu w cząsteczce zmienia częstotliwość rezonansową, dając w ten sposób dostęp do szczegółów budowy elektronowej cząsteczki i jej poszczególnych grup funkcyjnych. Ponieważ pola są unikalne lub bardzo charakterystyczne dla poszczególnych związków, we współczesnym chemii organicznej , spektroskopia NMR jest ostateczną metodą identyfikacji jednocząsteczkowych związków organicznych .
Zasada NMR zwykle obejmuje trzy kolejne etapy:
- 0 Wyrównanie (polaryzacja) magnetycznych spinów jądrowych w przyłożonym, stałym polu magnetycznym B .
- Zakłócenie tego wyrównania spinów jądrowych przez słabe oscylujące pole magnetyczne , zwykle określane jako impuls o częstotliwości radiowej (RF).
- Detekcja i analiza fal elektromagnetycznych emitowanych przez jądra próbki w wyniku tego zaburzenia.
Podobnie biochemicy używają NMR do identyfikacji białek i innych złożonych cząsteczek. Oprócz identyfikacji, spektroskopia NMR dostarcza szczegółowych informacji o strukturze, dynamice, stanie reakcji i środowisku chemicznym cząsteczek. Najpopularniejszymi rodzajami NMR są protonów i spektroskopia NMR węgla-13 , ale ma ona zastosowanie do każdego rodzaju próbki zawierającej jądra posiadające spin .
Widma NMR są unikalne, dobrze rozdzielone, analitycznie wykonalne i często wysoce przewidywalne dla małych cząsteczek . Różne grupy funkcyjne są oczywiście rozróżnialne, a identyczne grupy funkcyjne z różnymi sąsiednimi podstawnikami nadal dają rozróżnialne sygnały. NMR w dużej mierze zastąpił tradycyjne mokre testy chemiczne, takie jak odczynniki barwiące lub typowa chromatografia do identyfikacji. Wadą jest to, że wymagana jest stosunkowo duża ilość, 2–50 mg oczyszczonej substancji, chociaż można ją odzyskać poprzez obróbkę. Najlepiej rozpuścić próbkę w rozpuszczalniku, ponieważ analiza NMR ciał stałych wymaga wirowania pod kątem magicznym maszyny i może nie dawać równie dobrze rozdzielczych widm. Skala czasowa NMR jest stosunkowo długa i dlatego nie nadaje się do obserwacji szybkich zjawisk, dając jedynie uśrednione widmo. Chociaż w widmie NMR widoczne są duże ilości zanieczyszczeń, istnieją lepsze metody wykrywania zanieczyszczeń, ponieważ NMR z natury nie jest bardzo czuły - chociaż przy wyższych częstotliwościach czułość jest wyższa.
Spektroskopia korelacyjna jest rozwinięciem zwykłego NMR. W dwuwymiarowym NMR emisja skupia się wokół jednej częstotliwości i obserwuje się skorelowane rezonanse. Pozwala to na identyfikację sąsiednich podstawników obserwowanej grupy funkcyjnej, pozwalając na jednoznaczną identyfikację rezonansów. Istnieją również bardziej złożone metody 3D i 4D oraz różne metody przeznaczone do tłumienia lub wzmacniania określonych typów rezonansów. W jądrowego efektu Overhausera (NOE) relaksacja obserwuje się rezonanse. Ponieważ NOE zależy od bliskości jąder, ilościowe określenie NOE dla każdego jądra pozwala na zbudowanie trójwymiarowego modelu cząsteczki.

Spektrometry NMR są stosunkowo drogie; uczelnie zazwyczaj je mają, ale rzadziej w firmach prywatnych. W latach 2000-2015 spektrometr NMR kosztował około 500 000 - 5 mln USD . Nowoczesne spektrometry NMR mają bardzo silny, duży i drogi nadprzewodzący chłodzony ciekłym helem , ponieważ rozdzielczość zależy bezpośrednio od natężenia pola magnetycznego . Dostępne są również tańsze maszyny wykorzystujące magnesy trwałe i o niższej rozdzielczości, które nadal zapewniają wystarczającą wydajność do niektórych zastosowań, takich jak monitorowanie reakcji i szybkie sprawdzanie próbek. Są nawet stołowe spektrometry magnetycznego rezonansu jądrowego . NMR można zaobserwować w polach magnetycznych mniejszych niż militesla. NMR o niskiej rozdzielczości daje szersze piki, które mogą łatwo nakładać się na siebie, powodując problemy w rozwiązywaniu złożonych struktur. Zastosowanie pól magnetycznych o większej sile skutkuje wyraźną rozdzielczością pików i jest standardem w przemyśle.
Historia
Za odkrycie NMR należy Isidor Isaac Rabi , który otrzymał Nagrodę Nobla w dziedzinie fizyki w 1944 roku. Grupa Purcella z Uniwersytetu Harvarda i grupa Blocha z Uniwersytetu Stanforda niezależnie opracowały spektroskopię NMR pod koniec lat czterdziestych i na początku pięćdziesiątych XX wieku. Edward Mills Purcell i Felix Bloch podzielili się Nagrodą Nobla w dziedzinie fizyki z 1952 roku za swoje odkrycia.
Podstawowe techniki NMR

Częstotliwość rezonansowa
Po umieszczeniu w polu magnetycznym jądra aktywne NMR (takie jak 1H lub 13C ) absorbują promieniowanie elektromagnetyczne o częstotliwości charakterystycznej dla izotopu . Częstotliwość rezonansowa, energia pochłanianego promieniowania i intensywność sygnału są proporcjonalne do natężenia pola magnetycznego. Na przykład w polu magnetycznym o natężeniu 21 tesli jądra wodoru (powszechnie nazywane protonami) rezonują z częstotliwością 900 MHz. Często określa się magnes 21 T jako 900 MHz magnes, ponieważ najczęściej wykrywanym jądrem jest wodór, jednak różne jądra będą rezonować z różnymi częstotliwościami przy tym natężeniu pola, proporcjonalnie do ich jądrowych momentów magnetycznych . [ potrzebne źródło ]
Obsługa próbek
Spektrometr NMR zwykle składa się z obracającego się uchwytu próbki wewnątrz bardzo silnego magnesu, nadajnika o częstotliwości radiowej i odbiornika z sondą (zespołem anteny), która wchodzi do wnętrza magnesu, aby otoczyć próbkę, opcjonalnie cewki gradientowe do pomiarów dyfuzji oraz elektronikę do sterowania systemem. Wirowanie próbki jest zwykle konieczne do uśrednienia ruchu dyfuzyjnego, jednak niektóre eksperymenty wymagają próbki stacjonarnej, gdy ruch roztworu jest ważną zmienną. Na przykład pomiary stałych dyfuzji ( spektroskopia uporządkowana dyfuzji lub DOSY) są wykonywane przy użyciu stacjonarnej próbki z odwirowywaniem, a komórki przepływowe mogą być wykorzystywane do analizy przepływów procesowych w trybie online.
Rozpuszczalniki deuterowane
Zdecydowana większość cząsteczek w roztworze to cząsteczki rozpuszczalnika, a większość zwykłych rozpuszczalników to węglowodory , a więc zawierają protony aktywne w NMR. Aby uniknąć wykrywania tylko sygnałów z atomów wodoru rozpuszczalnika, stosuje się rozpuszczalniki deuterowane, w których ponad 99% protonów jest zastąpionych deuterem ( wodór-2). Najszerzej stosowanym rozpuszczalnikiem deuterowanym jest deuterochloroform (CDCl 3 ), chociaż inne rozpuszczalniki mogą być stosowane z różnych powodów, takich jak rozpuszczalność próbki, chęć kontrolowania wiązań wodorowych lub temperatury topnienia lub wrzenia. Przesunięcia chemiczne cząsteczki będą się nieznacznie zmieniać między rozpuszczalnikami, a zastosowany rozpuszczalnik prawie zawsze będzie podawany z przesunięciami chemicznymi. Widma NMR są często kalibrowane względem znanego piku resztkowego protonu rozpuszczalnika zamiast dodanego tetrametylosilanu. [ potrzebne źródło ]
Podkładka i zamek
Aby wykryć bardzo małe przesunięcia częstotliwości spowodowane jądrowym rezonansem magnetycznym, przyłożone pole magnetyczne musi być stałe w całej objętości próbki. Spektrometry NMR o wysokiej rozdzielczości wykorzystują podkładki regulacyjne , aby dostosować jednorodność pola magnetycznego do części na miliard ( ppb ) w objętości kilku centymetrów sześciennych. W celu wykrycia i skompensowania niejednorodności i dryfu w polu magnetycznym spektrometr utrzymuje „blokadę” częstotliwości deuteru rozpuszczalnika za pomocą oddzielnej jednostki blokującej, która jest zasadniczo dodatkowym nadajnikiem i procesorem RF dostrojonym do jądra blokady (deuteru) zamiast jąder próbki będącej przedmiotem zainteresowania. W nowoczesnych spektrometrach NMR ustawienie podkładek jest regulowane automatycznie, chociaż w niektórych przypadkach operator musi ręcznie zoptymalizować parametry podkładek, aby uzyskać najlepszą możliwą rozdzielczość
Akwizycja widm
Po wzbudzeniu próbki impulsem o częstotliwości radiowej (60–1000 MHz) uzyskuje się odpowiedź jądrowego rezonansu magnetycznego - zanik swobodnej indukcji (FID). Jest to bardzo słaby sygnał i wymaga wrażliwych odbiorników radiowych do odbioru. Przeprowadzana jest transformata Fouriera w celu wyodrębnienia widma w dziedzinie częstotliwości z surowego FID w dziedzinie czasu. Widmo z pojedynczego FID ma niski stosunek sygnału do szumu , ale łatwo poprawia się wraz z uśrednianiem powtarzanych akwizycji. dobry 1 Widma H NMR można uzyskać z 16 powtórzeniami, co zajmuje tylko kilka minut. Jednak w przypadku pierwiastków cięższych od wodoru czas relaksacji jest dość długi, np. około 8 sekund dla 13 C. Zatem pozyskanie ilościowych widm pierwiastków ciężkich może być czasochłonne, od dziesiątek minut do godzin. [ potrzebne źródło ]
Po impulsie jądra są średnio wzbudzane pod pewnym kątem w stosunku do pola magnetycznego spektrometru. Zakres wzbudzenia można kontrolować za pomocą szerokości impulsu, zazwyczaj ok. 3-8 µs dla optymalnego impulsu 90°. Szerokość impulsu można określić, wykreślając intensywność (ze znakiem) jako funkcję szerokości impulsu. Podąża za krzywą sinusoidalną i odpowiednio zmienia znak przy szerokościach impulsów odpowiadających impulsom 180° i 360°. [ potrzebne źródło ]
Czasy rozpadu wzbudzenia, zwykle mierzone w sekundach, zależą od skuteczności relaksacji, która jest szybsza dla lżejszych jąder iw ciałach stałych, a wolniejsza dla cięższych jąder i roztworów, aw gazach może być bardzo długa. Jeśli drugi impuls wzbudzenia zostanie wysłany przedwcześnie przed zakończeniem relaksacji, średni wektor namagnesowania nie zaniknie do stanu podstawowego, co wpływa na siłę sygnału w nieprzewidywalny sposób. W praktyce obszary pików nie są wtedy proporcjonalne do stechiometrii; tylko obecność, ale nie ilość grup funkcyjnych jest możliwa do rozpoznania. Można przeprowadzić eksperyment odzyskiwania inwersji, aby określić czas relaksacji, a tym samym wymagane opóźnienie między impulsami. Wysyłany jest impuls 180°, regulowane opóźnienie i impuls 90°. Kiedy impuls 90° dokładnie anuluje sygnał, opóźnienie odpowiada czasowi potrzebnemu na relaksację 90°. Odzyskiwanie inwersji jest opłacalne ze względów ilościowych 13 C, 2D i inne czasochłonne eksperymenty.
Przesunięcie chemiczne
Wirujący ładunek wytwarza pole magnetyczne, które powoduje powstanie momentu magnetycznego proporcjonalnego do spinu. W obecności zewnętrznego pola magnetycznego istnieją dwa stany spinowe (dla jądra o spinie 1/2): jeden spin w górę i jeden w dół, gdzie jeden jest zgodny z polem magnetycznym, a drugi przeciwny. Różnica energii (ΔE) między dwoma stanami spinowymi wzrasta wraz ze wzrostem natężenia pola, ale różnica ta jest zwykle bardzo mała, co prowadzi do konieczności stosowania silnych magnesów NMR (1-20 T dla nowoczesnych instrumentów NMR). Napromieniowanie próbki energią odpowiadającą dokładnej separacji stanów spinowych określonego zbioru jąder spowoduje wzbudzenie zbioru jąder o niższym stanie energetycznym do stanu o wyższej energii. [ potrzebne źródło ]
W przypadku jąder o spinie 1/2 różnica energii między dwoma stanami spinowymi przy danym natężeniu pola magnetycznego jest proporcjonalna do ich momentu magnetycznego. Jednak nawet jeśli wszystkie protony mają takie same momenty magnetyczne, nie dają one sygnałów rezonansowych przy tych samych wartościach częstotliwości. Ta różnica wynika z różnych środowisk elektronicznych jądra będącego przedmiotem zainteresowania. Po przyłożeniu zewnętrznego pola magnetycznego elektrony te poruszają się w odpowiedzi na pole i generują lokalne pola magnetyczne, które przeciwstawiają się znacznie silniejszemu przyłożonemu polu. To lokalne pole „osłania” zatem proton przed przyłożonym polem magnetycznym, które musi zatem zostać zwiększone, aby osiągnąć rezonans (pochłanianie energii RF). Takie przyrosty są bardzo małe, zwykle w częściach na milion (ppm). Na przykład pik protonu z aldehydu jest przesunięty o ok. 10 ppm w porównaniu z pikiem węglowodorowym, ponieważ jako an grupa odciągająca elektrony , karbonyl odsłania proton, zmniejszając lokalną gęstość elektronów. Różnica między 2,3487 T a 2,3488 T wynosi zatem około 42 ppm. Jednak skala częstotliwości jest powszechnie używana do wyznaczania sygnałów NMR, mimo że spektrometr może działać na zasadzie omiatania pola magnetycznego, a zatem 42 ppm to 4200 Hz dla częstotliwości odniesienia (rf) 100 MHz.
Jednak biorąc pod uwagę, że lokalizacja różnych sygnałów NMR zależy od natężenia zewnętrznego pola magnetycznego i częstotliwości odniesienia, sygnały są zwykle podawane w odniesieniu do sygnału odniesienia, zwykle sygnału TMS (tetrametylosilanu ) . Dodatkowo, ponieważ rozkład sygnałów NMR jest zależny od pola, częstotliwości te są dzielone przez częstotliwość spektrometru. Ponieważ jednak dzielimy Hz przez MHz, wynikowa liczba byłaby zbyt mała, dlatego mnoży się ją przez milion. Ta operacja daje zatem numer lokalizatora zwany „przesunięciem chemicznym” z jednostkami części na milion. Ogólnie rzecz biorąc, przesunięcia chemiczne protonów są wysoce przewidywalne, ponieważ przesunięcia te są determinowane głównie prostszymi efektami ekranowania (gęstość elektronów), ale przesunięcia chemiczne wielu cięższych jąder są silniej uzależnione od innych czynników, w tym stanów wzbudzonych („paramagnetyczny” udział w ekranowaniu napinacz). [ potrzebne źródło ]
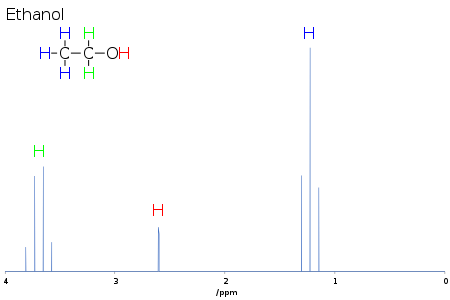
Przesunięcie chemiczne dostarcza informacji o strukturze cząsteczki. Konwersja surowych danych na te informacje nazywana jest przypisaniem widma. Na przykład dla 1H -NMR dla etanolu (CH 3 CH 2 OH) można by oczekiwać sygnałów przy każdym z trzech określonych przesunięć chemicznych: jednego dla grupy CH 3 , jednego dla grupy CH 2 i jednego dla grupa OH . Typowa grupa CH 3 ma przesunięcie około 1 ppm, a CH 2 przyłączony do OH ma przesunięcie około 4 ppm, a OH ma przesunięcie w dowolnym miejscu od 2 do 6 ppm, w zależności od użytego rozpuszczalnika i ilości wiązań wodorowych . Podczas gdy atom O odciąga gęstość elektronów od przyłączonego H poprzez wzajemne wiązanie sigma, samotne pary elektronów na O kąpią H w swoim efekcie ekranującym. [ potrzebne źródło ]
W spektroskopii paramagnetycznego NMR pomiary przeprowadza się na próbkach paramagnetycznych. Paramagnetyzm powoduje bardzo zróżnicowane przesunięcia chemiczne. W 1H NMR zakres przesunięć chemicznych może sięgać nawet tysięcy ppm.
Ze względu na ruch molekularny w temperaturze pokojowej, trzy protony metylowe uśredniają się podczas eksperymentu NMR (który zwykle wymaga kilku ms ). Te protony ulegają degeneracji i tworzą pik przy tym samym przesunięciu chemicznym.
Kształt i powierzchnia pików są również wskaźnikami struktury chemicznej. W powyższym przykładzie — widmie protonowym etanolu — pik CH3 ma trzykrotnie większą powierzchnię niż pik OH. Podobnie, pik CH2 byłby dwukrotnie większy niż obszar piku OH, ale tylko 2/3 obszaru piku CH3 .
Oprogramowanie pozwala na analizę intensywności sygnału pików, które w warunkach optymalnej relaksacji korelują z liczbą protonów tego typu. Analiza intensywności sygnału odbywa się poprzez całkowanie — proces matematyczny, który oblicza pole pod krzywą. Analityk musi scałkować pik, a nie mierzyć jego wysokość, ponieważ piki mają również szerokość — a zatem jego rozmiar zależy od jego powierzchni, a nie od wysokości. Należy jednak wspomnieć, że liczba protonów lub dowolnego innego obserwowanego jądra jest proporcjonalna do intensywności lub całki sygnału NMR tylko w najprostszych jednowymiarowych eksperymentach NMR. Na przykład w bardziej skomplikowanych eksperymentach, zwykle używanych do uzyskiwania węgla-13 , całka sygnałów zależy od szybkości relaksacji jądra oraz jego skalarnych i dipolarnych stałych sprzężenia. Bardzo często czynniki te są słabo znane - dlatego całka sygnału NMR jest bardzo trudna do interpretacji w bardziej skomplikowanych eksperymentach NMR.
sprzęgło typu J
| Wielość | Współczynnik intensywności |
|---|---|
| podkoszulek (s) | 1 |
| dublet (d) | 1:1 |
| Trójka (t) | 1:2:1 |
| kwartet (q) | 1:3:3:1 |
| Kwintet | 1:4:6:4:1 |
| Sekstet | 1:5:10:10:5:1 |
| septet | 1:6:15:20:15:6:1 |
Niektóre z najbardziej przydatnych informacji do określania struktury w jednowymiarowym widmie NMR pochodzą ze sprzężenia J lub sprzężenia skalarnego (specjalny przypadek sprzężenia spinowo-spinowego) między aktywnymi jądrami NMR. To sprzężenie wynika z interakcji różnych stanów spinowych poprzez wiązania chemiczne cząsteczki i skutkuje rozszczepieniem sygnałów NMR. W przypadku protonu lokalne pole magnetyczne jest nieco inne w zależności od tego, czy sąsiednie jądro jest skierowane w stronę, czy w przeciwną stronę pola magnetycznego spektrometru, co powoduje powstanie dwóch sygnałów na proton zamiast jednego. Te wzorce podziału mogą być złożone lub proste, a także mogą być łatwo interpretowalne lub zwodnicze. To sprzężenie zapewnia szczegółowy wgląd w połączenia atomów w cząsteczce. [ potrzebne źródło ]
Sprzężenie z n równoważnymi jądrami (spin ½) dzieli sygnał na multiplet n +1 ze stosunkami intensywności następującymi po trójkącie Pascala , jak opisano po prawej stronie. Sprzężenie z dodatkowymi spinami doprowadzi do dalszego rozszczepienia każdej składowej multipletu, np. sprzężenie z dwoma różnymi jądrami o spinie ½ o istotnie różnych stałych sprzężenia doprowadzi do dubletu dubletów (skrót: dd). Należy zauważyć, że sprzężenie między jądrami, które są chemicznie równoważne (to znaczy mają to samo przesunięcie chemiczne) nie ma wpływu na widma NMR, a sprzężenia między jądrami, które są odległe (zwykle więcej niż 3 wiązania od siebie dla protonów w elastycznych cząsteczkach) są zwykle zbyt małe spowodować zauważalne podziały. cyklicznych i aromatycznych często można zaobserwować sprzężenia dalekiego zasięgu obejmujące więcej niż trzy wiązania , co prowadzi do bardziej złożonych wzorców rozszczepiania. [ potrzebne źródło ]
Na przykład w opisanym powyżej widmie protonowym dla etanolu grupa CH3 jest podzielona na tryplet o stosunku intensywności 1:2:1 przez dwa sąsiednie protony CH2 . Podobnie, CH2 jest dzielony na kwartet o stosunku intensywności 1:3:3:1 przez trzy sąsiednie protony CH3 . W zasadzie dwa protony CH 2 również zostałyby ponownie podzielone na dublet , tworząc dublet kwartetów przez proton hydroksylowy, ale międzycząsteczkowa wymiana kwaśnego protonu hydroksylowego często powoduje utratę informacji o sprzężeniu.
Sprzężenie z dowolnymi jądrami o spinie 1/2, takimi jak fosfor-31 lub fluor-19, działa w ten sposób (chociaż wielkości stałych sprzężenia mogą być bardzo różne). Ale wzory rozszczepienia różnią się od tych opisanych powyżej dla jąder o spinie większym niż ½, ponieważ spinowa liczba kwantowa ma więcej niż dwie możliwe wartości. Na przykład sprzężenie z deuterem (jądro o spinie 1) dzieli sygnał na tryplet 1:1:1, ponieważ spin 1 ma trzy stany spinowe. Podobnie jądro o spinie 3/2, takie jak 35 Cl, dzieli sygnał na kwartet 1:1:1:1 i tak dalej.
Sprzężenie połączone z przesunięciem chemicznym (i całkowaniem dla protonów) mówi nam nie tylko o środowisku chemicznym jąder, ale także o liczbie sąsiednich aktywnych jąder NMR w cząsteczce. W bardziej złożonych widmach z wieloma pikami przy podobnych przesunięciach chemicznych lub w widmach jąder innych niż wodór, sprzężenie jest często jedynym sposobem na rozróżnienie różnych jąder.

Sprzężenie drugiego rzędu (lub silne).
W powyższym opisie założono, że stała sprzężenia jest mała w porównaniu z różnicą częstotliwości NMR pomiędzy nierównoważnymi spinami. Jeśli separacja przesunięć maleje (lub siła sprzężenia wzrasta), wzorce intensywności multipletów są najpierw zniekształcone, a następnie stają się bardziej złożone i trudniejsze do analizy (zwłaszcza jeśli w grę wchodzą więcej niż dwa spiny). Intensyfikacja niektórych pików w multiplecie jest osiągana kosztem reszty, która czasami prawie znika w szumie tła, chociaż scałkowana powierzchnia pod pikami pozostaje stała. Jednak w większości NMR z wysokim polem zniekształcenia są zwykle niewielkie, a charakterystyczne zniekształcenia ( pokrycia dachowe ) mogą w rzeczywistości pomóc w identyfikacji powiązanych szczytów.
Niektóre z tych wzorców można analizować za pomocą metody opublikowanej przez Johna Pople'a , chociaż ma ona ograniczony zakres.
Efekty drugiego rzędu zmniejszają się wraz ze wzrostem różnicy częstotliwości między multipletami, tak że widma NMR o wysokim polu (tj. o wysokiej częstotliwości) wykazują mniejsze zniekształcenia niż widma o niższej częstotliwości. Wczesne widma przy 60 MHz były bardziej podatne na zniekształcenia niż widma z późniejszych maszyn, zwykle pracujących na częstotliwościach 200 MHz lub wyższych.
Ponadto, jak na rysunku po prawej stronie, sprzężenie J może być użyte do identyfikacji podstawienia orto-meta-para pierścienia. Sprzężenie orto jest najsilniejsze przy 15 Hz, następnie Meta ze średnią 2 Hz, a ostatecznie sprzężenie para jest zwykle nieistotne dla badań.
Nierówność magnetyczna
Bardziej subtelne efekty mogą wystąpić, jeśli chemicznie równoważne spiny (tj. jądra powiązane symetrią, a więc mające tę samą częstotliwość NMR) mają różne zależności sprzężenia ze spinami zewnętrznymi. Spiny, które są chemicznie równoważne, ale nie są nie do odróżnienia (na podstawie ich relacji sprzężenia), nazywane są magnetycznie nierównoważnymi. Na przykład miejsca 4H 1,2-dichlorobenzenu dzielą się na dwie chemicznie równoważne pary przez symetrię, ale pojedynczy członek jednej z par ma różne sprzężenia ze spinami tworzącymi drugą parę. Nierównoważność magnetyczna może prowadzić do bardzo złożonych widm, które można analizować jedynie za pomocą modelowania komputerowego. Takie efekty są bardziej powszechne w widmach NMR układów aromatycznych i innych nieelastycznych, podczas gdy uśrednianie konformacyjne wiązań CC w elastycznych cząsteczkach ma tendencję do wyrównywania sprzężeń między protonami na sąsiednich atomach węgla, zmniejszając problemy z nierównowagą magnetyczną.
Spektroskopia korelacyjna
Spektroskopia korelacyjna jest jednym z kilku rodzajów dwuwymiarowej spektroskopii magnetycznego rezonansu jądrowego (NMR) lub 2D-NMR . Ten typ eksperymentu NMR jest najlepiej znany pod akronimem COSY . Inne rodzaje dwuwymiarowego NMR obejmują spektroskopię J, spektroskopię wymiany (EXSY), spektroskopię jądrowego efektu Overhausera (NOESY), spektroskopię całkowitej korelacji (TOCSY) i eksperymenty korelacji heterojądrowej, takie jak HSQC , HMQC i HMBC . W spektroskopii korelacyjnej emisja koncentruje się na piku pojedynczego jądra; jeśli jego pole magnetyczne jest skorelowane z innym jądrem przez wiązanie bezpośrednie (COSY, HSQC itp.) lub przez przestrzeń (NOE), odpowiedź można również wykryć na częstotliwości skorelowanego jądra. Dwuwymiarowe widma NMR dostarczają więcej informacji o cząsteczce niż jednowymiarowe widma NMR i są szczególnie przydatne do określania struktury cząsteczki , szczególnie w przypadku cząsteczek, które są zbyt skomplikowane, aby pracować z nimi przy użyciu jednowymiarowego NMR. Pierwszy dwuwymiarowy eksperyment, COSY, został zaproponowany przez Jeana Jeenera, profesora Université Libre de Bruxelles, w 1971 roku. Eksperyment ten został później przeprowadzony przez Waltera P. Aue, Enrico Bartholdiego i Richarda R. Ernsta, którzy opublikowali swoją pracę w 1976.
Jądrowy rezonans magnetyczny ciała stałego
Różnorodne okoliczności fizyczne nie pozwalają na badanie cząsteczek w roztworze, a jednocześnie innymi technikami spektroskopowymi na poziomie atomowym. W ośrodkach fazy stałej, takich jak kryształy, proszki mikrokrystaliczne, żele, roztwory anizotropowe itp., w szczególności sprzężenie dipolarne i anizotropia przesunięcia chemicznego stają się dominujące w zachowaniu jądrowych systemów spinowych. W konwencjonalnej spektroskopii NMR w roztworze te dodatkowe interakcje doprowadziłyby do znacznego poszerzenia linii widmowych. Różnorodność technik pozwala na ustalenie warunków o wysokiej rozdzielczości, które mogą, przynajmniej przez 13 Widma C, być porównywalne z widmami NMR w stanie roztworu.
Dwie ważne koncepcje dotyczące spektroskopii NMR w stanie stałym o wysokiej rozdzielczości to ograniczenie możliwej orientacji molekularnej przez orientację próbki oraz redukcja anizotropowych jądrowych oddziaływań magnetycznych przez wirowanie próbki. W przypadku tego drugiego podejścia, szybkie wirowanie wokół magicznego kąta jest bardzo wyróżniającą się metodą, gdy układ zawiera jądra o spinie 1/2. Prędkości wirowania ok. 20 kHz, co wymaga specjalnego wyposażenia. W spektroskopii NMR stosuje się obecnie szereg technik pośrednich, z próbkami o częściowym wyrównaniu lub ograniczonej ruchliwości.
Zastosowania, w których występują efekty NMR w stanie stałym, są często związane z badaniami struktury białek błonowych, włókienek białkowych lub wszelkiego rodzaju polimerów oraz analizą chemiczną w chemii nieorganicznej, ale obejmują również zastosowania „egzotyczne”, takie jak liście roślin i ogniwa paliwowe. Na przykład Rahmani i in. badali wpływ ciśnienia i temperatury na samoorganizację struktur dwucelarnych za pomocą spektroskopii NMR deuteru.
Spektroskopia biomolekularnego NMR
Białka
Wiele innowacji w spektroskopii NMR dotyczyło spektroskopii białek NMR , ważnej techniki w biologii strukturalnej . Wspólnym celem tych badań jest uzyskanie trójwymiarowych struktur białka o wysokiej rozdzielczości, podobnych do tego, co można osiągnąć za pomocą krystalografii rentgenowskiej . W przeciwieństwie do krystalografii rentgenowskiej, spektroskopia NMR jest zwykle ograniczona do białek mniejszych niż 35 kDa , chociaż rozwiązano większe struktury. Spektroskopia NMR jest często jedynym sposobem na częściowe lub całkowite uzyskanie informacji o wysokiej rozdzielczości białka samoistnie nieustrukturyzowane . Jest to obecnie powszechne narzędzie do określania zależności aktywności konformacyjnej , w którym struktura przed i po interakcji, na przykład z kandydatem na lek, jest porównywana ze znaną aktywnością biochemiczną. Białka to rzędy wielkości większe niż małe cząsteczki organiczne omówione wcześniej w tym artykule, ale zastosowanie mają również podstawowe techniki NMR i niektóre teorie NMR. Ze względu na znacznie większą liczbę atomów obecnych w cząsteczce białka w porównaniu z małym związkiem organicznym, podstawowe widma 1D stają się zatłoczone nakładającymi się sygnałami do tego stopnia, że bezpośrednia analiza spektralna staje się nie do utrzymania. Dlatego opracowano eksperymenty wielowymiarowe (2, 3 lub 4D), aby poradzić sobie z tym problemem. 15N , pożądane jest izotopowe znakowanie białka 13C i ponieważ dominujący naturalnie występujący izotop 12 C nie jest aktywny w NMR, a jądrowy moment kwadrupolowy dominującego naturalnie występującego izotopu 14 N uniemożliwia uzyskanie informacji o wysokiej rozdzielczości z tego izotopu azotu. Najważniejsza metoda stosowana do określania struktury białek wykorzystuje eksperymenty NOE do pomiaru odległości między atomami w cząsteczce. Następnie uzyskane odległości są wykorzystywane do generowania trójwymiarowej struktury cząsteczki poprzez rozwiązanie geometrii odległości problem. NMR można również wykorzystać do uzyskania informacji o dynamice i elastyczności konformacyjnej różnych regionów białka.
Kwasy nukleinowe
Kwas nukleinowy NMR to wykorzystanie spektroskopii NMR do uzyskania informacji o strukturze i dynamice kwasów polinukleinowych , takich jak DNA czy RNA . Od 2003 roku prawie połowa wszystkich znanych struktur RNA została określona za pomocą spektroskopii NMR.
Spektroskopia NMR kwasów nukleinowych i białek jest podobna, ale istnieją różnice. Kwasy nukleinowe mają mniejszy procent atomów wodoru, które są atomami zwykle obserwowanymi w spektroskopii NMR, a ponieważ podwójne helisy kwasów nukleinowych są sztywne i z grubsza liniowe, nie składają się z powrotem na siebie, dając korelacje „dalekiego zasięgu”. Typy NMR zwykle przeprowadzane z kwasami nukleinowymi to 1H lub protonowy NMR , 13C NMR , 15N NMR i 31P NMR . Dwuwymiarowy NMR metody są prawie zawsze stosowane, takie jak spektroskopia korelacyjna (COSY) i spektroskopia z przeniesieniem całkowitej koherencji (TOCSY) do wykrywania sprzężeń jądrowych poprzez wiązanie oraz jądrowa spektroskopia z efektem Overhausera (NOESY) do wykrywania sprzężeń między jądrami, które są blisko siebie w przestrzeni .
Parametry wzięte z widma, głównie piki krzyżowe NOESY i stałe sprzężenia , mogą być wykorzystane do określenia lokalnych cech strukturalnych, takich jak kąty wiązań glikozydowych , kąty dwuścienne (przy użyciu równania Karplusa ) i konformacje puckera cukru. W przypadku struktury na dużą skalę te lokalne parametry muszą być uzupełnione innymi założeniami lub modelami strukturalnymi, ponieważ błędy sumują się podczas przechodzenia przez podwójną helisę, a w przeciwieństwie do białek, podwójna helisa nie ma zwartego wnętrza i nie zawija się z powrotem samo. NMR jest również przydatny do badania niestandardowych geometrii, takich jak wygięte helisy , parowanie zasad inne niż Watson-Crick i współosiowe układanie w stosy . Było to szczególnie przydatne w badaniu struktury naturalnych oligonukleotydów RNA, które mają tendencję do przyjmowania złożonych konformacji, takich jak pętelki i pseudowęzły . NMR jest również przydatny do sondowania wiązania cząsteczek kwasu nukleinowego z innymi cząsteczkami, takimi jak białka lub leki, poprzez obserwację, które rezonanse są przesunięte po związaniu drugiej cząsteczki.
Węglowodany
NMR węglowodanów odpowiada na pytania dotyczące struktury i konformacji węglowodanów . Analiza węglowodanów za pomocą 1H NMR jest trudna ze względu na ograniczoną zmienność grup funkcyjnych, co prowadzi do rezonansów 1H skoncentrowanych w wąskich pasmach widma NMR. Innymi słowy, występuje słaba dyspersja widmowa. Rezonanse protonów anomerycznych są oddzielone od pozostałych, ponieważ anomeryczne atomy węgla zawierają dwa atomy tlenu. W przypadku mniejszych węglowodanów dyspersja anomerycznych rezonansów protonów ułatwia wykorzystanie eksperymentów 1D TOCSY do badania całych systemów spinowych poszczególnych reszt węglowodanowych.
Odkrycie narkotyków
Znajomość minimów energii i rotacyjnych barier energetycznych małych cząsteczek w roztworze można znaleźć za pomocą NMR, np. patrząc odpowiednio na preferencje konformacyjne wolnych ligandów i dynamikę konformacyjną. Można to wykorzystać do kierowania hipotezami dotyczącymi projektowania leków, ponieważ wartości eksperymentalne i obliczone są porównywalne. Na przykład AstraZeneca wykorzystuje NMR w swoich badaniach i rozwoju w dziedzinie onkologii.
Zobacz też
- NMR pola ziemskiego
- Spektroskopia rezonansu magnetycznego in vivo
- Funkcjonalna spektroskopia rezonansu magnetycznego mózgu
- Niskie pole NMR
- Obrazowanie metodą rezonansu magnetycznego
- Krystalografia NMR
- Baza danych widm NMR
- Spektroskopia NMR stereoizomerów
- Jądrowy rezonans kwadrupolowy
- Pulsujący magnes polowy
- Spektroskopia jądrowa wzmocniona protonami
- Spektroskopia magnetycznego rezonansu jądrowego z potrójnym rezonansem
- NMR pola zerowego
- Odsprzęganie jądrowego rezonansu magnetycznego
Powiązane metody spektroskopii jądrowej :
Dalsza lektura
- Johna D. Robertsa (1959). Jądrowy rezonans magnetyczny: zastosowania w chemii organicznej . Firma Book McGraw-Hill. ISBN 9781258811662 .
- JApopulacja ; WGSchneider ; HJBernstein (1959). Jądrowy rezonans magnetyczny o wysokiej rozdzielczości . Firma Book McGraw-Hill.
- A. Abragam (1961). Zasady magnetyzmu jądrowego . Prasa Clarendona. ISBN 9780198520146 .
- Charles P. Slichter (1963). Zasady rezonansu magnetycznego: z przykładami z fizyki ciała stałego . Harper & Row. ISBN 9783540084761 .
- Johna Emsleya ; Jamesa Feeneya; Leslie Howard Sutcliffe (1965). Spektroskopia magnetycznego rezonansu jądrowego o wysokiej rozdzielczości . Pergamon. ISBN 9781483184081 .
Linki zewnętrzne
- Jamesa Keelera. „Zrozumienie spektroskopii NMR” (przedruk na Uniwersytecie w Cambridge ) . Uniwersytet Kalifornijski, Irvine . Źródło 2007-05-11 .
- Podstawy NMR - nietechniczny przegląd teorii, sprzętu i technik NMR autorstwa dr Josepha Hornaka, profesora chemii w RIT
- Biblioteki GAMMA i PyGAMMA — GAMMA to otwarta biblioteka C++ napisana do symulacji eksperymentów spektroskopii magnetycznego rezonansu jądrowego. PyGAMMA to opakowanie Pythona wokół GAMMA.
- relax Oprogramowanie do analizy dynamiki NMR
- Vespa - VeSPA (Versatile Simulation, Pulses and Analysis) to bezpłatny pakiet oprogramowania składający się z trzech aplikacji w języku Python. Te narzędzia oparte na graficznym interfejsie użytkownika służą do symulacji spektralnej rezonansu magnetycznego (MR), projektowania impulsów RF oraz przetwarzania widmowego i analizy danych MR.


