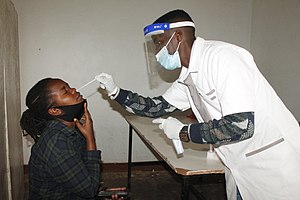
Szybki test na antygen COVID-19
| Szybki test antygenowy COVID-19 Wyniki | |
|---|---|
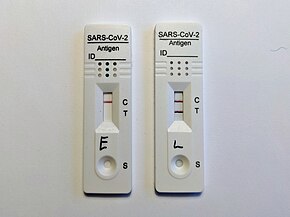 ujemne (po lewej widać linię kontrolną) i pozytywne (po prawej widać linie kontrolną i testową)
| |
| Synonimy | test antygenu SARS-CoV-2 lub COVID-19, szybki test wykrywania antygenu (RADT), test bocznego przepływu (LFT), urządzenie z przepływem bocznym (LFD), szybki test diagnostyczny do wykrywania antygenu (Ag-RDT), szybki test diagnostyczny antygenu (Antygen-RDT), test w punkcie opieki (POC), szybki test |
| Zamiar | Do diagnozowania infekcji SARS-CoV-2 ( COVID-19 ) |
| LOINC | 94558-4 , 95209-3 , 96119-3 , 97097-0 |
Szybkie testy antygenowe COVID-19 lub RAT , często nazywane również testami przepływu bocznego COVID-19 lub LFT , to szybkie testy antygenowe stosowane do wykrywania zakażenia SARS-CoV-2 ( COVID-19 ). Można je szybko wdrożyć przy minimalnym szkoleniu, kosztują ułamek innych form testów na COVID-19 i dają użytkownikom wynik w ciągu 5–30 minut. RAT były stosowane w kilku krajach w ramach masowych testów lub badań przesiewowych obejmujących całą populację. Wiele RAT można wykorzystać do autotestu, w którym osoba „zbiera własną próbkę… i samodzielnie interpretuje wyniki testu”.
Fałszywe alarmy są bardzo rzadkie; specyficzność testów wynosi 98%-99%. Jednak testy mają czułość 70%-72%, czyli mniej niż czułość reakcji łańcuchowej polimerazy (PCR) COVID-19 wynosząca 88%-96%. Mimo to COVID-19 RAT pozostaje cenny w wyszukiwaniu osób, które w przeciwnym razie nie wiedziałyby, że są zarażone, pomagając zapobiegać dalszemu przenoszeniu. Testy są bardziej czułe w objawowych i transmisyjnych stadiach choroby, gdy miano wirusa jest wyższe.
Używa
Zastosowanie w diagnostyce
Szybkie testy antygenowe COVID-19 (RAT) są szeroko stosowane do diagnozowania COVID-19. Definicja przypadku COVID-19 Światowej Organizacji Zdrowia (WHO) stanowi, że osobę z dodatnim wynikiem RAT (znanym również jako szybki test diagnostyczny antygenu lub antygen-RDT) można uznać za „potwierdzony przypadek zakażenia SARS-CoV-2” w dwie drogi. Po pierwsze, osoba z dodatnim antygenem-RDT może spełniać „prawdopodobną definicję przypadku”, taką jak niedawna utrata węchu lub smaku bez żadnej znanej przyczyny, lub może spełniać pewne „kryteria podejrzanego”, takie jak ciężka ostra choroba układu oddechowego. Po drugie, osoba z dodatnim antygenem-RDT może być bezobjawowa, ale „kontakt z prawdopodobnym lub potwierdzonym przypadkiem”. Niemniej jednak poszczególne kraje mogą mieć różne definicje przypadków COVID-19; na przykład w Nowej Zelandii pozytywny test PCR (nie tylko RAT) jest konieczny, aby dana osoba została uznana za „przypadek potwierdzony”.
Użyj w badaniach przesiewowych
Między połową 2020 r. a początkiem 2021 r. w badaniach z wykorzystaniem modeli matematycznych oszacowano korzyści wynikające z częstych RAT w badaniach przesiewowych populacji pod kątem COVID-19. Paltiel i wsp. przebadali hipotetyczny kampus uniwersytecki z 5000 studentami. Badanie przesiewowe wszystkich uczniów co dwa dni za pomocą „testu o niskiej czułości i wysokiej specyficzności” (takiego jak RAT) pozwoliłoby kontrolować wybuch COVID-19. Mina i wsp. wysunęli teorię, że badania przesiewowe o wyższej częstotliwości przy użyciu RAT o niższej czułości mogą być bardziej przydatne niż badania przesiewowe o niższej częstotliwości przy użyciu testów PCR o wyższej czułości, ponieważ te pierwsze „wychwytują większość infekcji, gdy są one nadal zakaźne”. Szybkie wyniki RAT posłużyłyby do ograniczenia bezobjawowego rozprzestrzeniania się. Larremore i wsp. symulowali różne strategie badań przesiewowych populacji COVID-19. Naukowcy odkryli, że „skuteczne badania przesiewowe zależą w dużej mierze od częstotliwości testów i szybkości raportowania, a wysoka czułość testu poprawia je tylko nieznacznie”.
Zastosowania humanitarne
Oprócz rutynowego użytku w społeczności, szybkie testy były również wykorzystywane w ramach działań humanitarnych podczas pandemii. Po powodzi w Dżakarcie w Indonezji 2 grudnia 2020 r. w schronach przeciwpowodziowych udostępniono szybkie testy. Co więcej, po zamknięciu granic państwowych w Europie w następstwie pojawienia się wariantu Alpha tuż przed Bożym Narodzeniem 2020 r., prawie 6000 kierowców ciężarówek utknęło bez jedzenia, skutecznie wstrzymując świąteczne dostawy żywności. Szybkie testy zostały wdrożone przez francuskich strażaków w ciągu 24 godzin nad kanałem La Manche. Szybkie testy umożliwiły ciężarówkom wyruszenie w drogę, sfinalizowanie dostaw i powrót do rodzin na Boże Narodzenie, demonstrując potencjalną globalną użyteczność posiadania łatwego do wdrożenia testu na COVID-19. Organizacja Médecins Sans Frontières zdecydowanie poparła stosowanie szybkich testów w krajach o niższych i średnich dochodach, zauważając, że „testy na antygen COVID-19 mogą dostarczyć szybkich i przydatnych wyników, zapewniając szybką identyfikację osób zakażonych wirusem na poziomie społeczności”.
Użyj do „powrotu do normalności”
Barcelonie odbył się bezpłatny koncert muzyczny dla osób, które przystąpiły do szybkiego testu. Podobne podejście przyjęto w Albanii , aby umożliwić festiwale muzyczne. Jednak wielu ekspertów nie było przekonanych co do tego podejścia, wierząc, że „szybkie testy nie są rozwiązaniem umożliwiającym powrót do normalnego życia”, ale można je stosować w połączeniu z innymi technikami kontroli infekcji.
Obawy dotyczące użytkowania
Fałszywe negatywy (niska czułość)
Chociaż specyficzność RAT jest wysoka (98% -99%), w 2020 r. RAT były krytykowane za czułość zaledwie 50%; to znaczy, gdyby osoby z COVID-19, jak określono na podstawie pozytywnego testu PCR, były również testowane za pomocą RAT, mniej więcej w połowie przypadków RAT byłby ujemny. Od 2022 r. Przeglądy systematyczne wykazały, że łączna wrażliwość RAT wynosiła 70–72%. W jednym przeglądzie systematycznym zakres czułości w badaniach wynosił 37–90%. Ponieważ WHO zaleca RAT o „czułości ≥ 80%”, wiele RAT nie spełnia zaleceń WHO.
W przeglądach systematycznych czułość była wyższa dla osób z objawami (76%-82%) niż dla osób bezobjawowych (57%-68%). Szczury były bardziej czułe, gdy próbki miały większe miano wirusa, jak zmierzono za pomocą niskiego „progu cyklu” PCR, i mniej czułe, gdy próbki miały mniejsze miano wirusa.
W badaniu z 2022 r. obserwowano 225 dorosłych i dzieci z COVID-19 przez 15 dni przy użyciu testów PCR, kultur wirusowych i domowych RAT. Stwierdzono, że czułość testu RAT (Quidel QuickVue) wzrosła z 0% dwa dni przed wystąpieniem objawów lub pierwszym dodatnim wynikiem testu PCR do 77% cztery dni po wystąpieniu objawów lub pierwszym pozytywnym wynikiem testu PCR, przy ogólnej czułości 50%. W porównaniu z testami PCR pobranymi tego samego dnia, czułość RAT wyniosła 64%; w porównaniu z kulturami wirusowymi zebranymi tego samego dnia, czułość RAT wyniosła 84%. Czułość testu RAT była niższa u osób zaszczepionych przeciwko COVID-19 niż u osób nieszczepionych przeciwko COVID-19.
Możliwość uzyskania wyników fałszywie ujemnych z powodu nowych wariantów
W listopadzie 2020 r. w Wielkiej Brytanii zidentyfikowano nowy, nieznacznie bardziej zakaźny szczep SARS-CoV-2, wariant SARS-CoV-2 Alpha . Szczep szybko rozprzestrzenił się na całym świecie. Przy powszechnym globalnym stosowaniu tej formy testów na COVID-19 istniała obawa, że ten wariant sprawi, że szybkie testy staną się przestarzałe. W ramach przyspieszonej oceny technologii przepływu bocznego w Wielkiej Brytanii, w ciągu 24 godzin Public Health England były w stanie potwierdzić, że RAT w globalnym rozwoju nie zostały naruszone (tj. że mogły zidentyfikować nowy wariant). Stało się tak dlatego, że szybki test na ogół celuje w kapsydu , a nie w białko szczytowe . Niektóre szczepy zostały zidentyfikowane z mutacją nukleokapsydu (D399N), która zmniejsza czułość co najmniej jednego RAT (Quidel Sofia 2) nawet 1000-krotnie. Na szczęście częstość mutacji D399N była nadal stosunkowo niska na całym świecie i wynosiła ~ 0,02% w maju 2021 r. Badanie opublikowane w 2022 r. Wykazało, że czułość sześciu szybkich testów wykrywania antygenu wynosiła 70,0% -92,9% dla wariantu Delta i 69,6 % - 78,3% dla wariantu Omicron w całym zakresie miana wirusa ; jednakże dla próbek Omicron o niskim mianie wirusa czułość wynosiła 0,0%-23,1%.
Fałszywie pozytywne wyniki, gdy instrukcje nie są przestrzegane
Jeśli COVID-19 RAT zostanie użyty poza zaleceniami producenta, wynik może być fałszywie dodatni . Począwszy od grudnia 2020 r., TikTok pokazywały, jak używać napojów bezalkoholowych do tworzenia fałszywie dodatnich wyników RAT COVID-19. Później naukowcy odkryli, że wprowadzenie soków owocowych, napojów alkoholowych, wody butelkowanej i innych produktów bezpośrednio do Abbott Panbio COVID-19 RAT bez zalecanego przez producenta roztworu buforowego dawało fałszywe alarmy. Natomiast inny RAT (BD Veritor) nie dał wyników fałszywie dodatnich w tych samych warunkach.
Powolne wdrażanie i absorpcja
Niektórzy wyrazili zaniepokojenie powolnym wdrażaniem i przyjmowaniem RAT oraz potencjalną utratą życia, która mogła w rezultacie nastąpić. Badanie modelowe przeprowadzone w Kanadzie oszacowało, że połowie zgonów w domach opieki w Kolumbii Brytyjskiej w 2020 r. można by zapobiec, gdyby dostępne były szybkie testy.
Metody
Antygen to obca cząsteczka lub struktura molekularna , która może wywołać odpowiedź immunologiczną . Szybkie testy antygenowe COVID-19 (RAT) wykrywają białka antygenowe na powierzchni koronawirusa SARS-CoV- 2 . Spośród szczurów COVID-19, które do stycznia 2022 r. otrzymały zezwolenie na użycie w nagłych wypadkach (EUA) od Amerykańskiej Agencji ds. Żywności i Leków (FDA), wszystkie wykryły białka nukleokapsydu , a jeden wykrył również domenę wiążącą receptor białka szczytowego koronawirusa . Podobnie, prawie wszystkie testy na wspólnej liście Unii Europejskiej COVID-19 RAT są ukierunkowane na białka nukleokapsydu.
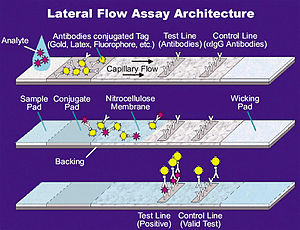
Typowy COVID-19 RAT to test przepływu bocznego (LFT). W przypadku LFT próbkę cieczy (np. z wymazu z nosa) umieszcza się na podkładce na jednym końcu porowatego, przypominającego papier paska. Ciecz przechodzi na drugi koniec papieru poprzez zasysanie ( działanie kapilarne ). Na „poduszce koniugatu” przeciwciała z nanocząstkami złota przyłączają się do wszelkich antygenów SARS-CoV-2 obecnych w próbce. Na linii testowej (która może być oznaczona jako „T”) obecne są przeciwciała swoiste dla SARS-CoV-2. W linii kontrolnej (która może być oznaczona jako „C”) obecne są przeciwciała, które mogą przyłączać się do przeciwciał z nanocząstkami. Jeśli widoczna jest tylko linia kontrolna, test jest negatywny; jeśli widoczne są zarówno linie kontrolne, jak i testowe, test jest pozytywny.
Historia rozwoju i wdrażania
2020
W maju 2020 r. amerykańska Agencja ds. Żywności i Leków (FDA) wydała pierwsze zezwolenie na użycie w sytuacjach awaryjnych (EUA) dla COVID-19 RAT, testu Sofia 2 wyprodukowanego przez firmę Quidel .
W sierpniu 2020 roku Departament Zdrowia i Opieki Społecznej Stanów Zjednoczonych ogłosił, że rząd USA kupi 150 milionów RAT BinaxNOW wyprodukowanych przez Abbott Laboratories „w celu rozszerzenia strategicznych testów opartych na dowodach”. Później agencja ogłosiła, że 100 milionów testów ma zostać wysłanych do gubernatorów do wykorzystania „według własnego uznania”, na przykład do ponownego otwarcia szkół.
Do września 2020 roku ogłoszono, że program Moonshot w Wielkiej Brytanii zainwestuje 100 miliardów funtów w systematyczną ocenę, rozwój i wdrażanie nowych technologii do testowania COVID-19, w tym RAT na COVID-19. W tym miesiącu Światowa Organizacja Zdrowia (WHO) opublikowała tymczasowe wytyczne dotyczące „szybkich testów diagnostycznych wykrywających antygen” (Ag-RDT) COVID-19, w tym zalecenia dotyczące ich stosowania, wyboru i wdrażania. W tymczasowych wytycznych zauważono, że Ag-RDT były łatwiejsze do wdrożenia i tańsze niż testy amplifikacji kwasów nukleinowych (NAAT). WHO zaleciła stosowanie Ag-RDT w ogniskach, w monitorowaniu trendów chorobowych oraz we wczesnej identyfikacji przypadków.
Health Canada zatwierdziła swój pierwszy COVID-19 RAT w październiku 2020 r., test Abbott Panbio. Od października 2020 r. W Stanach Zjednoczonych pojawiały się pytania, czy moce produkcyjne nadążą za potencjalnym popytem na setki milionów RAT. RAT zaczęto wdrażać w portugalskich szkołach i domach opieki.
Jedno z wczesnych dużych badań nad urządzeniami przepływu bocznego (LFD) COVID-19 zostało zakończone przez Public Health England i University of Oxford , a wstępny raport został opublikowany w listopadzie 2020 r. Naukowcy przeprowadzili ocenę 64 LFD, która przebiegała w kilku fazach. Spośród czterech LFD o „pożądanych parametrach użytkowych”, jeden (Innova) miał czułość 78,8% i odsetek wyników fałszywie dodatnich 0,32%.
2 listopada 2020 r. Słowacja jako pierwszy kraj na świecie zainicjowała ogólnokrajowe masowe testy przy użyciu szybkich testów. Pięć milionów szybkich testów zostało wykonanych przez 60 000 pracowników, którzy używali testu antygenowego SD Biosensor i pobierali wymazy z populacji. Na początku 2021 r. opublikowano dwa badania naukowe na temat doświadczeń Słowacji, jedno autorstwa profesora Martina Kahanca z Central European University i jego współautorów, a drugie autorstwa Martina Pavelki z London School of Hygiene & Tropical Medicine i jego zespołu. Oba badania sugerowały, że szybkie masowe testy antygenowe pomogły stłumić pandemię w kraju, chociaż według poprzedniego badania wpływ masowych testów na pandemię był tymczasowy i zaczął ustępować po około dwóch tygodniach.
Wielka Brytania kontynuowała trwający program rozwoju szybkich testów, korzystając z szybkiego testu Innova, z rosnącą pilnością w miarę wzrostu liczby przypadków COVID-19 w Europie. 6 listopada 2020 r. premier Boris Johnson rozpoczął ogólnomiejskie badanie Liverpoolu w ramach przyspieszonej oceny technologii. Rozpoczęto również dalsze rozszerzanie programów pilotażowych szybkich testów dla wielu sektorów, w których testowanie nie było wcześniej dostępne. Wśród nich byli studenci uniwersytetów, którzy zostali szczególnie dotknięci epidemiami. Początkowo zaczęło się to na Uniwersytecie w Durham , który miał infrastrukturę i wiedzę specjalistyczną do zarządzania programem szybkich testów, ale został rozszerzony na większość uniwersytetów w Wielkiej Brytanii i umożliwił krajowy plan ewakuacji, aby bezpiecznie sprowadzić uczniów do domu na Boże Narodzenie. Szybkie testy zostały również wdrożone w ramach Narodowej Służby Zdrowia (NHS) dla personelu, aby ograniczyć możliwą transmisję do pacjentów, władz lokalnych i domów opieki, aby umożliwić odwiedzanie mieszkańców. 18 listopada 2020 r. Walia zakończyła pierwsze testy całej gminy w Merthyr Tydfil .
Globalne wysiłki na rzecz zintensyfikowania ocen szybkich testów zostały zainicjowane przez Departament ds. Sytuacji Nadzwyczajnych Światowej Organizacji Zdrowia (WHO), który 10 listopada 2020 r. rozpoczął duży projekt wdrożenia szybkich testów diagnostycznych, wspomagany zgodą Fundacji Billa i Melindy Gatesów , która ograniczyła koszty dla krajów o niskich i średnich dochodach.
Austria rozpoczęła masowe testy w całym kraju 5 grudnia 2020 r. I zamówiła siedem milionów testów składających się z testu SD Biosensor i Siemens Clinitest (aka Orientgene).
Do połowy grudnia 2020 r. przeprowadzono wiele badań potwierdzających skuteczność i powodzenie stosowania szybkich testów do identyfikacji osób z COVID-19, w tym badania w Holandii, Wielkiej Brytanii i USA. Wszystkie te badania umożliwiły wprowadzenie szybkich testów do standardowych krajowych strategii testowania COVID-19. Globalny pilotaż szybkich testów był teraz powszechny w szkołach w Kanadzie, w centrach podróży w Indonezji i w całych Indiach.
W Stanach Zjednoczonych w grudniu 2020 r. profesor Michael Mina z Uniwersytetu Harvarda zauważył, że testy domowe były „bardzo potężnym dodatkiem do wszystkiego, co ludzie już robią”. Pogląd ten został wzmocniony przez profesora Williama A. Haseltine'a , również z Harvardu, w artykule w czasopiśmie Forbes, w którym stwierdził, że „szybkie, samodzielne testy mogą powstrzymać stale rosnącą falę chorób i śmierci”. Jednak dalsze wdrażanie szybkich testów w ramach podejść do masowych testów w USA utknęło w martwym punkcie w wyniku impasu wokół 900 miliardów dolarów pomocy związanej z COVID-19, zawartej w ustawie o skonsolidowanych środkach z 2021 r . Projekt ustawy został skrytykowany za to, że nie wspierał w szczególności szybkich autotestów COVID. W międzyczasie FDA zatwierdziła Abbott BinaxNOW RAT „do użytku domowego na receptę”. Ellume wydało późniejszą zgodę na pierwszy domowy RAT na COVID-19 dostępny bez recepty.
W Wielkiej Brytanii w grudniu 2020 r. Agencja Regulacyjna ds. Leków i Produktów Opieki Zdrowotnej zatwierdziła szybki test Innova do samodzielnego badania osób bezobjawowych. Główny lekarz kliniczny Wielkiej Brytanii, dr Susan Hopkins , zauważyła, że szybkie testy umożliwiają znalezienie „ludzi, których… nie moglibyśmy znaleźć w inny sposób”.
Odnotowując możliwość szybszego identyfikowania przypadków i biorąc pod uwagę wynikającą z tego eskalację przypadków w Europie, Komisja Europejska (KE) spotkała się w grudniu 2020 r. i opracowała wspólne europejskie ramy „stosowania, walidacji i wzajemnego uznawania szybkich testów”, zobowiązując się do 100 mln euro na zakup testów od firm Roche i Abbott . Stella Kyriakides , komisarz ds. zdrowia i bezpieczeństwa żywności, powiedziała: „Szybkie testy antygenowe zapewniają nam szybkość, niezawodność i szybką reakcję na izolowanie przypadków COVID. Ma to kluczowe znaczenie dla spowolnienia rozprzestrzeniania się pandemii”.
2021
Do stycznia 2021 r. Rada Unii Europejskiej opowiedziała się za częstszym stosowaniem szybkich testów, zwracając uwagę, że „jeśli badania wykażą, że szybkie testy antygenowe mogą być przeprowadzane przez samą osobę badaną… można by również rozważyć samobadanie z profesjonalnymi wskazówkami lub bez nich ”. W Stanach Zjednoczonych nowo zainaugurowany prezydent USA Joe Biden opublikował krajową strategię dotyczącą COVID-19, która zobowiązała się do „finansowania pozyskiwania i dystrybucji szybkich testów dla populacji priorytetowych, pracy na rzecz pobudzenia rozwoju i produkcji testów w domu oraz pracy w celu zapewnienia, że testy są powszechnie dostępne." W marcu 2021 roku amerykańska FDA dopuściła Abbott BinaxNOW RAT i Quidel QuickVue RAT do użytku domowego bez recepty.
firma Innova dobrowolnie rozpoczęła w Stanach Zjednoczonych wycofanie ponad 77 000 swoich RAT klasy I. Dwa miesiące później FDA ostrzegła Amerykanów, aby przestali używać tego testu, ponieważ miał „poważne obawy, że wykonanie testu nie zostało odpowiednio przyjęty." Tydzień po ostrzeżeniu FDA o teście Innova brytyjska Agencja Regulacyjna ds. Leków i Produktów Opieki Zdrowotnej (MHRA) zezwoliła na stosowanie szybkiej diagnostyki i przedłużyła jej autoryzację.
W październiku 2021 r. WHO zaktualizowała swoje tymczasowe wytyczne dotyczące Ag-RDT. Wśród innych zmian tymczasowe wytyczne WHO z 2021 r. zawierały zaktualizowane informacje na temat wyników testów, wyboru zastosowań i przechowywania. Również w październiku 2021 r. Ellume wycofał ponad 2,2 miliona swoich testów domowych z powodu „wyższych niż akceptowalne fałszywie dodatnich wyników testów na SARS-CoV-2”.
W grudniu 2021 roku prezydent USA Biden ogłosił, że rząd planuje zakup i dystrybucję za darmo 500 milionów domowych RAT COVID-19. W odpowiedzi zacytowano dr Leanę Wen , która powiedziała, że liczba testów „nie zbliża się nawet do tego, co jest potrzebne”.
2022
Prezydent USA Biden zapowiedział w styczniu 2022 r. zakup 500 mln dodatkowych RAT do bezpłatnej dystrybucji. W marcu 2022 r. WHO wydała tymczasowe wytyczne dotyczące samokontroli za pomocą Ag-RDT. WHO wydała stanowcze zalecenie, aby samokontrola COVID-19 Ag-RDT „była oferowana jako dodatek do profesjonalnie administrowanych usług testowych”. Ostrzeżenie amerykańskiej FDA z kwietnia 2022 r. dotyczyło dwóch podrobionych domowych RAT COVID-19.
Aspekty ekonomiczne
Koszty i opłacalność
Pod koniec 2020 roku zauważono, że w USA RAT kosztuje od 5 do 23 USD , w przeciwieństwie do testów PCR, które kosztują co najmniej 75 USD. W duńskim badaniu opublikowanym w 2021 r. RAT kosztuje około 5,70 USD za test, w przeciwieństwie do PCR za 10,80 USD za test. Badanie przeprowadzone w Niemczech w 2021 r. wykazało, że monitorowanie pracowników służby zdrowia narażonych na COVID-19 za pomocą RAT pozwala zaoszczędzić pieniądze w porównaniu z wysyłaniem ich na kwarantannę. Badanie z 2021 r. wykazało, że jeśli Stany Zjednoczone są skłonne zapłacić 100 000 USD za rok uniknięcia utraty życia , to cotygodniowe lub comiesięczne testowanie populacji za pomocą RAT prawdopodobnie będzie opłacalne . W innym badaniu z 2021 r. Oszacowano przyrostowe wskaźniki opłacalności na „7890 USD na unikniętą infekcję i 1 430 000 USD na unikniętą śmierć”, jeśli cotygodniowe badania przesiewowe za pomocą domowych RAT były przeprowadzane w całej populacji USA przez okres 60 dni.
Globalna wartość rynkowa
Szacunki wartości światowego rynku RAT są różne. Według jednego z szacunków wielkość rynku wyniosła 28 miliardów dolarów w 2021 roku, przy złożonej rocznej stopie wzrostu (CAGR) na poziomie -21,7%, co prowadzi do wielkości 14 miliardów dolarów w 2028 roku. Drugie oszacowanie sugerowało, że wartość rynku wyniosła 4,6 miliarda dolarów w 2021 roku, z CAGR na poziomie -26,3%, co prowadzi do wartości 743 mln USD w 2027 r. Trzecie oszacowanie wykazało wartość 5,3 mld USD w 2020 r., która „oczekiwano, że wzrośnie przy zdrowym tempie wzrostu przekraczającym 6,7% w okresie prognozy 2021-2027."
Zobacz też
Notatki
- ^ a b Kahanec M, Lafférs L, Schmidpeter B (2021). „Wpływ powtarzanych masowych testów antygenowych w kierunku COVID-19 na częstość występowania choroby” . J Popul Econ . 34 (4): 1105–1140. doi : 10.1007/s00148-021-00856-z . PMC 8241209 . PMID 34219976 .
- ^ a b c „Zastosowanie szybkich testów diagnostycznych do wykrywania antygenu SARS-CoV-2 do samodzielnego testowania COVID-19. Tymczasowe wytyczne” . Światowa Organizacja Zdrowia. 9 marca 2022 . Źródło 4 lipca 2022 r .
- ^ a b c d e f g h Khalid MF, Selvam K, Jeffry AJ, Salmi MF, Najib MA, Norhayati MN i in. (4 stycznia 2022). „Wydajność szybkich testów antygenowych w diagnostyce COVID-19: przegląd systematyczny i metaanaliza” . Diagnostyka . 12 (1): 110. doi : 10.3390/diagnostics12010110 . PMC 8774565 . PMID 35054277 .
- ^ a b c d e f g Brümmer LE, Katzenschlager S, McGrath S, Schmitz S, Gaeddert M, Erdmann C, et al. (26 maja 2022). „Dokładność szybkiej diagnostyki SARS-CoV-2 opartej na antygenach w punkcie opieki: zaktualizowany systematyczny przegląd i metaanaliza z analizą meta-regresji czynników wpływających” . PLOS Med . 19 (5): e1004011. doi : 10.1371/journal.pmed.1004011 . PMC 9187092 . PMID 35617375 .
- ^ a b c d e f g Tapari A, Braliou GG, Papaefthimiou M, Mavriki H, Kontou PI, Nikolopoulos GK, Bagos PG (4 czerwca 2022). „Wydajność testów wykrywania antygenu dla SARS-CoV-2: przegląd systematyczny i metaanaliza” . Diagnostyka . 12 (6): 1388. doi : 10.3390/diagnostics12061388 . PMC 9221910 . PMID 35741198 .
- ^ Pecoraro V, Negro A, Pirotti T, Trenti T (2022). „Oszacuj wskaźniki fałszywie ujemnych wyników RT-PCR dla SARS-CoV-2. Przegląd systematyczny i metaanaliza” . Eur J Clin Invest . 52 (2): e13706. doi : 10.1111/eci.13706 . PMC 8646643 . PMID 34741305 .
- ^ Pu R, Liu S, Ren X, Shi D, Ba Y, Huo Y i in. (2022). „Wartość przesiewowa RT-LAMP i RT-PCR w diagnostyce COVID-19: przegląd systematyczny i metaanaliza” . J Metody wirusowe . 300 : 114392. doi : 10.1016/j.jviromet.2021.114392 . PMC 8629515 . PMID 34856308 .
- ^ „Oxford University i PHE potwierdzają, że testy przepływu bocznego wykazują wysoką swoistość i są skuteczne w identyfikacji większości osób zakaźnych” . Uniwersytet Oksfordzki . 11 listopada 2020 r.
- ^ Guglielmi G. (2020). „Szybkie testy na koronawirusa: co mogą, a czego nie mogą” . Natura . 585 (7826): 496–498. Bibcode : 2020Natur.585..496G . doi : 10.1038/d41586-020-02661-2 . PMID 32939084 .
- ^ a b c „WHO COVID-19: Definicje przypadków” . Światowa Organizacja Zdrowia. 16 grudnia 2020 . Źródło 8 lipca 2022 r .
- ^ „Definicja przypadku i wytyczne dotyczące badań klinicznych dla COVID-19” . Ministerstwo Zdrowia Nowej Zelandii – Manatū Hauora . 30 czerwca 2022 . Źródło 8 lipca 2022 r .
- ^ a b Paltiel AD, Zheng A, Walensky RP (2020). „Ocena strategii badań przesiewowych SARS-CoV-2 w celu umożliwienia bezpiecznego ponownego otwarcia kampusów uniwersyteckich w Stanach Zjednoczonych” . JAMA Netw Open . 3 (7): e2016818. doi : 10.1001/jamanetworkopen.2020.16818 . PMC 7395236 . PMID 32735339 .
- ^ a b Mina MJ, Parker R, Larremore DB (2020). „Przemyślenie czułości testu Covid-19 – strategia powstrzymywania” . The New England Journal of Medicine . 383 (22): e120. doi : 10.1056/NEJMp2025631 . PMID 32997903 .
- ^ ab Larremore DB, Wilder B, Lester E, Shehata S , Burke JM, Hay JA i in. (2021). „Czułość testu jest drugorzędna w stosunku do częstotliwości i czasu realizacji badań przesiewowych w kierunku COVID-19” . Postępy nauki . 7 (1): eabd5393. Bibcode : 2021SciA....7.5393L . doi : 10.1126/sciadv.abd5393 . PMC 7775777 . PMID 33219112 .
- ^ „Północna Dżakarta zapewni szybkie testy dla ludzi w schronach przeciwpowodziowych” . Poczta Dżakarta . 2 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ „Covid-19: organizacje charytatywne wysyłają żywność unieruchomionym kierowcom ciężarówek” . wiadomości BBC . 23 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ Rawlinson K, Halliday J (24 grudnia 2020). „Armia przejmie testy Covid dla przewoźników uwięzionych w pobliżu Dover” . Strażnik . ISSN 0261-3077 . Źródło 11 lipca 2022 r .
- ^ „COVID-19: Surowy gniew wśród kierowców ciężarówek w Dover, ponieważ testy na koronawirusa nie łagodzą napięć” . Wiadomości z nieba . 24 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ „Diagnostyka COVID-19: MSF z zadowoleniem przyjmuje tańsze szybkie testy dla krajów o niższych i średnich dochodach - Świat” . ReliefWeb . 29 stycznia 2021 . Źródło 11 lipca 2022 r .
- ^ Glenn A (7 grudnia 2020). „Apteki w Hiszpanii wprowadzą szybkie testy na COVID-19” . Euro Weekly News Hiszpania . Źródło 11 lipca 2022 r .
- ^ Dorn S (12 grudnia 2020). „Barcelona organizuje koncert dla 500 mieszkańców w ramach eksperymentu szybkiego testu COVID” . Poczta Nowego Jorku . Źródło 11 lipca 2022 r .
- ^ „Rząd Albanii zatwierdził szybkie testy Covid na Unum Festival 2021” . Magazyn cracka . 2 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ „Szybkie testy nie są rozwiązaniem umożliwiającym wznowienie normalnego życia, mówi ekspert” . Brukselski Times . 22 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ „Badanie przepływu bocznego - nowe szybkie testy do wykrywania COVID-19 - sprawy zdrowia publicznego” . publichealthmatters.blog.gov.uk . 8 grudnia 2020 . Źródło 11 lipca 2022 r .
- ^ Serwis RF (22 maja 2020). „Testy na antygeny koronawirusa: szybkie i tanie, ale zbyt często błędne?” . nauka . Źródło 10 lipca 2022 r .
- ^ Saxena R (17 sierpnia 2020). „Dlaczego szybkie testy antygenowe w Indiach na obecność koronawirusa są jak„ rzut monetą ” ” . Druk . Źródło 10 lipca 2022 r .
- ^ Halliday J, Pidd H (22 grudnia 2020). „Plany 30-minutowych testów Covid w Anglii zostały wstrzymane z powodu obaw o dokładność” . Strażnik . Źródło 10 lipca 2022 r .
- ^ a b c „Wykrywanie antygenu w diagnostyce zakażenia SARS-CoV-2. Tymczasowe wytyczne” . Światowa Organizacja Zdrowia. 6 października 2021 . Źródło 4 lipca 2022 r .
- ^ a b c d Chu VT, Schwartz NG, Donnelly MA, Chuey MR, Soto R, Yousaf AR i in. (2022). „Porównanie domowych testów antygenowych z RT-PCR i kulturą wirusową w przebiegu zakażenia SARS-CoV-2” . JAMA stażysta med . 182 (7): 701–709. doi : 10.1001/jamainternmed.2022.1827 . PMC 9055515. PMID 35486394 .
- ^ „Szybka ocena potwierdza skuteczność urządzeń z przepływem bocznym w wykrywaniu nowego wariantu COVID-19” . GOV.Wielka Brytania . Źródło 4 lipca 2022 r .
- ^ a b Bourassa L, Perchetti GA, Phung Q, Lin MJ, Mills MG, Roychoudhury P i in. (2021). „Wariant nukleokapsydu SARS-CoV-2, który wpływa na wydajność testu na antygen” . J Clin Virol . 141 : 104900. doi : 10.1016/j.jcv.2021.104900 . PMC 8219478 . PMID 34171548 .
- ^ Bayart JL, Degosserie J, Favresse J, Gillot C, Didembourg M, Djokoto HP i in. (2022). „Czułość analityczna sześciu szybkich testów antygenowych SARS-CoV-2 dla wariantu Omicron i Delta” . Wirusy . 14 (4): 654. doi : 10.3390/v14040654 . PMC 9031584 . PMID 35458384 .
- ^ Lorch, Mark (5 lipca 2021). „Jak dzieci fałszują testy Covid-19 za pomocą napojów bezalkoholowych” . BBC . Źródło 3 lipca 2022 r .
-
^ ab ; Patriquin G, Davidson RJ, Hatchette TF, szef BM, Mejia E, Becker MG
i in. (2021). „Generowanie fałszywie dodatnich wyników antygenu SARS-CoV-2 w warunkach testowania poza zaleceniami producenta: naukowe podejście do błędnych informacji o pandemii” . Widmo mikrobiomu . 9 (2): e0068321. doi : 10.1128/Spectrum.00683-21 . PMC 8528119 . PMID 34668722 .
{{ cite journal }}: CS1 maint: wiele nazwisk: lista autorów ( link ) - ^ Wakacje I (29 stycznia 2021). „Szybkie testy mogły zapobiec połowie zgonów w domach opieki BC w 2020 r., sugeruje modelowanie” . CTVWiadomości . Źródło 7 lipca 2022 r .
- ^ a b Odpływ PK (2022). „Szybkie testy diagnostyczne w kierunku SARS-CoV-2” . N angielski J Med . 386 (3): 264–272. doi : 10.1056/NEJMcp2117115 . PMC 8820190 . PMID 34995029 .
- ^ „Wspólna unijna lista szybkich testów antygenowych COVID-19” (PDF) . Komisja Europejska, Dyrekcja Generalna ds. Zdrowia i Bezpieczeństwa Żywności . 10 czerwca 2022 . Źródło 6 lipca 2022 r .
- ^ a b c d e Shirazi S, Stanford CM, Cooper LF (2021). „Badania w kierunku COVID-19 w gabinetach stomatologicznych: mechanizm działania, zastosowanie i interpretacja badań przesiewowych laboratoryjnych i przyłóżkowych” . The Journal of American Dental Association . 152 (7): 514–525.e8. doi : 10.1016/j.adaj.2021.04.019 . ISSN 0002-8177 . PMC 8096195 . PMID 34176567 .
- ^ a b „Jak działają testy bocznego przepływu COVID-19” . rząd walijski. 30 czerwca 2022 . Źródło 6 lipca 2022 r .
- ^ a b Frew E, Roberts D, Barry S, Holden M, Restell Mand A, Mitsock E i in. (2021). „Szybki test diagnostyczny antygenu SARS-CoV-2 dla ustawień o ograniczonych zasobach” . Przedstawiciel nauk ścisłych 11 (1): 23009. Bibcode : 2021NatSR..1123009F . doi : 10.1038/s41598-021-02128-y . PMC 8626481 . PMID 34837001 .
- ^ Hahn SM, Shuren JE (9 maja 2020). „Aktualizacja dotycząca koronawirusa (COVID-19): FDA zezwala na pierwszy test na antygen, który pomoże w szybkim wykryciu wirusa wywołującego COVID-19 u pacjentów” . Administracja Żywności i Leków . Źródło 4 lipca 2022 r .
-
^
„Administracja Trumpa wdroży 150 milionów szybkich testów w 2020 roku” . Departament Zdrowia i Opieki Społecznej Stanów Zjednoczonych. 27 sierpnia 2020 r. Zarchiwizowane od oryginału w dniu 28 sierpnia 2020 r . Źródło 4 lipca 2022 r .
{{ cite web }}: CS1 maint: nieodpowiedni adres URL ( link ) - ^ Blad E (9 października 2020). „Dlaczego szybkie testy na koronawirusa w szkołach mogą nie być„ zmianą gry ”, na którą mają nadzieję niektórzy urzędnicy” . Tydzień Edukacji . Źródło 12 lipca 2022 r .
-
^
Iacobucci G, Coombes R (2020). „Covid-19: rząd planuje wydać 100 miliardów funtów na zwiększenie liczby testów do 10 milionów dziennie” . BMJ . 370 : m3520. doi : 10.1136/bmj.m3520 . PMID 32907851 .
Rzecznik Departamentu Zdrowia i Opieki Społecznej powiedział: „… idziemy dalej, inwestując 500 milionów funtów w testy nowej generacji, takie jak… szybkie testy, które mogą dostarczyć wyniki w zaledwie 20 minut”.
- ^ a b c „Wykrywanie antygenu w diagnostyce zakażenia SARS-CoV-2 za pomocą szybkich testów immunologicznych. Tymczasowe wytyczne” (PDF) . Światowa Organizacja Zdrowia. 11 września 2020 . Źródło 4 lipca 2022 r .
- ^ Tasker JP (6 października 2020). „Health Canada zatwierdza pierwszy szybki test na antygen COVID-19, federalni planują kupić 20 milionów” . Wiadomości CBC . Źródło 4 lipca 2022 r .
- ^ a b Rubin R (2020). „Wyzwania związane z rozszerzeniem szybkich testów w celu ograniczenia COVID-19” . JAMA . 324 (18): 1813–1815. doi : 10.1001/jama.2020.21106 . PMID 33084882 .
- ^ „Ogromne zapotrzebowanie na szybkie testy antygenu COVID-19 może napotkać ograniczenia produkcyjne” . Nowoczesna Opieka Zdrowotna . 8 października 2020 . Źródło 10 lipca 2022 r .
- ^ Donn N (27 października 2020). „Portugalia wprowadza„ szybkie testy ”, aby pomóc powstrzymać epidemie w szkołach i domach OAP” . Mieszkaniec Portugalii . Źródło 12 lipca 2022 r .
- ^ „Oxford University i PHE potwierdzają, że testy przepływu bocznego wykazują wysoką swoistość i są skuteczne w identyfikacji większości osób zakaźnych” . Uniwersytet Oksfordzki. 11 listopada 2020 . Źródło 4 lipca 2022 r .
- ^ a b Peto T, brytyjski zespół nadzoru bocznego przepływu COVID-19 (2021). „COVID-19: Szybkie wykrywanie antygenu SARS-CoV-2 za pomocą testu przepływu bocznego: krajowa systematyczna ocena czułości i swoistości testów masowych” . Ekliniczna medycyna . 36 : 100924. doi : 10.1016/j.eclinm.2021.100924 . PMC 8164528 . PMID 34101770 .
- ^ Mahase E (grudzień 2020). „Covid-19: masowe testy na Słowacji mogły pomóc ograniczyć infekcje” . BMJ . 371 : m4761. doi : 10.1136/bmj.m4761 . PMID 33293348 .
- ^ Agence France-Presse (2 listopada 2020). „Słowacja przeprowadza masowe testy Covid na dwóch trzecich populacji” . Strażnik . ISSN 0261-3077 . Źródło 11 lipca 2022 r .
- ^ Pavelka M, Van-Zandvoort K, Abbott S, Sherratt K, Majdan M, Jarčuška P i in. (2021). „Wpływ szybkich testów antygenowych w całej populacji na częstość występowania SARS-CoV-2 na Słowacji” . nauka . 372 (6542): 635–641. Bibcode : 2021Sci...372..635P . doi : 10.1126/science.abf9648 . PMC 8139426 . PMID 33758017 .
- ^ Boseley S, Elgot J (2 listopada 2020). „Liverpool będzie pionierem w Wielkiej Brytanii jako pierwsza próba masowych testów Covid” . Strażnik . ISSN 0261-3077 . Źródło 11 lipca 2022 r .
- ^ Littlejohns P (6 listopada 2020). „Wielka Brytania testuje test przepływu bocznego do masowej diagnozy Covid-19 – jak to działa?” . Urządzenia medyczne NS .
- ^ Sigsworth T (19 listopada 2020). „Aktualności dotyczące Covid-19: testy przepływu bocznego na uniwersytecie dostępne do rezerwacji od jutra” . Palatynat . Źródło 11 lipca 2022 r .
- ^ „Covid-19: uniwersytety będą nadzorować exodus studentów na Boże Narodzenie” . wiadomości BBC . 11 listopada 2020 . Źródło 11 lipca 2022 r .
- ^ Serle J (9 listopada 2020). „Personel NHS otrzymuje dwa razy w tygodniu domowe testy covidowe ze skutkiem natychmiastowym” . Dziennik służby zdrowia . Źródło 11 lipca 2022 r .
- ^ „Szybsze testy na COVID-19 zostaną wprowadzone w całej Anglii” . GOV.Wielka Brytania . 10 listopada 2020 . Źródło 12 lipca 2022 r .
- ^ „COVID-19: Mieszkańcy domu opieki zezwolili na widywanie się z rodziną po przeprowadzeniu szybkich testów –„ to było bardzo emocjonalne ” ” . Wiadomości z nieba . 25 grudnia 2020 . Źródło 12 lipca 2022 r .
- ^ „149 milionów funtów na wsparcie zwiększonych testów w domach opieki” . GOV.Wielka Brytania . 23 grudnia 2020 . Źródło 12 lipca 2022 r .
- ^ „Masowe testy w Merthyr Tydfil potrwają do piątku” . 14 grudnia 2020 . Źródło 12 lipca 2022 r .
- ^ Wightwick A (10 grudnia 2020). „Opublikowano wyniki masowych testów na koronawirusa w szkołach Merthyr” . Walia Online . Źródło 12 lipca 2022 r .
- ^ „Projekty wdrożenia szybkiego testu diagnostycznego wykrywającego antygen SARS-CoV-2” . www.kto.int . 10 listopada 2020 . Źródło 27 grudnia 2020 r .
- ^ „Globalne partnerstwo na rzecz udostępnienia 120 milionów niedrogich, wysokiej jakości szybkich testów COVID-19 dla krajów o niskich i średnich dochodach” . www.kto.int . 28 września 2020 . Źródło 27 grudnia 2020 r .
- ^ „Masowe testy na COVID-19 w Austrii: wszystkie szczegóły” . Vindobona.org | Wiedeńskie wiadomości międzynarodowe . Źródło 27 grudnia 2020 r .
- ^ „„ 20 000 dziennie ”: jak działają masowe testy w Austrii” . www.lokalny.at . 7 grudnia 2020 r. Zarchiwizowane od oryginału w dniu 9 grudnia 2020 r . Źródło 27 grudnia 2020 r .
- ^ Gremmels H, Winkel BM, Schuurman R, Rosingh A, Rigter NA, Rodriguez O i in. (styczeń 2021). „Prawdziwa walidacja szybkiego testu Panbio™ COVID-19 antigen (Abbott) u osób mieszkających w społeczności z objawami potencjalnego zakażenia SARS-CoV-2” . Ekliniczna medycyna . 31 : 100677. doi : 10.1016/j.eclinm.2020.100677 . PMC 7832943 . PMID 33521610 .
- ^ Batra R, Olivieri LG, Rubin D, Vallari A, Pearce S, Olivo A i in. (listopad 2020). „Ocena porównawcza szybkiego testu Abbott Panbio™ COVID-19 IgG/IgM i testu Abbott Architect™ SARS CoV-2 IgG” . Journal of Clinical Virology . 132 : 104645. doi : 10.1016/j.jcv.2020.104645 . PMC 7493757 . PMID 32961429 .
- ^ Basu A, Zinger T, Inglima K, Woo KM, Atie O, Yurasits L i in. (lipiec 2020). „Wydajność testu szybkiej amplifikacji kwasu nukleinowego COVID-19 firmy Abbott ID Now przy użyciu wymazów z nosogardzieli transportowanych w wirusowych mediach transportowych i suchych wymazów z nosa w instytucji akademickiej w Nowym Jorku” . Journal of Clinical Microbiology . 58 (8). doi : 10.1128/JCM.01136-20 . PMC 7383552 . PMID 32471894 .
- ^ „Szybkie testy na COVID-19 rozszerzają się na wrażliwe populacje w Albercie” . thestar.com . 23 grudnia 2020 . Źródło 27 grudnia 2020 r .
- ^ Kokosy Bali (22 grudnia 2020). „Pasażerowie tworzą długie kolejki, aby wykonać szybkie testy antygenowe na lotnisku Ngurah Rai na Bali | Coconuts Bali” . Kokosy . Źródło 27 grudnia 2020 r .
- ^ Pinto R, Iyer M (28 czerwca 2020). „Mumbaj: Ponieważ w tym tygodniu rozpoczynają się 15-minutowe szybkie testy, spodziewany jest wzrost liczby przypadków” . Wiadomości z Bombaju. Czasy Indii . Źródło 27 grudnia 2020 r .
- ^ Allen V (11 grudnia 2020). „Jak szybkie wyniki testów domowych na COVID-19 mogą obniżyć wskaźnik infekcji” . Sygnał dnia . Źródło 4 lipca 2022 r .
- ^ Haseltine WA (11 grudnia 2020). „Nawet przy szczepionce nadal potrzebujemy szybkich testów, aby zakończyć Covid-19” . Forbesa . Źródło 4 lipca 2022 r .
- ^ Dickerson MD, Ditch D (22 grudnia 2020). „9 rzeczy, które musisz wiedzieć o wartym 1,4 biliona dolarów zbiorczym roku podatkowym 2021 i pakiecie COVID-19 o wartości 900 miliardów dolarów” . Fundacja Dziedzictwa . Źródło 4 lipca 2022 r .
- ^ „Aktualizacja dotycząca koronawirusa (COVID-19): FDA wydaje nowe zezwolenie na domowy test karty BinaxNOW COVID-19 Ag” . Administracja Jedzenia i Leków. 16 grudnia 2020 . Źródło 4 lipca 2022 r .
- ^ Wan W (16 grudnia 2020). „Jak działają domowe testy na koronawirusa? Gdzie mogę je dostać?” . Washington Post . Źródło 4 lipca 2022 r .
- ^ Odwaga KH (18 grudnia 2020). „Szybkie domowe testy na Covid-19 są wreszcie dostępne. Oto jak mogą pomóc zakończyć pandemię” . Głos . Źródło 4 lipca 2022 r .
- Bibliografia _ „Covid-19: brytyjski regulator zatwierdza test przepływu bocznego do użytku domowego pomimo obaw dotyczących dokładności” . BMJ . 371 : m4950. doi : 10.1136/bmj.m4950 . PMID 33361088 .
- ^ Woodcock A (5 grudnia 2020). „Negatywny wynik szybkiego testu Covid nie jest zielonym światłem do rezygnacji z dystansu społecznego, ostrzega naczelny medyk” . Niezależny . Źródło 8 lipca 2022 r .
- ^ a b „Koronawirus: Komisja przedstawia przepisy dotyczące szybkich testów antygenowych i zabezpiecza 20 milionów testów dla państw członkowskich” . Komisja Europejska . 18 grudnia 2020 . Źródło 8 lipca 2022 r .
- ^ „Rada zgadza się na wzmocnienie stosowania szybkich testów antygenowych i wzajemne uznawanie wyników testów na COVID-19” . Rada Unii Europejskiej. 21 stycznia 2021 . Źródło 4 lipca 2022 r .
- ^ Biden JR Jr (21 stycznia 2021). „Krajowa strategia reagowania na COVID-19 i gotowości na pandemię” (PDF) . Biały Dom . Źródło 4 lipca 2022 r .
- ^ „Aktualizacja dotycząca koronawirusa (COVID-19): FDA kontynuuje rozwój bez recepty i innych testów przesiewowych” . Administracja Jedzenia i Leków. 31 marca 2021 . Źródło 4 lipca 2022 r .
- ^ a b „Przestań używać szybkiego testu jakościowego antygenu Innova SARS-CoV-2: komunikat bezpieczeństwa FDA” . Administracja Jedzenia i Leków. 10 czerwca 2021 . Źródło 4 lipca 2022 r .
- ^ Hale C (18 czerwca 2021). „Wielka Brytania podwaja szybki test COVID-19 Innova po tym, jak FDA wezwała użytkowników do wyrzucenia go” . FierceBiotech . Źródło 4 lipca 2022 r .
- ^ „Ellume przypomina domowy test COVID-19 pod kątem potencjalnie fałszywie dodatnich wyników testu SARS-CoV-2” . Administracja Jedzenia i Leków. 16 listopada 2021 . Źródło 4 lipca 2022 r .
- ^ ab Diaz J, Naylor B (21 grudnia 2021). „Biden ogłasza bezpłatne testy i broni reakcji Białego Domu w miarę wzrostu liczby przypadków COVID” . Narodowe Radio Publiczne . Waszyngton, DC . Źródło 4 lipca 2022 r .
- ^ Naylor B (14 stycznia 2022). „Od środy będzie można zamówić bezpłatne domowe zestawy testowe na COVID” . Narodowe Radio Publiczne . Waszyngton, DC . Źródło 4 lipca 2022 r .
- ^ „Fałszywe domowe testy diagnostyczne COVID-19 bez recepty” . Administracja Jedzenia i Leków. 29 kwietnia 2022 . Źródło 4 lipca 2022 r .
- ^ Jakobsen KK, Jensen JS, Todsen T, Tolsgaard MG, Kirkby N, Lippert F i in. (2021). „Dokładność i koszt opisu szybkiego testu antygenowego w porównaniu z reakcją łańcuchową polimerazy z odwrotną transkryptazą do wykrywania SARS-CoV-2” . Dan Med J. 68 (7): A03210217. PMID 34169830 .
- ^ Diel R, Hittel N, Nienhaus A (2021). „Badanie antygenu COVID-19 w miejscu opieki nad narażonymi niemieckimi pracownikami służby zdrowia — model kosztów” . Int J Environ Res Public Health . 18 (20): 10767. doi : 10.3390/ijerph182010767 . PMC 8536062 . PMID 34682514 .
- ^ Du Z, Pandey A, Bai Y, Fitzpatrick MC, Chinazzi M, Pastore y Piontti A i in. (2021). „Porównawcza opłacalność strategii testowania SARS-CoV-2 w USA: badanie modelowe” . Lancet Zdrowia Publicznego . 6 (3): e184 – e191. doi : 10.1016/S2468-2667(21)00002-5 . PMC 7862022 . PMID 33549196 .
- ^ Paltiel AD, Zheng A, Sax PE (2021). „Kliniczne i ekonomiczne skutki powszechnych szybkich testów w celu zmniejszenia transmisji SARS-CoV-2” . Anna Stażysta Med . 174 (6): 803–810. doi : 10.7326/M21-0510 . PMC 9317280 . PMID 33683930 .
- ^ „Globalny raport z badania rynku zestawów szybkich testów antygenowych COVID-19 2022” . Raporty rynkowe Świat. 10 czerwca 2022 . Źródło 10 lipca 2022 r .
- ^ „Rynek szybkich zestawów testowych na antygen COVID-19 - globalne prognozy i prognozy 2022-2027” . Doradztwo i wywiad Arizton. czerwiec 2022 . Źródło 10 lipca 2022 r .
- Bibliografia _ . Raport z badania rynku. 17 lipca 2021 . Źródło 10 lipca 2022 r .