Waskulopatia alloprzeszczepu serca
 | |
| Waskulopatia alloprzeszczepu serca | |
|---|---|
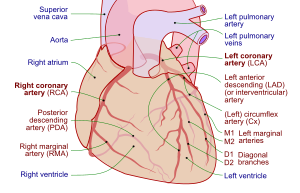
| Tętnice wieńcowe | |
| Specjalność | Kardiologia , angiologia |
| Objawy | Brak, duszność, zmęczenie |
| Zwykły początek | Po przeszczepie serca |
| Metoda diagnostyczna | angiografia wieńcowa , ultrasonografia wewnątrznaczyniowa , echokardiografia obciążeniowa dobutaminowa , pozytonowa tomografia emisyjna , angiografia CT , biomarkery , biopsja endomiokardialna |
| Leczenie | Kontrola czynników ryzyka sercowo-naczyniowego, inhibitory mTOR , retransplantacja |
| Lek | syrolimus , ewerolimus |
| Rokowanie | Progresywny |
| Częstotliwość | Około 50% (za 10 lat) |
| Zgony | 11-13% przeszczepów serca rok po operacji |
Waskulopatia alloprzeszczepu serca (CAV) jest postępującym typem choroby wieńcowej u osób po przeszczepie serca . Ponieważ serce dawcy utraciło dopływ nerwów, zwykle nie odczuwa bólu w klatce piersiowej, a CAV jest zwykle wykrywany podczas rutynowych badań. Może objawiać się takimi objawami, jak zmęczenie i duszność.
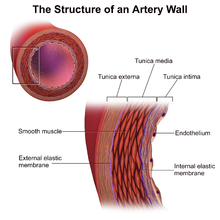
Powstaje, gdy naczynia krwionośne zaopatrujące przeszczepione serce zmieniają swoją strukturę. Stopniowo zwężają się i ograniczają przepływ krwi , co w konsekwencji prowadzi do uszkodzenia mięśnia sercowego lub nagłej śmierci. Oprócz tych samych czynników ryzyka choroby niedokrwiennej serca z powodu gromadzenia się blaszek miażdżycowych , CAV jest bardziej prawdopodobne , jeśli dawca był starszy lub zmarł w wyniku wybuchowej śmierci mózgu oraz w przypadku zakażenia wirusem cytomegalii . Jego mechanizm obejmuje czynniki immunologiczne ( wrodzone i adaptacyjne ) oraz nieimmunologiczne, z wyraźnymi cechami w próbkach histologicznych tętnic wieńcowych . Inne główne przyczyny śmierci po przeszczepie serca to niewydolność przeszczepu, odrzucenie narządu i infekcja.
Rozpoznanie polega na regularnej obserwacji i monitorowaniu przeszczepionego serca pod kątem wczesnych objawów choroby. Badania obejmują angiografię wieńcową , ultrasonografię wewnątrznaczyniową , echokardiografię wysiłkową z dobutaminą , pozytronową tomografię emisyjną , angiografię tomografii komputerowej (angiografię CT) i kilka biomarkerów .
statyn i aspiryny rozpoczyna się wcześnie po transplantacji i po wykryciu CAV. Leki, w tym syrolimus i ewerolimus , mogą spowolnić postęp choroby. Może być wymagany powtórny przeszczep serca.
CAV dotyka około połowy biorców przeszczepu serca w ciągu 10 lat. Przyczynia się do śmierci 11-13% rok po przeszczepie serca.
Definicja
Waskulopatia alloprzeszczepu serca jest przyspieszonym typem choroby wieńcowej u osób po przeszczepie serca.
Symptomy i objawy
W przeciwieństwie do dusznicy bolesnej w klatce piersiowej u osób, które nie przeszły przeszczepu serca, osoby z CAV zazwyczaj nie odczuwają bólu w klatce piersiowej, ponieważ serce dawcy utraciło zaopatrzenie w nerwy . Kilku odzyskuje nerwy po kilku latach i może rozwinąć się niezwykły ból w klatce piersiowej. Osoby z CAV mogą wykazywać szerokie spektrum objawów, w tym zmęczenie, nudności lub dyskomfort w jamie brzusznej lub mogą nie mieć żadnych objawów. Mogą również wystąpić duszności i arytmie .
Czynniki ryzyka
Podobnie jak w przypadku choroby wieńcowej u osób, które nie przeszły przeszczepu serca, czynniki ryzyka CAV obejmują wysokie ciśnienie krwi , wysoki poziom cholesterolu i cukrzycę . Inne czynniki ryzyka występujące wyłącznie w przypadku CAV obejmują starszych dawców , zakażenie wirusem cytomegalii i krążące przeciwciała po przeszczepie serca. Wykazano, że istotnym czynnikiem jest mechanizm śmierci mózgu dawcy, w szczególności wybuchowa śmierć mózgu dawcy. Jest to prawdopodobnie kombinacja urazów alloprzeszczepu które określają ryzyko rozwoju CAV.
Mechanizm
immunologiczne ( wrodzone i adaptacyjne ) oraz nieimmunologiczne przyczyniają się do złożonej patogenezy CAV.
U osób bez przeszczepu, u których rozwinęła się choroba wieńcowa z powodu miażdżycy, postęp choroby jest powolny, zmiany histologiczne ograniczają się głównie do głównych tętnic wieńcowych, a poszerzenie tętnic obserwuje się jako formę kompensacyjnej przebudowy. Jednak w przypadku CAV preparaty histologiczne zazwyczaj wykazują koncentryczne pogrubienie błony wewnętrznej głównych tętnic wieńcowych na powierzchni serca i tętnicach śródmięśniowych, które może ulec zatarciu w ciągu kilku lat. Występuje komórek mięśni gładkich , makrofagów piankowatych i limfocytarnych infiltruje. Można zauważyć, że wpływa to na całą długość tętnic wieńcowych i często na mniejsze tętnice. Zwapnienia nie zawsze występują w CAV, a jeśli się pojawiają, to dzieje się to późno. Kompensacyjne poszerzenie tętnic nie występuje w CAV. W przeciwieństwie do osób bez przeszczepu z chorobą wieńcową w przebiegu miażdżycy , w CAV niedrożność światła naczynia ze skrzepliną występuje rzadko.
Zapalenie i uszkodzenie śródbłonka może być wywołane zatrzymaniem dawcy , pobraniem narządu oraz niedokrwieniem i reperfuzją alloprzeszczepu .
Diagnoza
Ponieważ objawy są tak zmienne i często nieobecne, diagnoza była wyzwaniem. Dlatego zaleca się regularną obserwację i monitorowanie alloprzeszczepu pod kątem wczesnych objawów choroby.
Koronarografia
Obserwację prowadzi się regularnie powtarzając koronarografię w pracowni cewnikowania serca , jako badanie diagnostyczne z wyboru. Jest to zwykle wykonywane corocznie przez pierwsze pięć lat po przeszczepie. Angiografia w CAV charakterystycznie pokazuje rozlane zwężenia w dużych tętnicach wieńcowych i zmniejszoną liczbę mniejszych tętnic wieńcowych, znane również jako „przycinanie obwodowe”. Jednakże, ponieważ CAV często obejmuje całą długość tętnicy wieńcowej, CAV może nie być widoczny w samej angiografii.
USG wewnątrznaczyniowe (IVUS)
Ultrasonografia wewnątrznaczyniowa (IVUS) jest bardziej czuła w wykrywaniu subtelnych zmian w grubości błony wewnętrznej ścian tętnic i zapewnia pomiar światła tętnicy. Po przeszczepie seryjne pomiary porównuje się z linią podstawową. Większy niż 0,5 mm wzrost grubości błony wewnętrznej rok po transplantacji pozwala przewidzieć zmiany CAV w angiografii w ciągu pięciu lat. Paradoksalne zmniejszenie liczby naczyń krwionośnych można wykryć również za pomocą ultrasonografii wewnątrznaczyniowej.
IVUS jest jednak zwykle używany do badań ze względu na jego wady polegające na inwazyjności, wymaganiu użycia materiału kontrastowego i kosztów.
Echokardiografia wysiłkowa z dobutaminą (DSE)
Alternatywnie powszechnie wykonuje się echokardiografię wysiłkową z dobutaminą (DSE), która ma 85% czułość na obecność CAV. Ujemny wynik DSE koreluje z dobrym rokowaniem.
Inne nieinwazyjne metody diagnostyczne obejmują pozytonową tomografię emisyjną i angiografię tomografii komputerowej (angiografia CT). Ponadto zapis EKG może wykazywać nietypowe cechy niedokrwienia.
Biomarkery
Sugeruje się, że biomarkery zwiększonego ryzyka CAV obejmują białko C-reaktywne , peptyd natriuretyczny w surowicy i troponinę I.
Klasyfikacja
Stopień CAV po przeszczepie serca uzyskano z różnych źródeł, w tym z The Cardiac Transplant Research Database, rejestru ISHLT i rejestru The United Network for Organ Sharing.
Międzynarodowe Towarzystwo Transplantacji Serca i Płuc (ISHLT) sformułowało i ustandaryzowało terminologię opartą na wynikach diagnostycznych, aby określić obecność i ciężkość CAV, co z kolei odzwierciedla rokowanie. Ciężkość CAV określa się na podstawie stopnia zwężenia tętnic wieńcowych i obecności restrykcyjnej choroby serca.
| Kod | Powaga | Wyniki diagnostyczne |
|---|---|---|
| ISHLT CAV0 | Nieistotne | Brak wykrywalnych zmian w angiografii |
| ISHLT CAV 1 | Łagodny | Angiograficzna lewa pnia pnia (LM) 50% lub naczynie pierwotne z maksymalnym uszkodzeniem 70% lub jakiekolwiek zwężenie gałęzi 70% (w tym rozlane zwężenie) bez dysfunkcji alloprzeszczepu |
| ISHLT CAV 2 | Umiarkowany | Angiograficzna LM 50%; pojedyncze naczynie pierwotne 70% lub izolowane zwężenie gałęzi 70% w gałęziach 2 układów, bez dysfunkcji alloprzeszczepu |
| ISHLT CAV 3 | Ciężki : silny | Angiograficzna LM 50% lub dwa lub więcej naczyń pierwotnych 70% zwężenie lub pojedyncze zwężenie gałęzi 70% we wszystkich 3 systemach; lub ISHLT CAV1 lub CAV2 z dysfunkcją alloprzeszczepu (zdefiniowaną jako LVEF ≤ 45%, zwykle w obecności regionalnych nieprawidłowości ruchomości ścian) lub objawami fizjologii znacznego restrykcji |
Leczenie
statyny
Zapobieganie progresji CAV jest ważne, ponieważ po opracowaniu istniejące metody leczenia CAV są często nieskuteczne. Rozpoczęcie leczenia statynami prawastatyną i symwastatyną wcześnie po transplantacji zmniejsza częstość występowania i nasilenie CAV.
Witaminy
lekami immunosupresyjnymi, postęp CAV mógłby prawdopodobnie zostać spowolniony przez witaminy C i E.
Aspiryna
Ponieważ rola aspiryny jest już ustalona w chorobie wieńcowej u osób, które nie miały przeszczepu serca, zwykle podaje się ją również po przeszczepie serca.
Środki antyproliferacyjne
Wykazano, że po wykryciu CAV leki, w tym inhibitory mTOR, syrolimus i ewerolimus , spowalniają postęp choroby.
Inne opcje leczenia
Klinicznie istotny CAV może wymagać przezskórnej interwencji wieńcowej z powodu choroby ogniskowej, ale prawdopodobieństwo restenozy jest wysokie. Można rozważyć powtórne przeszczepienie serca.
Wynik
Gdy dochodzi do obniżenia frakcji wyrzutowej lewej komory i wystąpienia objawów niewydolności serca , rokowanie jest zazwyczaj złe. Ryzyko poważnych niepożądanych incydentów sercowo-naczyniowych wzrasta 3,4-krotnie, jeśli CAV jest obecny w angiografii.
Epidemiologia
Częstość CAV po przeszczepie serca uzyskano z różnych źródeł, w tym z The Cardiac Transplant Research Database, rejestru ISHLT i rejestru The United Network for Organ Sharing. W porównaniu z latami 1994-2001 nastąpił spadek częstości występowania CAV w latach 2001-2007. Dane ISHLT pokazują częstość występowania CAV na poziomie około 50% po 10 latach od przeszczepu serca.
CAV jest główną przyczyną późnej śmiertelności po przeszczepieniu serca. Większość nie jest ciężka, ale przyczynia się do śmierci 11-13% w ciągu roku od przeszczepu serca.
Historia
W przeciwieństwie do odrzucenia i zakażenia, CAV w przeszczepionym sercu nie był początkowo przewidywanym wynikiem. U osób, które wcześnie przeżyły przeszczepy serca, wkrótce rozwinęła się ta postać waskulopatii tętnic wieńcowych, początkowo zidentyfikowana podczas sekcji zwłok. Pojawiły się wczesne sugestie, że zapobieganie zakażeniu wirusem cytomegalii (CMV) może zmniejszyć częstość występowania CAV. Wpływ CAV zmieniał się w czasie, przy czym pierwsi biorcy byli młodsi, mieli więcej czynników odrzucania i ryzyka sercowo-naczyniowego oraz rzadziej stosowali statyny. Późniejsi biorcy rutynowo stosowali statyny i zostali zapoznani z lekiem immunosupresyjnym mykofenolanem mofetylu (MMF) i profilaktyka CMV. Ponadto późniejsi biorcy byli monitorowani pod kątem odrzucenia alloprzeszczepu serca za pośrednictwem przeciwciał (AMR).
Przed 2010 rokiem nie było jednolitych międzynarodowych standardów nazewnictwa CAV. Konsensus w sprawie standardowego języka dla CAV został po raz pierwszy opublikowany w 2010 roku przez ISHLT. Zostało to opracowane w sposób podobny do wcześniejszego systemu stopniowania ostrego odrzucania na podstawie biopsji endomiokardialnej .
Kierunki badań
Odrzucenie alloprzeszczepu serca za pośrednictwem przeciwciał (AMR) jest istotnym czynnikiem prowadzącym do szybkiego postępu CAV. Przyszłe kierunki badań w tej dziedzinie mogą obejmować prospektywne bazy danych korelujące czynniki kliniczne z obserwacją częstości występowania i ciężkości oporności na środki przeciwdrobnoustrojowe, częstością zakażenia CMV oraz stosowaniem leków immunosupresyjnych. Rola wywoływania tolerancji immunologicznej nie została jeszcze ustalona.