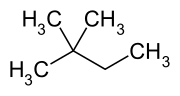
2,2-dimetylobutan
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2,2-dimetylobutan |
|||
| Inne nazwy Neoheksan, 22DMB
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 1730736 | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.000.825 | ||
| Numer WE |
|
||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS |
|
||
| UNII | |||
| Numer ONZ | 1208 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 6 H 14 | |||
| Masa cząsteczkowa | 86,178 g·mol -1 | ||
| Wygląd | Bezbarwna ciecz | ||
| Zapach | Bezwonny | ||
| Gęstość | 649 mg ml -1 | ||
| Temperatura topnienia | -102 do -98 °C; -152 do -145 ° F; 171 do 175 K | ||
| Temperatura wrzenia | 49,7 do 49,9 °C; 121,4 do 121,7 ° F; 322,8 do 323,0 K | ||
| dziennik P | 3.51 | ||
| Ciśnienie pary | 36,88 kPa (przy 20 ° C) | ||
|
Stała prawa Henry'ego
( k H ) |
6,5 nmol Pa -1 kg -1 | ||
| -76,24· 10-6 cm3 / mol | |||
|
Współczynnik załamania światła ( n D )
|
1.369 | ||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
189,67 JK -1 mol -1 | ||
|
Standardowa entropia molowa ( S ⦵ 298 ) |
272,00 JK -1 mol -1 | ||
|
Standardowa entalpia formowania (Δ f H ⦵ 298 ) |
−214,4–212,4 kJ mol −1 | ||
|
Standardowa entalpia spalania (Δ c H ⦵ 298 ) |
−4,1494–−4,1476 MJ mol −1 | ||
| Zagrożenia | |||
| Oznakowanie GHS : | |||
   
|
|||
| Niebezpieczeństwo | |||
| H225 , H304 , H315 , H336 , H411 | |||
| P210 , P261 , P273 , P301+P310 , P331 | |||
| NFPA 704 (ognisty diament) | |||
| Punkt zapłonu | -29 ° C (-20 ° F; 244 K) | ||
| 425 ° C (797 ° F; 698 K) | |||
| Wybuchowe granice | 1,2–7,7% | ||
| NIOSH (limity ekspozycji na zdrowie w USA): | |||
|
PEL (dopuszczalny)
|
nic | ||
| Związki pokrewne | |||
|
Powiązane alkany
|
|||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
2,2-dimetylobutan , potocznie znany jako neoheksan , jest związkiem organicznym o wzorze C 6 H 14 lub (H 3 C-) 3 -C-CH 2 -CH 3 . Jest to zatem alkan , rzeczywiście najbardziej zwarty i rozgałęziony z izomerów heksanu — jedyny z czwartorzędowym węglem i butanem (C4 ) w szkielecie.
Synteza
2,2-dimetylobutan można zsyntetyzować przez hydroizomeryzację 2,3-dimetylobutanu przy użyciu kwaśnego katalizatora.
Można go również syntetyzować przez izomeryzację n -pentanu w obecności katalizatora zawierającego kombinację jednego lub więcej palladu, platyny, rodu i renu na matrycy zeolitu, tlenku glinu, dwutlenku krzemu lub innych materiałów. Takie reakcje tworzą mieszaninę produktów końcowych, w tym izopentanu, n -heksanu, 3-metylopentanu, 2-metylopentanu, 2,3-dimetylobutanu i 2,2-dimetylobutanu. Ponieważ skład końcowej mieszaniny jest zależny od temperatury, pożądany składnik końcowy można otrzymać, wybierając katalizator i kombinację kontroli temperatury i destylacji.
Używa
Neoheksan jest stosowany jako dodatek do paliw oraz w produkcji chemii rolniczej. Jest również stosowany w wielu produktach handlowych, samochodowych i domowych, takich jak kleje, środki do czyszczenia styków elektronicznych i spraye do polerowania tapicerki.
W warunkach laboratoryjnych jest powszechnie stosowana jako cząsteczka sondy w technikach badania aktywnych miejsc katalizatorów metalicznych. Takie katalizatory są stosowane w reakcjach wymiany wodoru z deuterem, hydrogenolizy i izomeryzacji. Dobrze nadaje się do tego celu, ponieważ 2,2-dimetylobutan zawiera zarówno grupę izobutylową, jak i etylową.
Zobacz też
- Metylobutan (izopentan)
- 2-Metylopentan (izoheksan)


