2.2.2-Propellan
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Tricyklo[2.2.2.0 1,4 ]oktan |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
|
Identyfikator klienta PubChem
|
|||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 8 H 12 | |||
| Masa cząsteczkowa | 108,184 g·mol -1 | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
[2.2.2]Propellan , formalnie tricyklo[2.2.2.0 1,4 ]oktan , jest związkiem organicznym należącym do rodziny propellanów . Jest to węglowodór o wzorze C 8 H 12 lub C 2 (C 2 H 4 ) 3 . Jego cząsteczka ma trzy pierścienie z czterema atomami węgla w każdym, dzielące jedno wiązanie C-C.
Związek ten jest niestabilny (chociaż nie tak bardzo jak [1.1.1]propellan , ale jest mniej trwały niż [1.1.1]propellan). Kąty wiązań na wspólnych węglach są znacznie napięte: trzy z nich są bliskie 90°, pozostałe trzy do 120°. Energię odkształcenia szacuje się na 93 kcal/mol (390 kJ/mol).
Synteza
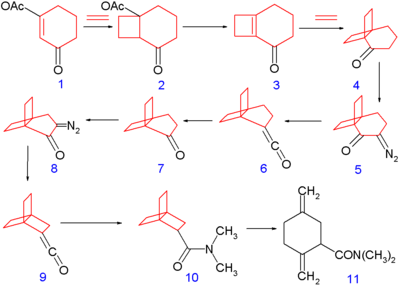
[2.2.2]Propellan został po raz pierwszy zsyntetyzowany w 1973 roku przez grupę Philipa Eatona (który wcześniej uzyskał kuban ), zgodnie z następującym schematem:
Synteza rozpoczyna się od fotochemicznej [2+2] cykloaddycji etylenu do pochodnej cykloheksenu 1 w celu wytworzenia związku bicyklicznego 2 , po której następuje reakcja eliminacji t -butanolanem potasu z kwasem octowym do cyklobutenu 3 , po czym następuje kolejna cykloaddycja etylenem do 4 . Związek ten przekształca się w diazoketon 5 przez deprotonowanie (przy użyciu kwasu octowego i metanolanu sodu ) i reakcję z azydkiem tosylu . Keton następnie przechodzi przegrupowanie Wolffa do ketenu 6 . Ozonoliza tworzy keton 7 , kolejne diazowanie daje diazoketon 8 , który ponownie ulega przegrupowaniu Wolffa do ketenu 9 . Reakcja z dimetyloaminą daje szkielet [2.2.2]propelanu z podstawnikiem dimetyloamidowym 10 .
Stwierdzono, że końcowy produkt 10 spontanicznie izomeryzuje w roztworze do monocyklicznego amidu 11 , z okresem półtrwania wynoszącym 28 minut w temperaturze pokojowej.
Pochodne
Wysoce fluorowany [2.2.0] propellan został również zsyntetyzowany przez grupę Davida Lemala.