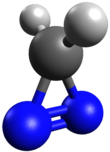Diazyryna
|
|
|||
| Identyfikatory | |||
|---|---|---|---|
|
|||
|
Model 3D ( JSmol )
|
|||
| 605387 | |||
| CHEBI |
|
||
| ChemSpider |
|
||
|
Identyfikator klienta PubChem
|
|
||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
||
|
|||
|
|||
| Nieruchomości | |||
| C H 2 N 2 | |||
| Masa cząsteczkowa | 42,041 g · mol -1 | ||
| Związki pokrewne | |||
|
Związki pokrewne
|
1H-diazyren | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
W chemii organicznej diazyryny to klasa cząsteczek organicznych składających się z węgla związanego z dwoma atomami azotu , które są ze sobą połączone wiązaniami podwójnymi , tworząc pierścień podobny do cyklopropenu , 3H -diazyren ( >CN 2 ). Są izomeryczne z grupami diazowęglowymi ( >C=N=N ) i podobnie jak one mogą służyć jako prekursory karbenów poprzez utratę cząsteczki diazotu. Na przykład napromieniowanie diazyryn światłem ultrafioletowym prowadzi do wstawienia karbenu w różne wiązania C-H , N-H i OH . W związku z tym diazyryny zyskały na popularności jako małe, fotoreaktywne , sieciujące odczynniki. Są one często wykorzystywane w znakowania fotopowinowactwa do obserwacji różnych interakcji, w tym interakcji ligand -receptor, ligand- enzym , białko-białko i białko- kwas nukleinowy .
Synteza
W literaturze istnieje wiele sposobów wytwarzania diazyryn, które rozpoczynają się od różnych odczynników.
Synteza z ketonów
Ogólnie schematy syntezy rozpoczynające się od ketonów ( >C=O ) obejmują konwersję ketonu z żądanymi podstawnikami do diazyrydyn ( >CN 2 H 2 ). Te diazirideny są następnie utleniane z wytworzeniem pożądanych diazyryn.
Diazyrydyny można wytworzyć z ketonów przez oksymację, następnie tosylację (lub mesylację ), a na końcu przez traktowanie amoniakiem ( NH 3 ). Ogólnie reakcje oksymowania przeprowadza się w reakcji ketonu z chlorkiem hydroksyloamoniowym ( NH 3 OH - Cl + ) w warunkach ogrzewania w obecności zasady, takiej jak pirydyna . Późniejsze tosylowanie lub mesylowanie alfa-podstawionego tlenu tosylu lub mesylu w obecności zasady daje oksym tosylu lub mesylu . Ostateczna obróbka oksymu tosylu lub mesylu amoniakiem daje diazyrydynę.
Diazyrydyny można również wytwarzać bezpośrednio w reakcji ketonów z amoniakiem w obecności środka aminującego , takiego jak monochloramina lub hydroksyloamina, kwas O-sulfonowy.
Diazyrydyny można utleniać do diazyryn wieloma metodami. Obejmują one utlenianie chromu , takie jak utlenianie Jonesa , utlenianie jodem i trietyloaminą , utlenianie tlenkiem srebra , utlenianie chlorkiem oksalilu, a nawet utlenianie elektrochemiczne na anodzie platynowo-tytanowej.
Synteza w reakcji Grahama
Diazyryny można alternatywnie wytwarzać w procesie jednonaczyniowym, stosując reakcję Grahama , wychodząc z amidyn . Ta reakcja daje fluorowcowaną diazyrynę, której halogen można zastąpić różnymi odczynnikami nukleofilowymi .
Chemia
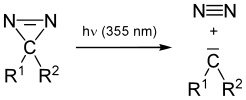
Po napromieniowaniu światłem UV diazyryny tworzą reaktywne formy karbenów . Karben może występować w postaci singletowej, w której dwa wolne elektrony zajmują ten sam orbital lub w formie trypletowej, z dwoma niesparowanymi elektronami na różnych orbitalach.
Produkty karbenowe Triplet vs Singlet
Podstawniki na diazyrynie wpływają na to, które rodzaje karbenów są generowane po napromieniowaniu i późniejszym rozszczepieniu fotolitycznym. Podstawniki diazyrynowe, które z natury są donorami elektronów, mogą przekazywać gęstość elektronów pustemu p-orbitalowi karbenu, który zostanie utworzony, a zatem mogą stabilizować stan singletowy. Na przykład fenylodiazyryna wytwarza fenylokarben w stanie singletowego karbenu, podczas gdy p-nitrofenylochlorodiazyryna lub trifluorofenylodiazyryna wytwarzają odpowiednie trypletowe produkty karbenowe.
Podstawniki będące donorami elektronów mogą również sprzyjać fotoizomeryzacji do liniowego związku diazowego [30] , a nie singletowego karbenu, a zatem związki te są niekorzystne do stosowania w testach biologicznych. Z drugiej strony, w szczególności trifluoroarylodiazyryny wykazują korzystną stabilność i właściwości fotolityczne i są najczęściej stosowane w zastosowaniach biologicznych.
Karbeny wytwarzane z diazyryn są szybko gaszone w reakcji z cząsteczkami wody, a zatem wydajności fotoreaktywnych testów sieciowania są często niskie. Ponieważ jednak ta cecha minimalizuje niespecyficzne etykietowanie, w rzeczywistości jest to zaleta stosowania diazyryn.
Zastosowanie w sieciowaniu fotoreaktywnym
Diazyryny są często stosowane jako fotoreaktywne odczynniki sieciujące, ponieważ reaktywne karbeny, które tworzą po napromieniowaniu światłem UV, mogą wstawiać się w wiązania CH, NH i OH. Powoduje to zależne od bliskości znakowanie innych gatunków związkiem zawierającym diazyrynę.
Diazyryny są często preferowane w stosunku do innych fotoreaktywnych odczynników sieciujących ze względu na ich mniejszy rozmiar, dłuższą długość fali napromieniowania, wymagany krótki okres naświetlania oraz stabilność w obecności różnych nukleofili, zarówno w warunkach kwaśnych, jak i zasadowych. Benzofenony , które po napromieniowaniu tworzą reaktywne formy karbonylu typu triplet, często wymagają długich okresów naświetlania, co może skutkować niespecyficznym znakowaniem, a ponadto są często obojętne na różne rozpuszczalniki polarne. Azydki arylu wymagają promieniowania o niskiej długości fali, które może uszkodzić badane makrocząsteczki biologiczne.
Przykłady w badaniach znakowania receptorów
Diazyryny są szeroko stosowane w badaniach znakowania receptorów. Dzieje się tak, ponieważ analogi różnych ligandów zawierające diazyrynę można syntetyzować i inkubować z ich odpowiednimi receptorami, a następnie wystawiać na działanie światła w celu wytworzenia reaktywnych karbenów. Karben będzie kowalencyjnie wiązał się z resztami w miejscu wiązania receptora. Związek karbenowy może zawierać bioortogonalny znacznik lub uchwyt, za pomocą którego można wyizolować białko będące przedmiotem zainteresowania. Białko można następnie strawić i zsekwencjonować za pomocą spektrometrii masowej w celu zidentyfikowania, z którymi resztami związany jest ligand zawierający karben, a tym samym tożsamości miejsca wiązania w receptorze.
Przykłady diazyryn stosowanych w badaniach znakowania receptorów obejmują:
- Odkrycie receptora brassinosteroidowego dla brasinosteroidowych hormonów roślinnych przez Kinoshita i in. Naukowcy wykorzystali analog hormonu roślinnego z ugrupowaniem sieciującym diazyrynę i znacznik biotynowy do izolacji w celu zidentyfikowania nowego receptora. Badanie to doprowadziło do wielu podobnych badań przeprowadzonych w odniesieniu do innych hormonów roślinnych.
- Odkrycie nowych receptorów kannabinoidowych innych niż CB1/CB2 przy użyciu sond analogowych anandamidu zawierających grupę diazyrynową przez Balasa i in.
- Jama wiążąca środka nasennego propofolu w receptorze GABA A przy użyciu analogu propofolu zawierającego diazyrynę.
Przykłady w badaniach enzym-substrat
W sposób analogiczny do znakowania receptorów, związki zawierające diazyrynę, które są analogami naturalnych substratów, zostały również wykorzystane do identyfikacji kieszeni wiążących enzymów. Przykłady obejmują:
- Synteza diazyryny zawierającej analog etopozydu , szeroko stosowanego leku przeciwnowotworowego ukierunkowanego na topoizomerazę II , co daje nadzieję na identyfikację miejsca wiązania etopozydu.
- Odkrycie, że inhibitory gamma-sekretazy typu kaprolaktamu celują w podjednostkę SPP gamma-sekretazy , która jest powiązana z chorobą Alzheimera.
Przykłady w badaniach kwasów nukleinowych
Diazyryny były również używane w eksperymentach znakowania fotopowinowactwem z udziałem kwasów nukleinowych. Przykłady obejmują:
- Włączenie ugrupowania diazyryny do cukru nukleozydowego w polimerze DNA w celu zbadania interakcji między mniejszym rowkiem DNA a polimerazami DNA.
- Włączenie ugrupowania diazyryny do zasady nukleozydowej w polimerze DNA w celu zbadania sposobu naprawy DNA przez białka.
Diazyryny były również używane do badania interakcji białek z lipidami, na przykład interakcji różnych sfingolipidów z białkami in vivo.
30. SM Korneev: Izomeryzacja walencyjna między związkami diazowymi i diazyrynami . W: EUR. J.Org. chemia (2011), zespół 31, S. 6153–6175, doi: 10.1002/ejoc.201100224