MG132
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
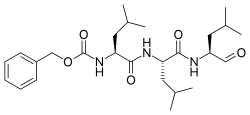
Benzyl [(2S ) -4-metylo-1-{[(2S ) -4-metylo-1-{[(2S ) -4-metylo-1-oksopentan-2-ylo]amino}-1- oksopentan-2-ylo]amino}-1-oksopentan-2-ylo]karbaminian |
|
| Inne nazwy N -benzyloksykarbonylo- L -leucylo- L -leucylo- L -leucynal Z-Leu-Leu-Leu-al |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C26H41N3O5 _ _ _ _ _ _ _ | |
| Masa cząsteczkowa | 475,630 g·mol -1 |
| Wygląd | Białe ciało stałe |
| Rozpuszczalność | 100 mM w EtOH i DMSO |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
MG132 Ki jest silnym, odwracalnym i przepuszczalnym dla komórek inhibitorem proteasomu ( = 4 nM). Należy do klasy syntetycznych aldehydów peptydowych. Zmniejsza degradację z ubikwityną w komórkach ssaków i przepuszczalnych szczepach drożdży przez kompleks 26S bez wpływu na aktywność ATPazy lub izopeptydazy . MG132 aktywuje N-końcową kinazę c-Jun (JNK1), która inicjuje apoptozę . MG132 hamuje również aktywację NF-κB za pomocą IC 50 3 μM i zapobiega rozszczepianiu β-sekretazy .
Mechanizm molekularny
Istnieje kilka inhibitorów, które mogą łatwo wnikać do komórki i selektywnie hamować szlak degradacyjny. Obejmuje aldehydy peptydowe, takie jak Cbz-leu-leu-leucynal (MG132), Cbz-leu-leu-norwalinal (MG115) i acetylo-leu-leu-norleucynal (ALLN). Są to analogi substratów i silne inhibitory stanu przejściowego chymotrypsyny aktywności maszynerii proteasomu . Wiadomo również, że aldehydy peptydowe hamują pewne lizosomalne proteazy cysteinowe i kalpainy , stąd MG132 może nie być wyłącznym inhibitorem szlaku proteasomalnego.