Rak olbrzymiokomórkowy płuc
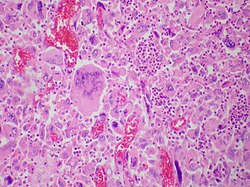 | |
| Rak olbrzymiokomórkowy płuc | |
|---|---|
| Rak olbrzymiokomórkowy płuc reprezentuje rzadką odmianę niedrobnokomórkowego raka płuc, charakteryzującego się obecnością licznych olbrzymich komórek nowotworowych i napływem komórek zapalnych, które są głównie leukocytami wielojądrzastymi z domieszką makrofagów. Gęste owalne agregaty leukocytów polimorfojądrowych widoczne na tym obrazie są prawdopodobnie zlokalizowane w cytoplazmie komórek olbrzymich guza (emperiopolesis), które zostały pocięte w płaszczyźnie, która nie obejmuje ich jąder. | |
| Specjalność |
Onkologia |
Olbrzymiokomórkowy rak płuca ( GCCL ) jest rzadką histologiczną postacią wielkokomórkowego raka płuca , podtypu niezróżnicowanego raka płuca , tradycyjnie zaliczanego do niedrobnokomórkowych raków płuca (NSCLC).
Charakterystyczną cechą tego wysoce śmiercionośnego nowotworu jest charakterystyczny mikroskopijny wygląd niezwykle dużych komórek , które są dziwaczne i wysoce pleomorficzne , i które często zawierają więcej niż jedno ogromne, zniekształcone, pleomorficzne jądro ( „ syncytia ”), które powstają z komórek fuzja .
Chociaż w literaturze dotyczącej raka płuc często określa się histologicznie mieszane guzy zawierające znaczną liczbę złośliwych komórek olbrzymich jako „raki olbrzymiokomórkowe”, technicznie diagnoza „raka olbrzymiokomórkowego” powinna być ograniczona wyłącznie do nowotworów zawierających tylko złośliwe komórki olbrzymie komórek (tj. „czystego” raka olbrzymiokomórkowego).
Oprócz dużej heterogenności obserwowanej w raku płuca (szczególnie u palaczy tytoniu), znacznej zmienności w diagnostyce i technikach pobierania próbek stosowanych w praktyce medycznej, wysokim względnym odsetku osób z podejrzeniem GCCL, które nie są poddawane całkowitej resekcji chirurgicznej , oraz niemal powszechny brak pełnego cięcia i badania patologicznego wyciętych próbek guza uniemożliwia wysoki poziom dokładności ilościowej.
Klasyfikacja
Przez kilka dziesięcioleci pierwotny rak płuc był konsekwentnie dychotomicznie klasyfikowany do celów leczenia i badań na drobnokomórkowy rak płuca (SCLC) i niedrobnokomórkowy rak płuca (NSCLC), w oparciu o nadmiernie uproszczone podejście, które jest obecnie wyraźnie przestarzałe. Nowy paradygmat uznaje, że raki płuc to duża i niezwykle heterogenna rodzina nowotworów złośliwych , z ponad 50 różnymi wariantami histologicznymi zawartymi w czwartej (2004) rewizji systemu typowania Światowej Organizacji Zdrowia , najczęściej stosowanego schematu klasyfikacji raka płuc („ WHO-2004"). Warianty te są coraz bardziej doceniane jako mające różne właściwości genetyczne , biologiczne i kliniczne , w tym rokowania i odpowiedzi na schematy leczenia , a zatem prawidłowa i spójna klasyfikacja histologiczna raka płuc jest niezbędna do walidacji i wdrożenia optymalnych strategii postępowania.
Około 1% przypadków raka płuc to mięsaki , guzy zarodkowe i nowotwory układu krwiotwórczego , podczas gdy 99% przypadków raka płuc to rak . Raki to nowotwory złożone z transformowanych, nieprawidłowych komórek o tkanki nabłonkowej i/lub cechach molekularnych , które wywodzą się z embrionalnej endodermy . W klasyfikacji WHO-2004 rozpoznano osiem głównych taksonów raków płuc:
- Rak drobnokomórkowy
- Rak kolczystokomórkowy
- Rak gruczołowy
- Rak wielkokomórkowy
- Rak gruczolakowaty
- Rak sarkomatoidalny
- Rakowiak
- Rak ślinopodobny
Podklasyfikacja GCCL wśród tych głównych taksonów uległa znaczącym zmianom w ostatnich dziesięcioleciach. W drugiej rewizji (1981) klasyfikacji WHO uznano go za podtyp raka wielkokomórkowego . W trzeciej rewizji (1999) został umieszczony w taksonie zwanym „Raki z elementami pleomorficznymi, sarkomatoidalnymi lub mięsakowatymi”, wraz z rakiem pleomorficznym, rakiem wrzecionowatokomórkowym , rakiem mięsakiem i blastoma płuc , które są (prawdopodobnie) spokrewnionymi wariantami. Podczas gdy czwarta rewizja („WHO-2004”) zachowała tę samą grupę zmian, co trzecia rewizja, nazwa głównego taksonu została skrócona do „ raków sarkomatoidalnych ”.
Obecne zasady klasyfikacji raka płuca w ramach WHO-2004, choć przydatne i udoskonalone, pozostają do pewnego stopnia dość złożone, niejednoznaczne, arbitralne i niekompletne. Chociaż dość często guzy mieszane, które zawierają złośliwe komórki olbrzymie, są nazywane „rakami olbrzymiokomórkowymi”, dokładna klasyfikacja guza płuc jako GCCL wymaga, aby cały guz składał się wyłącznie ze złośliwych komórek olbrzymich. Dlatego całkowite pobranie próbki całego guza — uzyskanego poprzez resekcję chirurgiczną — jest absolutnie konieczne do postawienia ostatecznej diagnozy GCCL.
Cytologia
Tło zawierało liczne limfocyty i neutrofile. Kształt komórki nowotworowej był wrzecionowaty lub pleomorficzny, a rozmiary komórek nowotworowych zmieniały się ponad 5-krotnie. Komórki nowotworowe miały obfitą, grubą i dobrze odgraniczoną cytoplazmę. Położenie jądra było odśrodkowe, a jądro było owalne lub o nieregularnym kształcie. Często obserwowano wielojądrzaste komórki olbrzymie. Rozmiar jądra był ponad 5 razy większy niż normalnych limfocytów, a jego rozmiar również zmieniał się ponad 5-krotnie. Błona jądrowa była cienka, a chromatyna jądrowa była grubo ziarnista, podczas gdy jąderko było pojedyncze i okrągłe.
W preparatach cytologicznych komórki olbrzymie zwykle pojawiają się jako pojedyncze komórki lub w płaskich luźnych skupiskach, a czasami w pęczkach.
GCCL są uważane za członka najpowszechniejszego typu raka płuc , zwanego „ rakiem niedrobnokomórkowym ”. Ta grupa śmiertelnych nowotworów stanowi około 85% wszystkich raków płuca. Zgodnie z definicją „raka wielkokomórkowego w porównaniu z rakiem drobnokomórkowym”, średnica komórek GCCL musi być znacznie większa niż trzykrotność średnicy spoczynkowego (tj. niestymulowanego) limfocytu . Również z definicji GCCL nie zawierają żadnej ilości tych małych, neuroendokrynnych komórek neuroendokrynnych , które są charakterystyczne dla raków drobnokomórkowych — kiedy tak się dzieje, guz powinien być klasyfikowany jako złożony rak drobnokomórkowy .
W porównaniu z większością innych wariantów raka płuc, komórki zawierające GCCL są zwykle znacznie większe (do 150 mikrometrów średnicy lub nawet większe). Zarówno komórki, jak i jądra wykazują skrajne różnice w rozkładzie wielkości i kształcie. Zgłaszano, że jądra raka komórek olbrzymich są średnio 5 razy większe niż jądra limfocytów.
Komórki raków olbrzymiokomórkowych są anaplastyczne i nie wykazują oznak dojrzewania ani różnicowania komórek, brakuje im cytologicznych i tkankowych cech architektonicznych raka płaskonabłonkowego , gruczolakoraka , raków neuroendokrynnych lub innych bardziej zróżnicowanych typów komórek raka płuc. Zwykle są wysoce pleomorficzne (tj. zmienne pod względem charakterystyki), ale najczęściej mają kształt okrągły i/lub wielokątny, ze stosunkowo niskim stosunkiem liczby jąder do cytoplazmy . W połączeniu z komórkami wrzecionowatymi, co bardzo często występuje w nowotworach o mieszanej histologii, złośliwe komórki olbrzymie mają tendencję do tworzenia w badaniu cytologicznym luźno spójnych struktur agregatowych. Jednakże, gdy biopsyjna składa się wyłącznie ze złośliwych komórek olbrzymich, komórki te są zwykle pojedyncze i zdezagregowane.
Seria przypadków sugeruje, że względna liczba komórek olbrzymich w danym guzie jest na ogół wprost proporcjonalna do wielkości guza i względnej ilości martwicy.
Komórki olbrzymie w raku płuc są silnie związane z obecnością komórek wrzecionowatych.
Chromatyna złośliwych komórek olbrzymich jest zwykle hiperchromatyczna i grubo zbrylona. Jądra są zwykle liczne i widoczne.
Cechy subkomórkowe często obserwowane w złośliwych komórkach olbrzymich przypadków GCCL obejmują obfite mitochondria, koncentryczne zwoje fibryli podobnych do tonofilamentów i agregaty kilku par centrioli.
Zarówno emperipoleza „komórka nowotworowa-komórka nowotworowa”, jak i „leukocyt-komórka nowotworowa” (tj. aktywna penetracja tej drugiej przez pierwszą) jest bardzo często obserwowana w przypadkach GCCL.
Cechy architektury tkanki
W guzach mieszanych komórki olbrzymie częściej występują w większych proporcjach na krawędzi guza. Gdy występuje rozległa martwica, możliwe jest, że guz olbrzymiokomórkowy ma tylko cienką obwódkę żywych komórek pozostających na obwodzie masy. [ potrzebne źródło ]
W jednej z wczesnych serii przypadków zauważono, że obfite wytwarzanie luźnych złośliwych komórek olbrzymich wypełnia pęcherzyki płucne pacjentów bez niszczenia, naciekania lub zakłócania normalnej podstawowej architektury, co jest patologicznym zachowaniem, które w pewnym stopniu przypomina płucną odmianę raka oskrzelikowo-pęcherzykowego .
Rozległa martwica guza i krwotok są niezwykle częste w GCCL.
Chociaż kwestia ta nie została dokładnie zbadana w kontrolowany sposób, stwierdzono, że GCCL zawierają znacznie podwyższone poziomy VEGF . Jednak w jednym badaniu, w którym guz raka olbrzymiokomórkowego, który został całkowicie wycięty, został pocięty i zbadany, nie odnotowano żadnych jakościowych ani ilościowych nieprawidłowości w unaczynieniu tkanek.
Zauważono, że GCCL jest zamknięty w kapsułkach i podzielony przez przegrody na „pseudolobule” przez wysoce włóknisty zrąb, co do którego sugeruje się, że jest wytwarzane proporcjonalnie do wzrostu guza. Kapsułka jest zazwyczaj naciekana złośliwymi komórkami olbrzymimi.
Cechy makroskopowe
Raki olbrzymiokomórkowe płuc często wykazują rozległą martwicę i zwyrodnienie śluzowate.
Zaobserwowano trend w kierunku mniejszego unaczynienia i gęstości tkanki (z mniejszym wzmocnieniem kontrastu w CT) w kierunku centrum tych zmian, zwłaszcza w większych guzach, a nawet w guzach bez znacznej objętości całkowitej martwicy.
Ogólnie rzecz biorąc, powierzchnie przecięcia tych nowotworów są często szarobiałe lub jasnobrązowe i często wykazują ogniska śluzowate, martwicze i/lub krwotoczne. Tego rodzaju obszary często wykazują niski poziom wzmocnienia kontrastu w komputerowej . [ potrzebne źródło ]
Zwykle obserwuje się niską otoczkę i wysoki poziom kolagenu tkankowego, z dużym wzmocnieniem kontrastu w tych obszarach.
Zaobserwowano, że GCCL rozwija się z/w pęcherzach rozedmowych .
Barwienie i immunohistochemia
Przypadek przerzutu do mózgu z raka olbrzymiokomórkowego płuca (oba „czyste”) dał wynik pozytywny dla cytokeratyn AE1 / AE3 i negatywny dla CK-7, CK-20, TTF-1 i GFAP.
Komórki GCCL często intensywnie barwią się odczynnikiem Schiffa z kwasem nadjodowym, co sugeruje obecność znacznych ilości glikogenu w cytoplazmie komórki .
Diagnostyka różnicowa
Pod mikroskopem świetlnym gigantyczne złośliwe komórki pleomorficzne tworzące GCCL przypominają komórki występujące w raku kosmówkowym , naczyniakomięsaku i niektórych postaciach prawdziwego mięsaka , takich jak złośliwy włóknisty histiocytoma i mięśniakomięsak prążkowanokomórkowy. W niektórych przypadkach mogą również wykazywać znaczne podobieństwo do „aktywowanych” histiocytów obserwowanych w niektórych stanach zapalnych .
Rzadki i potencjalnie trudny dylemat diagnostyczny różnicowy pojawia się, gdy GCCL muszą być oddzielone od raka kosmówki płucnej lub śródpiersia , co jest dla mnie krytycznym rozróżnieniem, ponieważ chociaż istnieje znany standard opieki w leczeniu raka kosmówki, jak dotąd nie ma ogólnie przyjętego standardowego leczenia dla GCCL. Dokładny przegląd morfologii komórek jest kluczem do ich określenia - podczas gdy GCCL wykazują duże zróżnicowanie rozkładu wielkości komórek i morfologii w nowotworach, rak kosmówki konsekwentnie zawiera tylko syncytiotrofoblasty i cytotrofoblasty . GCCL i pierwotny rak kosmówki płucnej można również różnicować na podstawie cech ultrastrukturalnych za pomocą mikroskopii elektronowej , chociaż EM nie ma jeszcze szerokiego zastosowania.
Czasami przerzuty GCCL do kości można potencjalnie pomylić z pierwotnym guzem olbrzymiokomórkowym kości — ten ostatni podmiot może zachowywać się jak nowotwór o łagodnym , szczerze mówiąc złośliwym lub granicznym zachowaniu klinicznym.
Miejsca przerzutów
GCCL są szczególnie godne uwagi wśród raków płuc ze względu na ich niezwykle niezwykłą skłonność do przerzutów do jelita cienkiego , czasami powodując niedrożność , ciężkie krwawienie i / lub wgłobienie jelita . Ta kliniczna cecha GCCL była obserwowana w przypadkach obejmujących ponad pół wieku.
W obrębie jelita cienkiego preferowanym miejscem przerzutów GCCL wydaje się być jelito czcze.
GCCL często daje przerzuty do kości, nadnerczy, mózgu, płuc, wątroby, nerek,
Przerzuty do mózgu z GCCL są szczególnie prawdopodobne, aby powodować znaczne krwotoki mózgowe w porównaniu z innymi wariantami raka płuc, prawdopodobnie z powodu znacznie zwiększonego tempa proliferacji śródbłonka i neowaskularyzacji, wzrostu tkanki nowotworowej, rozległej martwicy i agresywnego miejscowego naciekającego charakteru komórek GCCL.
Patogeneza
W kilku badaniach, zarówno na próbkach guza olbrzymiokomórkowego, jak i na liniach komórkowych, zidentyfikowano rearanżację i amplifikację onkogenu c -myc , czasami w połączeniu z mutacjami genu K-ras .
Wykazano, że nadekspresja czynnika wzrostu śródbłonka naczyń (VEGF) występuje w GCCL i uważa się, że jest związana z wysokim potencjałem przerzutowym tego wariantu raka płuc.
Złośliwe komórki olbrzymie identyczne z tymi występującymi w GCCL często występują w przypadkach raka płuc z wyraźnym większym lub mniejszym wzorem raka jasnokomórkowego (omówienie tego wariantu, patrz na przykład). Postawiono hipotezę, że pochodzą z niezróżnicowanego multipotentnego prekursora złośliwych komórek macierzystych , który jest generowany w dystalnych oskrzelikach za pośrednictwem nieznanego jeszcze szlaku onkogenetycznego lub czynnika onkogenetycznego .
Pod względem ultrastrukturalnym złośliwe komórki olbrzymie często zawierają nagromadzenia mikrowłókien ułożonych w spirale w pobliżu jądra komórkowego. Podmioty te wydają się podobne w strukturze do mikrofilamentów i wiązek występujących w komórkach D1 układu hormonalnego żołądkowo-jelitowo-trzustkowego i zaproponowano, że te komórki D1 mogą być nowotworowymi komórkami macierzystymi przynajmniej dla niektórych GCCL. W niektórych komórkach dróg oddechowych zwierząt po potraktowaniu rakotwórczymi nitrozoaminami wytworzono również identycznie wyglądające struktury filamentów okółkowych .
Badania ultrastrukturalne sugerują, że złośliwe komórki olbrzymie w GCCL są pochodzenia endodermalnego.
Niezwykle szybko rosnące guzy.
Nowotwory złożone/wielofazowe zawierające komórki olbrzymie
Złośliwe komórki olbrzymie są powszechnie spotykane — i różnią się względnymi proporcjami w większym lub mniejszym stopniu — zarówno w guzach pierwotnych, jak i przerzutach wielu różnych wariantów raka płuc. Wielu autorów zauważyło, że dziwaczne złośliwe komórki olbrzymie występują częściej w guzach pierwotnych i wtórnych – w tym we wszelkich pozostałych „złogach” guza – które wcześniej były leczone chemioterapią i / lub radioterapią w protokołach adiuwantowych lub neoadiuwantowych .
Charakterystyka obrazowania
GCCL często przedstawia się jako duża masa obwodowa, która jest silnie kawitowana.
W badaniu radiograficznym prawie 2000 pacjentów z rakiem płuc, opublikowanym 50 lat temu, 3,4% raków płuc okazało się być guzami kawitacyjnymi, z których większość była rakiem płaskonabłonkowym .
W wielu przypadkach ciężkiej kawitacji, wycięty guz składa się tylko z cienkiej krawędzi proliferujących komórek. [ potrzebne źródło ]
Skanowanie pozytonowej tomografii emisyjnej
Podczas skanowania pozytonowej tomografii emisyjnej (PET) stwierdzono, że GCCL ma wyjątkowo wysokie standaryzowane wartości wychwytu (SUV) radioaktywnej glukozy, wartości, które są statystycznie istotnie wyższe niż w innych histologicznych wariantach raka płuc.
Szlaki metaboliczne
Skanowanie PET sugeruje, że GCCL są nowotworami o szczególnie szybkim metabolizmie i że szlaki metaboliczne GCCL mogą być niezwykle zależne od glikolizy lub z nią powiązane .
Zespoły paranowotworowe
GCCL są od dawna znane z wydzielania podjednostki beta ludzkiej gonadotropiny kosmówkowej ( beta -HCG), często w dużych ilościach, co może prowadzić do bardzo wysokiego poziomu estrogenu i bolesnej ginekomastii (powiększenia piersi) u mężczyzn jako objawów paranowotworowych.
Olbrzymiokomórkowy rak płuc jest dobrze znany z paranowotworowej produkcji i wydzielania czynnika stymulującego tworzenie kolonii granulopoetycznych (G-CSF)
Doniesiono również, że GCCL wytwarza aktywator plazminogenu jako zjawisko paranowotworowe.
Leczenie
Ze względu na jego rzadkość nie przeprowadzono randomizowanych badań klinicznych dotyczących leczenia GCCL, a wszystkie dostępne informacje pochodzą z małych retrospektywnych serii instytucjonalnych lub metadanych wieloośrodkowych.
Rokowanie
Olbrzymiokomórkowy rak płuca od dawna uważany jest za wyjątkowo agresywny nowotwór, który rozwija się bardzo szybko i ma bardzo złe rokowanie.
Wiele małych serii sugeruje, że rokowanie w przypadku guzów płuc z komórkami olbrzymimi jest gorsze niż w przypadku większości innych postaci niedrobnokomórkowego raka płuca (NSCLC), w tym raka płaskonabłonkowego i raka wrzecionowatokomórkowego.
Ogólny wskaźnik przeżycia pięcioletniego w GCCL różni się w zależności od badania, ale ogólnie uważa się, że jest bardzo niski. Instytut Patologii Sił Zbrojnych (USA) podał liczbę 10%, aw badaniu analizującym ponad 150 000 przypadków raka płuc podano liczbę 11,8%. Jednak w tym ostatnim raporcie liczba 11,8% była oparta na danych obejmujących raka wrzecionowatokomórkowego , wariant, który ogólnie uważa się za mniej ponury niż GCCL. Dlatego prawdopodobne przeżycie „czystego” GCCL jest prawdopodobnie niższe niż podana liczba.
W dużym przeglądzie bazy danych z 1995 roku przeprowadzonym przez Travisa i współpracowników, rak olbrzymiokomórkowy ma trzecie najgorsze rokowanie wśród 18 histologicznych postaci raka płuc. (Tylko rak drobnokomórkowy i rak wielkokomórkowy miały krótszy średni czas przeżycia).
Większość GCCL już się rozrosła i zaatakowała lokalnie i/lub regionalnie i/lub dała już przerzuty odległe i są nieoperacyjne w momencie rozpoznania.
Epidemiologia
Prawdziwa częstość występowania , rozpowszechnienie i śmiertelność GCCL jest ogólnie nieznana ze względu na brak dokładnych danych dotyczących raka na poziomie krajowym. Wiadomo jednak, że jest to bardzo rzadki wariant nowotworu we wszystkich badanych populacjach. W amerykańskim badaniu bazy danych zawierającej ponad 60 000 przypadków raka płuca, GCCL stanowił od 0,3% do 0,4% pierwotnych nowotworów płuc , a współczynnik zachorowalności dostosowany do wieku wynosił około 3 nowych przypadków na milion osób rocznie. Przy około 220 000 przypadków raka płuc diagnozowanych każdego roku w Stanach Zjednoczonych , odsetek ten sugeruje, że rocznie diagnozuje się około 660 i 880 nowych przypadków u Amerykanów.
Jednak w nowszej serii 4212 kolejnych przypadków raka płuc tylko jedną (0,024%) zmianę określono jako „czysty” rak olbrzymiokomórkowy po całkowitym pocięciu całej dostępnej tkanki nowotworowej . Chociaż niektóre dowody sugerują, że GCCL mógł występować znacznie częściej kilka dekad temu, przy czym jedna seria identyfikuje 3,4% wszystkich raków płuc jako nowotwory olbrzymiokomórkowe, możliwe, że liczba ta odzwierciedla
Większość opublikowanych serii przypadków i raportów na temat raków płuca zawierających komórki olbrzymie pokazuje, że są one diagnozowane znacznie częściej u mężczyzn niż u kobiet, a niektóre badania wykazują wyjątkowo wysoki stosunek mężczyzn do kobiet (12:1 lub więcej). Jednak w badaniu obejmującym ponad 150 000 osób z rakiem płuc w USA stosunek płci wyniósł nieco ponad 2:1, przy czym kobiety miały wyższy względny odsetek raka olbrzymiokomórkowego (0,4%) niż mężczyźni (0,3%).
Zgłaszano, że raki olbrzymiokomórkowe są diagnozowane w znacznie młodszej populacji niż wszystkie raki niedrobnokomórkowe rozpatrywane jako grupa. Jednak podobnie jak prawie wszystkie raki płuc, GCC są niezwykle rzadkie u bardzo młodych ludzi: w amerykańskim SEER odnotowano tylko 2 przypadki wystąpienia u osób w wieku poniżej 30 lat w latach 1983-1987. Średni wiek w momencie rozpoznania tych nowotworów guzów oszacowano na 60 lat.
Zdecydowana większość osób z GCCL to nałogowi palacze.
Chociaż definicje „ ośrodkowego ” i „ obwodowego ” mogą się różnić w zależności od badania, GCCL są konsekwentnie diagnozowane znacznie częściej na obrzeżach płuc . W przeglądzie literatury zebranym przez Kallenburga i współpracowników mniej niż 30% GCCL powstało we wnęce lub innych częściach „centralnego” drzewa płucnego.
Postulowano również istotną predylekcję do genezy GCCL w górnych płatach pacjentów.
Historia
Większość źródeł przypisuje Nashowi i Stoutowi opublikowanie pierwszego szczegółowego raportu w literaturze medycznej uznającego GCCL za odrębną jednostkę kliniczno-patologiczną w 1958 r. Istnieją jednak pewne dowody sugerujące, że ten fenotyp nowotworu został opisany już w 1951 r. W raporcie dotyczącym 3 przypadków olbrzymiokomórkowego raka płuc opublikowanego w 1961 roku przez ZM Naiba, autor cytuje 2 wcześniejsze badania związane z GCCL — jedno opublikowane w 1951 roku przez MM Pattona i współpracowników oraz jedno opublikowane w 1955 roku przez Waltona i Pryce'a. W 1969 roku dr Alexander Kennedy w serii przypadków 3 GCCL Kennedy opublikowanej w 1969 roku przypisał Hadleyowi i Bullockowi pierwsze użycie terminu „rak olbrzymiokomórkowy” 16 lat wcześniej.
GCCL został po raz pierwszy potwierdzony jako guz nabłonkowy (a nie odróżnicowany mięsak pleomorficzny ) w 1961 r. W latach 1964–65 postulowano teorie, że GCCL są odróżnicowanymi gruczolakorakami, aw niektórych przypadkach uważano, że wywodzą się z gruczolakoraków jasnokomórkowych .
Linki zewnętrzne
- „Patologia i genetyka nowotworów płuc, opłucnej, grasicy i serca” . Klasyfikacja nowotworów Światowej Organizacji Zdrowia . Zarchiwizowane od oryginału w dniu 2015-11-15 . Źródło 2010-06-02 . (Strona pobierania).
- „Strona dotycząca raka płuc” . Narodowy Instytut Raka.