kanałowy
|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
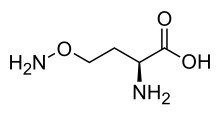
(2S ) -2-amino-4-aminooksybutanowy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Bank Leków | |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C4H10N2O3 _ _ _ _ _ _ _ | |
| Masa cząsteczkowa | 134,135 g·mol -1 |
| Gęstość | 1,298 g/ml |
| Temperatura topnienia | 213°C |
| Temperatura wrzenia | 378,1 ° C (712,6 ° F; 651,2 K) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
l -kanalina ( nazwa IUPAC: kwas 2-amino-4-(aminooksy)masłowy)) jest aminokwasem nieproteogennym . Związek ten znajduje się w roślinach strączkowych , które zawierają kanawaninę , z której jest ona wytwarzana w wyniku działania arginazy . Najczęściej stosowanym źródłem tego aminokwasu jest fasola zwyczajna, Canavalia ensiformis .
Toksyczność
l -Kanalina jest jedynym znanym naturalnie występującym aminokwasem, który ma grupę funkcyjną O - alkilohydroksyloaminy w łańcuchu bocznym. Aminokwas ten jest strukturalnie spokrewniony z ornityną (jest pochodną 5-oksa) i jest silnym środkiem owadobójczym . Larwy dzioborożca tytoniowego karmione dietą zawierającą 2,5 mM canaline wykazywały ogromne aberracje rozwojowe, a większość tak traktowanych larw umierała w stadium poczwarki. Wykazuje również silne działanie neurotoksyczne u ćmy.

Jego toksyczność wynika przede wszystkim z faktu, że łatwo tworzy oksymy z ketokwasami i aldehydami, zwłaszcza kofaktorem fosforanu pirydoksalu wielu enzymów zależnych od witaminy B6 . Hamuje aminotransferazę ornityny już przy stężeniu 10 nM.
Odżywianie roślin
l -Kanalina jest substratem dla aminotransferazy ornityny , co prowadzi do syntezy l -ureidohomoseryny (odpowiedniego analogu l -cytruliny). Ten z kolei tworzy l -kanawaninobursztynowy w reakcji, w której pośredniczy syntetaza kwasu argininobursztynowego . Kwas l -kanawaninobursztynowy jest rozszczepiany do postaci l -kanawaniny przez syntetazę kwasu argininobursztynowego. W wyniku tych kolejnych reakcji powstaje cykl kanaliczno-mocznikowy (analogicznie do cyklu ornityna-mocznik). Za każdym razem, gdy cząsteczka kanawaniny przechodzi przez cykl kanalina-mocznik, dwa końcowe atomy azotu są uwalniane jako mocznik. Mocznik jest ważnym produktem ubocznym tej sekwencji reakcji, ponieważ wytwarza amoniak amonowy (za pośrednictwem ureazy), który jest dostępny do wspomagania pośredniego metabolizmu azotu. l -kanalina może zostać rozszczepiona redukcyjnie do l - homoseryny , aminokwasu niebiałkowego o dużym znaczeniu w tworzeniu szeregu niezbędnych aminokwasów. W ten sposób trzeci atom azotu kanawaniny wchodzi w reakcje metabolizmu azotu rośliny. Jako homoseryna, jej szkielet węglowy również znajduje ważne zastosowanie.
- Rosenthal, Gerald A. (1982). Aminokwasy i iminokwasy niebiałkowe roślin: właściwości biologiczne, biochemiczne i toksykologiczne . Boston: Akademicka Prasa. ISBN 0-12-597780-8 . [ potrzebna strona ]