Clostridium tetani
|
|
| Clostridium tetani | |
|---|---|
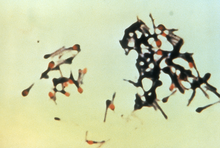
| Clostridium tetani tworzące zarodniki | |
| Klasyfikacja naukowa | |
| Domena: | Bakteria |
| Gromada: | Bacillota |
| Klasa: | Clostridia |
| Zamówienie: | eubakterie |
| Rodzina: | Clostridiaceae |
| Rodzaj: | Clostridium |
| Gatunek: |
C. tetani
|
| Nazwa dwumianowa | |
|
Clostridium tetani
Flugge , 1881
|
|
Clostridium tetani jest powszechnie występującą bakterią glebową i czynnikiem wywołującym tężec . Komórki wegetatywne Clostridium tetani mają zwykle kształt pręta i długość do 2,5 μm , ale podczas tworzenia zarodników stają się powiększone i przypominają rakietę tenisową lub pałeczkę do gry na perkusji . Zarodniki C. tetani są niezwykle odporne i można je znaleźć na całym świecie w glebie lub przewodzie pokarmowym zwierząt. Po zaszczepieniu rany C. tetani może rosnąć i wytwarzać silną toksynę, tetanospasminę , która zakłóca neurony ruchowe, powodując tężec. Działaniu toksyny można zapobiec za pomocą z toksoidem tężcowym , które często podaje się dzieciom na całym świecie.
Charakterystyka
Clostridium tetani to Gram-dodatnia bakteria w kształcie pałeczki , typowo o szerokości do 0,5 μm i długości 2,5 μm. Porusza się dzięki różnym wiciom otaczającym jego ciało. C. tetani nie może rosnąć w obecności tlenu. Najlepiej rośnie w temperaturze od 33 do 37°C.
Pod wpływem różnych warunków C. tetani może zrzucić wici i utworzyć zarodnik . Każda komórka może tworzyć pojedynczy zarodnik, zwykle na jednym końcu komórki, nadając komórce charakterystyczny kształt podudzia. C. tetani są wyjątkowo odporne na ciepło, różne środki antyseptyczne i gotowanie przez kilka minut. Zarodniki są długowieczne i występują na całym świecie w glebie, a także w jelitach różnych zwierząt gospodarskich i towarzyszących.
Ewolucja
Clostridium tetani zalicza się do rodzaju Clostridium , szerokiej grupy obejmującej ponad 150 gatunków bakterii Gram-dodatnich. C. tetani należy do grupy prawie 100 gatunków, które są ze sobą bliżej spokrewnione niż z jakimkolwiek innym rodzajem. Skupisko to obejmuje inne patogenne Clostridium , takie jak C. botulinum i C. perfringens . Najbliższym krewnym C. tetani jest C. cochlearium . Inne Clostridium można podzielić na kilka genetycznie spokrewnionych grup, z których wiele jest bliżej spokrewnionych z przedstawicielami innych rodzajów niż z C. tetani . Przykładem tego jest ludzki patogen C. difficile , który jest bliżej spokrewniony z przedstawicielami rodzaju Peptostreptococcus niż z C. tetani .
Rola w chorobie

Chociaż C. tetani jest często łagodna w glebie lub przewodzie pokarmowym zwierząt, czasami może powodować ciężką chorobę, tężec . Choroba na ogół zaczyna się od przedostania się zarodników do organizmu przez ranę. W głębokich ranach, takich jak te powstałe w wyniku nakłucia lub zanieczyszczonej igły, połączenie śmierci tkanki i ograniczonej ekspozycji na powietrze powierzchniowe może skutkować środowiskiem o bardzo niskiej zawartości tlenu, co umożliwia kiełkowanie i wzrost zarodników C. tetani . Gdy C. tetani rośnie w miejscu rany, uwalnia toksyny tetanolizynę i tetanospasminę podczas lizy komórek. Funkcja tetanolizyny jest niejasna, chociaż może pomóc C. tetani w ustaleniu infekcji w ranie. Tetanospasmina („toksyna tężcowa”) jest jedną z najsilniejszych znanych toksyn, z szacowaną śmiertelną dawką mniejszą niż 2,5 nanograma na kilogram masy ciała i jest odpowiedzialna za objawy tężca. Tetanospasmina rozprzestrzenia się przez układ limfatyczny i krwioobieg po całym ciele, gdzie jest wchłaniana do różnych części układu nerwowego . W układzie nerwowym tetanospasmina działa poprzez blokowanie uwalniania hamujących neuroprzekaźników glicyny i kwasu gamma-aminomasłowego na zakończeniach nerwów ruchowych . Ta blokada prowadzi do powszechnej aktywacji neuronów ruchowych i skurczów mięśni w całym ciele. Te skurcze mięśni zwykle zaczynają się od górnej części ciała i przesuwają się w dół, rozpoczynając się około 8 dni po zakażeniu szczękościskiem , po czym następują skurcze mięśni brzucha i kończyn. Skurcze mięśni utrzymują się przez kilka tygodni.
Gen kodujący tetanospasminę znajduje się na plazmidzie przenoszonym przez wiele szczepów C. tetani ; szczepy bakterii pozbawione plazmidu nie są w stanie wytwarzać toksyny. Funkcja tetanospasminy w fizjologii bakterii jest nieznana.
Leczenie i profilaktyka
Clostridium tetani jest wrażliwe na wiele antybiotyków , w tym chloramfenikol , klindamycynę , erytromycynę , penicylinę G i tetracyklinę . Jednak przydatność leczenia C. tetani antybiotykami pozostaje niejasna. Zamiast tego tężec jest często leczony immunoglobuliną przeciwtężcową w celu związania krążącej tetanospasminy. Dodatkowo benzodiazepiny lub środki zwiotczające mięśnie w celu zmniejszenia skutków skurczów mięśni.
Uszkodzeniom spowodowanym infekcją C. tetani można na ogół zapobiegać przez podawanie szczepionki przeciw tężcowi składającej się z tetanospasminy inaktywowanej formaldehydem , zwanej toksoidem tężcowym. Jest to wytwarzane komercyjnie poprzez hodowanie dużych ilości C. tetani w fermentorach , a następnie oczyszczanie toksyny i inaktywację w 40% formaldehydzie przez 4-6 tygodni. Toksoid jest na ogół podawany jednocześnie z anatoksyną błoniczą i pewną postacią szczepionki przeciw krztuścowi, jak szczepionka DPT lub DTaP . Podaje się go w kilku dawkach rozłożonych w ciągu miesięcy lub lat, aby wywołać odpowiedź immunologiczną, która chroni gospodarza przed działaniem toksyny.
Badania
Clostridium tetani można hodować na różnych podłożach beztlenowych , takich jak podłoża tioglikolanowe , podłoża z hydrolizatem kazeiny i agar z krwią . Kultury rosną szczególnie dobrze na pożywkach o pH od obojętnego do zasadowego, uzupełnionych czynnikami redukującymi . Genom C. tetani został zsekwencjonowany i zawiera 2,80 miliona par zasad z 2373 genami kodującymi białka.
Historia
związanego z ranami można znaleźć co najmniej w IV wieku pne w Aforyzmach Hipokratesa . Pierwsze wyraźne powiązanie z glebą miało miejsce w 1884 r., kiedy Arthur Nicolaier wykazał, że u zwierząt, którym wstrzyknięto próbki gleby, rozwinie się tężec. W 1889 r. Kitasato Shibasaburō wyizolował C. tetani z ludzkiej ofiary , który później wykazał, że organizm ten może wywoływać choroby po wstrzyknięciu zwierzętom oraz że toksyna może zostać zneutralizowana przez specyficzne przeciwciała . W 1897 roku Edmond Nocard wykazał, że antytoksyna tężcowa indukuje bierną odporność u ludzi i może być stosowana w profilaktyce i leczeniu. Podczas I wojny światowej wstrzykiwanie surowicy odpornościowej przeciw tężcowi z koni było szeroko stosowane jako profilaktyka tężca u rannych żołnierzy, co doprowadziło do dramatycznego spadku zachorowań na tężec w trakcie wojny. Nowoczesną metodę inaktywacji toksyny tężcowej za pomocą formaldehydu opracował Gaston Ramon w latach dwudziestych XX wieku; doprowadziło to do opracowania przez P. Descombeya w 1924 r. szczepionki z anatoksyną tężcową, która była szeroko stosowana w zapobieganiu tężcowi wywołanemu ranami bojowymi podczas II wojny światowej.
