Diglime
|
|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
1-Metoksy-2-(2-metoksyetoksy)etan |
|
| Inne nazwy Diglyme Eter 2-metoksyetylowy Eter di(2-metoksyetylowy) Eter dimetylowy glikolu dietylenowego |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 1736101 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Bank Leków | |
| Karta informacyjna ECHA | 100.003.568 |
| Numer WE |
|
| 26843 | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS |
|
| UNII | |
| Numer ONZ | 2252 1993 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C6H14O3 _ _ _ _ _ | |
| Masa cząsteczkowa | 134,175 g/mol |
| Gęstość | 0,937 g/ml |
| Temperatura topnienia | -64 ° C (-83 ° F; 209 K) |
| Temperatura wrzenia | 162 ° C (324 ° F; 435 K) |
| Mieszalny | |
| Zagrożenia | |
| Oznakowanie GHS : | |
 
|
|
| Niebezpieczeństwo | |
| H226 , H360 | |
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P280 , P281 , P303+P361+P353 , P308+P313 , P370+P378 , P403+P235 , P405 , P501 | |
| Punkt zapłonu | 57 ° C (135 ° F; 330 K) |
| Związki pokrewne | |
|
Związki pokrewne
|
Eter dietylowy glikolu dietylenowego , eter dimetylowy glikolu etylenowego |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Diglyme , czyli eter bis(2-metoksyetylowy), jest rozpuszczalnikiem o wysokiej temperaturze wrzenia . Jest związkiem organicznym będącym eterem dimetylowym glikolu dietylenowego . (Nazwa diglyme to połączenie eteru col . ) eter . metylowego digly Jest to bezbarwna ciecz o lekkim zapachu przypominającym Jest mieszalny z wodą i rozpuszczalnikami organicznymi.
Otrzymuje się go w reakcji eteru dimetylowego i tlenku etylenu na kwaśnym katalizatorze.
Rozpuszczalnik
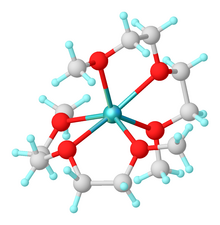
Ze względu na swoją odporność na silne zasady, diglyme jest preferowanym rozpuszczalnikiem w reakcjach odczynników z metalami alkalicznymi, nawet w wysokich temperaturach. Podczas stosowania diglymu jako rozpuszczalnika obserwowano przyspieszenie reakcji z udziałem odczynników metaloorganicznych , takich jak reakcje Grignarda lub redukcje wodorkami metali.
Diglyme jest również stosowany jako rozpuszczalnik w reakcjach hydroborowania z diboranem .
Pełni rolę chelatu dla kationów metali alkalicznych , pozostawiając bardziej aktywne aniony .
Bezpieczeństwo
Europejska Agencja Chemikaliów wymienia diglym jako substancję wzbudzającą szczególnie duże obawy (SVHC) jako toksynę reprodukcyjną.
Wiadomo, że w wyższych temperaturach iw obecności aktywnych metali diglym ulega rozkładowi, co może powodować wytwarzanie dużych ilości gazu i ciepła. Ten rozkład doprowadził do wybuchu reaktora T2 Laboratories w 2007 roku.
- ^ Nomenklatura chemii organicznej: zalecenia IUPAC i preferowane nazwy 2013 (Blue Book) . Cambridge: Królewskie Towarzystwo Chemii . 2014. s. 704. doi : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- Bibliografia _ Dietera Mayera. "Glikol etylenowy". Encyklopedia chemii przemysłowej Ullmanna . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a10_101 .
-
^
S. Neander, J. Kornich, F. Olbrich (2002). „Nowe kompleksy fluorenylu metali alkalicznych DIGLYME: synteza i struktury ciała stałego”. J. Organomet. chemia . 656 (1–2): 89. doi : 10.1016/S0022-328X(02)01563-2 .
{{ cite journal }}: CS1 maint: używa parametru autorów ( link ) -
^
JE Ellis, A. Davison (1976). „Tris [bis (2-metoksyetylo) eter] potas i tetrafenylarsonium heksakarbonylometalany (1-) niobu i tantalu”. Tris[bis(2-metoksyetylo)eter]potasu i tetrafenylarsonium heksakarbonylometalany(1–) niobu i tantalu . Inorg. Syntezator . Syntezy nieorganiczne. Tom. 16. s. 68–73. doi : 10.1002/9780470132470.ch21 . ISBN 9780470132470 .
{{ cite book }}: CS1 maint: używa parametru autorów ( link ) -
^
JE Siggins, AA Larsen, JH Ackerman, CD Carabateas (1973). „3,5-dinitrobenzaldehyd”. Syntezy organiczne . 53 : 52. doi : 10.15227/orgsyn.053.0052 .
{{ cite journal }}: CS1 maint: używa parametru autorów ( link ) -
^
Michael W. Rathke, Alan A. Millard (1978). „Borany w funkcjonalizacji olefin do amin: 3-pinanamina”. Syntezy organiczne . 58:32 . doi : 10.15227/orgsyn.058.0032 .
{{ cite journal }}: CS1 maint: używa parametru autorów ( link ) -
^
Ei-ichi Negishi, Herbert C. Brown (1983). „Perhydro-9b-borafenalen i perhydro-9b-fenalenol”. Syntezy organiczne . 61 : 103. doi : 10.15227/orgsyn.061.0103 .
{{ cite journal }}: CS1 maint: używa parametru autorów ( link ) - ^ „Włączenie substancji wzbudzających szczególnie duże obawy do listy kandydackiej (decyzja Europejskiej Agencji Chemikaliów)” . 19 grudnia 2011 r.
- ^ Pitt, Martin J. (12 lipca 2010). „Bezpieczeństwo chemiczne: niebezpieczeństwa Diglyme” . cen.acs.org . Zarchiwizowane od oryginału w dniu 11.05.2012 . Źródło 2021-09-01 .
- ^ Willey, Ronald J.; Fogler, H. Scott; Cutlip, Michael B. (marzec 2011). „Włączenie bezpieczeństwa procesowego do kursu inżynierii reakcji chemicznych: Modelowanie kinetyczne incydentu T2” . Postęp w zakresie bezpieczeństwa procesowego . 30 (1): 39–44. doi : 10.1002/prs.10431 . hdl : 2027.42/83180 . S2CID 109207593 .