Pentafluorek chlorku siarki
|
|
|||
| Nazwy | |||
|---|---|---|---|
| Inne nazwy Pentafluorochlorosulfanyl
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.034.014 | ||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| SF 5 kl | |||
| Masa cząsteczkowa | 162,510 g/mol | ||
| Wygląd | Bezbarwny gaz | ||
| Gęstość | 6,642 g/dm 3 | ||
| Temperatura topnienia | -64 ° C (-83 ° F; 209 K) | ||
| Temperatura wrzenia | -19 ° C (-2 ° F; 254 K) | ||
| Zagrożenia | |||
| Bezpieczeństwo i higiena pracy (BHP): | |||
|
Główne zagrożenia
|
Toksyczny | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
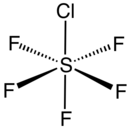
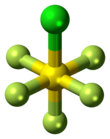
Pentafluorek chlorku siarki jest związkiem nieorganicznym o wzorze SF 5 Cl . Występuje jako bezbarwny gaz w temperaturze pokojowej i jest wysoce toksyczny, podobnie jak większość związków nieorganicznych zawierających grupę funkcyjną pentafluorosiarczku (– SF 5 ). Związek przyjmuje geometrię oktaedryczną z
symetrią C4v . Pentafluorek chlorku siarki jest jedynym dostępnym na rynku odczynnikiem do dodawania –SF 5 do związków organicznych.
Reaktywność
SF 5 Cl jest wysoce reaktywny i toksyczny. W przeciwieństwie do tego sześciofluorek siarki ( SF 6 ) jest obojętny i nietoksyczny, mimo że ma blisko spokrewniony wzór chemiczny. Ta różnica podkreśla labilność wiązania S – Cl w SF 5 Cl .
W warunkach wolnorodnikowych SF 5 Cl dodaje się poprzez podwójne wiązania. Z propenem zachodzi następująca reakcja :
-
CH
3 CH=CH
2 + SF
5 Cl → CH 3 CHClCH 2 SF 5
Reakcja addycji jest katalizowana przez (CH 3 CH 2 ) 3 B w temperaturze około -30 °C. Podobnie stosuje się SF 5 Br .
SF 5 Cl jest także prekursorem O(SF 5 ) 2 i F 2 NSF 5 (z tetrafluorohydrazyny ).
Synteza
Chloropentafluorek siarki można zsyntetyzować kilkoma drogami, zaczynając od dwóch niższych fluorków siarki, tetrafluorku siarki i dekafluorku disiarki :
-
SF
4 + Cl
2 + CsF → SF
5 Cl + CsCl -
ClF + SF
4 → SF
5 Cl -
S
2 F
10 + Cl
2 → 2 SF
5 Cl
Odpowiedni SF5Br wytwarza się podobnie
z monofluorku bromu generowanego in situ .