Selenol
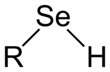
Selenole są związkami organicznymi , które zawierają grupę funkcyjną o połączeniu C– Se –H. Selenole są czasami nazywane także selenomerkaptanami i selenotiolami . Selenole są jedną z głównych klas związków selenoorganicznych . Najbardziej znanym przedstawicielem tej grupy jest aminokwas selenocysteina .
Struktura, wiązanie, właściwości
Selenole są strukturalnie podobne do tioli , ale wiązanie C-Se jest o około 8% dłuższe przy 196 pm. Kąt C–Se–H zbliża się do 90°. Wiązanie obejmuje prawie czyste p-orbitale na Se, stąd blisko 90 kątów. Energia wiązania Se–H jest słabsza niż wiązania S–H, w związku z czym selenole łatwo ulegają utlenieniu i służą jako donory atomów H. Wiązanie Se-H jest znacznie słabsze niż wiązanie SH, co znajduje odzwierciedlenie w odpowiedniej energii dysocjacji wiązania (BDE). Dla C 6 H 5 Se-H BDE wynosi 326 kJ/mol, podczas gdy dla C 6 H 5 SH BDE wynosi 368 kJ/mol.
1000 razy silniejsze niż tiole: p Ka CH3SeH wynosi 5,2 w porównaniu z 8,3 dla CH3SH . Deprotonowanie daje anion selenolanowy , RSe - , którego większość przykładów jest wysoce nukleofilowa i szybko utlenia się powietrzem.
Temperatury wrzenia selenoli są zwykle nieco wyższe niż tioli. Można to przypisać zwiększonemu znaczeniu silniejszych wiązań van der Waalsa dla większych atomów. Lotne selenole mają bardzo odrażający zapach.
Zastosowania i występowanie
Selenole mają niewiele zastosowań komercyjnych, ponieważ są ograniczone wysoką toksycznością selenu, a także wrażliwością wiązania Se – H. Ich sprzężone zasady , selenolany, mają ograniczone zastosowanie w syntezie organicznej .

Rola biochemiczna
Selenole są ważne w niektórych procesach biologicznych. Trzy enzymy występujące u ssaków zawierają selenole w swoich miejscach aktywnych: peroksydaza glutationowa , dejodynaza jodotyroniny i reduktaza tioredoksyny . Selenole w tych białkach są częścią niezbędnego aminokwasu selenocysteiny . Selenole działają jako środki redukujące, dając kwasu selenowego (RSe – OH), która z kolei jest ponownie redukowana przez enzymy zawierające grupę tiolową. Metaselenol (powszechnie nazywany „metyloselenolem”) (CH 3 SeH), który można wytworzyć in vitro przez inkubację selenometioniny z bakteryjnym enzymem gamma-liazą metioninową (METaza), przez biologiczną metylację jonu selenku lub in vivo przez redukcję kwasu metanoseleninowego (CH 3 SeO 2 H), został przywołany do wyjaśnić działanie przeciwnowotworowe niektórych związków selenoorganicznych. Prekursory metaneselenolu są aktywnie badane w profilaktyce i terapii raka. W badaniach tych stwierdzono, że metaneselenol jest bardziej aktywny biologicznie niż etanoselenol czy 2-propaneselenol.
Przygotowanie
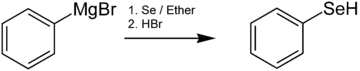
Selenole są zwykle przygotowywane w reakcji odczynników litoorganicznych lub odczynników Grignarda z pierwiastkowym Se. Na przykład benzeneselenol powstaje w reakcji bromku fenylomagnezu z selenem, po której następuje zakwaszenie:
Inna droga preparatywna do selenoli obejmuje alkilowanie selenomocznika , a następnie hydrolizę. Selenole są często generowane przez redukcję diselenków, po której następuje protonowanie powstałego selenianu:
- 2 RSeSeR + 2 LiHB(C 2 H 5 ) 3 → 2 RSeLi + 2 B(C 2 H 5 ) 3 + H 2
- RSeLi + HCl → RSeH + LiCl
Diselenek dimetylu można łatwo zredukować do metaneselenolu w komórkach.
Reakcje
Selenole łatwo utleniają się do diselenków, związków zawierających wiązanie Se-Se. Na przykład traktowanie benzeneselenolu bromem daje diselenek difenylu .
- 2 C 6 H 5 SeH + Br 2 → (C 6 H 5 Se) 2 + 2 HBr
W obecności zasady selenole łatwo ulegają alkilowaniu dając selenki. Zależność tę ilustruje metylacja metaneselenolu z wytworzeniem selenku dimetylu .
Bezpieczeństwo
Związki selenoorganiczne (lub jakikolwiek związek selenu) są truciznami kumulacyjnymi, mimo że śladowe ilości Se są potrzebne dla zdrowia.