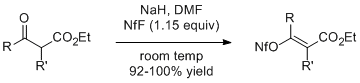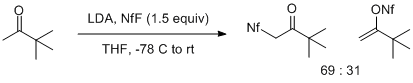Fluorek perfluorobutanosulfonylu

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
fluorek 1,1,2,2,3,3,4,4,4-nonafluorobutano-1-sulfonylu |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| Skróty | NfF |
| ChemSpider | |
| Karta informacyjna ECHA | 100.006.175 |
| Numer WE |
|
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 4 F 10 O 2 S | |
| Masa cząsteczkowa | 302,09 g/mol |
| Gęstość | 1,682 g/ml |
| Temperatura topnienia | < -120 ° C (-184 ° F; 153 K) |
| Temperatura wrzenia | 65 do 66 ° C (149 do 151 ° F; 338 do 339 K) |
| Związki pokrewne | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Fluorek perfluorobutanosulfonylu (fluorek nonafluorobutanosulfonylu, NfF) jest bezbarwną, lotną cieczą, która nie miesza się z wodą, ale rozpuszcza się w zwykłych rozpuszczalnikach organicznych. Jest przygotowywany przez elektrochemiczne fluorowanie sulfolanu . NfF służy jako punkt wejścia do nonafluorobutanosulfonianów ( nonaflates ), które są cenne jako elektrofile w katalizowanych palladem reakcjach sprzęgania krzyżowego . Jako środek perfluoroalkilosulfonylujący, NfF oferuje zalety niższego kosztu i większej stabilności w porównaniu z częściej stosowanym bezwodnikiem trifluorometanosulfonowym . Fluorkowa grupa opuszczająca jest łatwo zastępowana przez nukleofile, takie jak aminy , fenolany i enolany , dając odpowiednio sulfonamidy, nonaflaty arylu i nonaflaty alkenylu. Nie jest jednak atakowany przez wodę (w której jest stabilny przy pH<12). Hydroliza wodorotlenkiem baru daje Ba(ONf) 2 , który po potraktowaniu kwasem siarkowym daje kwas perfluorobutanosulfonowy i nierozpuszczalny siarczan baru .
Oczyszczenie
Dostępny w handlu NfF jest zanieczyszczony 6-10% molowych perfluorosulfolanu pochodzącego z jego produkcji. Można to łatwo usunąć przez energiczne mieszanie materiału handlowego ze stężonym wodnym roztworem K 3 PO 4 i K 2 HPO 4 w stosunku molowym 1:1 przez 96 godzin. Ta obróbka, po której następuje usunięcie warstwy wodnej i destylacja z P2O5 , daje produkt, który zawiera >99% molowych NfF z niemal ilościowym odzyskiem .
Synteza nonaflatów arylowych i alkenylowych
Jak wspomniano powyżej, nonaflaty arylowe i alkenylowe są przydatne jako elektrofile w katalizowanych palladem reakcjach sprzęgania krzyżowego. Ich reaktywność generalnie odzwierciedla reaktywność częściej spotykanych elektrofilów triflatowych, ale nonaflaty są mniej podatne na hydrolizę do ketonów (w przypadku alkenylosulfonianów) i fenoli (w przypadku arylosulfonianów). Ich odporność na hydrolizę sprawia, że nonflaty są lepszymi elektrofilami w sprzężeniach Buchwalda-Hartwiga, gdzie ta reakcja uboczna może być szkodliwa dla wydajności pożądanego produktu.
Enolany sodu β-ketoestrów reagują z 1,15 równoważnika NfF, dając z wysoką wydajnością odpowiednie nonaflaty alkenylowe. Tą metodą otrzymuje się geometrycznie czysty izomer E z 2-metyloacetylooctanu etylu (R=R'=Me).
Proste aldehydy i ketony reagują z NfF w obecności zasad, takich jak DBU lub fosfazeny, dając alkenylowe nonaflaty z dużą wydajnością bez tworzenia odrębnego enolanu. Stosowanie zasady fosfazenu P2 w temperaturze od -30 do -20°C daje mniej podstawiony alkenylononaflan z niesymetrycznie podstawionymi ketonami. Podobne reakcje z bezwodnikiem trifluorometanosulfonowym na ogół wymagają zastosowania drogiej 2,6-di- tert -butylopirydyny w celu uzyskania wysokich wydajności.
Reakcja enolanów z NfF silnie zależy zarówno od struktury enolanu, jak i jego przeciwjonu metalu. Enolany litu ketonów metylowych dają mieszaniny produktów pochodzących z elektrofilowego ataku na atomy O (oczekiwany) lub C (nieoczekiwany) enolanu. Efekt ten jest szczególnie widoczny w przypadku enolanu litu pinakolonu, który daje mieszaninę 2:1 sprzyjającą atakowi C. Bardziej podstawione enolany litu dają tylko produkty O-sulfonylowania ze zmienną wydajnością.
Etery trimetylosililoenolowe reagują z NfF w obecności podstechiometrycznego źródła fluorku w temperaturze od 0 ° C do temperatury otoczenia, dając alkenylowe nonaflaty z wydajnością od umiarkowanej do dobrej. Suszone Bu 4 F było preferowanym źródłem fluoru w jednym badaniu, ale CsF stosowano w trudnych przypadkach z doskonałymi wynikami.
Nonaflaty arylowe można otrzymać bezpośrednio z fenoli i NfF w obecności zasad, takich jak węglan Et3N , potasu i z wydajnością zbliżoną do ilościowej. Można również stosować mocniejsze zasady, takie jak NaH i BuLi , ale mają one tendencję do dawania nieco niższych wydajności.
Reakcje z alkoholami
Reakcja NfF z alkoholami uwidacznia labilność nonaflatów alkilowych – w większości przypadków końcowym produktem reakcji jest albo fluorek alkilu (z F – atak na nonaflat alkilowy), albo olefina (z eliminacji NfOH z półproduktu nonflat).
Synteza bis -nonafluorobutanosulfonimidu (Nf 2 NH)
NfF reaguje z chlorkiem amonu w obecności trietyloaminy w acetonitrylu, dając sól trietyloamoniową superkwasowego bis -nonafluorobutanosulfonimidu z wydajnością 97%. Odpowiednią sól potasową otrzymuje się przez traktowanie metanolowego roztworu soli trietyloamoniowej KOH . Kwas otrzymuje się metodą chromatografii jonowymiennej soli trietyloamoniowej z Amberlite IR-100 jako fazą stacjonarną i metanolem jako eluentem. Rzeczywiste związki wytworzone w tej ostatniej procedurze to prawdopodobnie MeOH 2 + Nf 2 N- . _