Oksydaza piranozowa
| oksydazy piranozowej | |||||||||
|---|---|---|---|---|---|---|---|---|---|
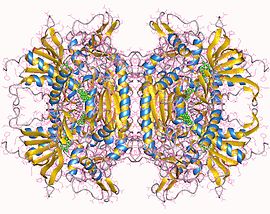 , Trametes ochracea
| |||||||||
| Identyfikatory | |||||||||
| nr WE | 1.1.3.10 | ||||||||
| Nr CAS | 37250-80-9 | ||||||||
| Bazy danych | |||||||||
| IntEnz | Widok IntEnz | ||||||||
| BRENDA | Wpis BRENDY | ||||||||
| EXPASY | Widok NiceZyme | ||||||||
| KEGG | Wpis KEGG | ||||||||
| MetaCyc | szlak metaboliczny | ||||||||
| PRYAM | profil | ||||||||
| Struktury WPD | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia genów | AmiGO / QuickGO | ||||||||
| |||||||||
W enzymologii oksydaza piranozowa ( EC 1.1.3.10 ) jest enzymem katalizującym reakcję chemiczną
- D-glukoza + O 2 2-dehydro-D-glukoza + H 2 O 2
Zatem dwoma substratami tego enzymu są D produktami H2O2 . -glukoza i O2 , 2 podczas gdy jego dwoma są -dehydro-D- glukoza i
Oksydaza piranozowa jest zdolna do utleniania D-ksylozy , L-sorbozy , D-galaktozy i D-glukono-1,5-laktonu , które mają tę samą konformację i konfigurację pierścienia przy C-2, C-3 i C-4.
Enzym ten należy do rodziny oksydoreduktaz , w szczególności tych działających na grupę CH-OH donora z tlenem jako akceptorem. Systematyczna nazwa tej klasy enzymów to 2-oksydoreduktaza piranoza:tlen . Inne powszechnie używane nazwy obejmują 2-oksydazę glukozową i 2-oksydazę piranozową . Enzym ten uczestniczy w szlaku pentozofosforanowym . Wykorzystuje jeden kofaktor , FAD .
Badania strukturalne
Pod koniec 2007 r. rozwiązano 8 struktur dla tej klasy enzymów, z kodami dostępu PDB 1TT0 , 1TZL , 2F5V , 2F6C , 2IGK , 2IGM , 2IGN i 2IGO .
Zastosowanie w biosensorach
Ostatnio oksydaza piranozowa zyskuje na popularności w biosensorach. W przeciwieństwie do oksydazy glukozowej może wytwarzać większą moc wyjściową, biorąc pod uwagę, że nie jest glikozylowana, ma korzystniejszą wartość stałych Michaelisa-Mentena i może katalitycznie przekształcać oba anomery glukozy. Reaguje z szerszą gamą podłoży. Oksydaza piranozowa nie powoduje niepożądanej zmiany pH. Możliwe jest również łatwe jego wyrażanie i wytwarzanie z dużą wydajnością przy użyciu E. coli .
Dalsza lektura
- Machida Y., Nakanishi T. (1984). „Oczyszczanie i właściwości oksydazy piranozowej z Coriolus versicolor” . Chemia Rolnicza i Biologiczna . 48 (10): 2463–2470. doi : 10.1271/bbb1961.48.2463 .
- Neidleman SL, Amon Jr WF, Geigert J (1981). „Proces produkcji fruktozy”. Chem. Streszczenie _ 94 : 20737.
- Ruelius HW, Kerwin RM, Janssen FW (listopad 1968). „Oksydaza węglowodanowa, nowy enzym z Polyporus obtusus. I. Izolacja i oczyszczanie”. Biochimica et Biophysica Acta (BBA) - Enzymologia . 167 (3): 493–500. doi : 10.1016/0005-2744(68)90039-9 . PMID 5725162 .
