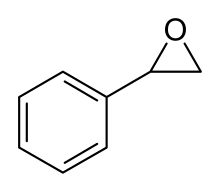
Tlenek styrenu
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
fenyloksiran |
|
| Inne nazwy epoksystyren; tlenek styrylu; Tlenek fenyloetylenu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 108582 | |
| CHEBI | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.002.252 |
| Numer WE |
|
| 50213 | |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS |
|
| UNII | |
| Numer ONZ | 2810 3082 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 8 H 8 O | |
| Masa cząsteczkowa | 120,151 g·mol -1 |
| Wygląd | Bezbarwna do jasnożółtej ciecz |
| Gęstość | 1,052 g/ml |
| Temperatura topnienia | -37 ° C (-35 ° F; 236 K) |
| Temperatura wrzenia | 194 ° C (381 ° F; 467 K) |
| Zagrożenia | |
| Oznakowanie GHS : | |
 
|
|
| Niebezpieczeństwo | |
| H312 , H319 , H350 | |
| P201 , P202 , P264 , P280 , P281 , P302+P352 , P305+P351+P338 , P308+P313 , P312 , P322 , P337+P313 , P363 , P405 , P501 | |
| Karta charakterystyki (SDS) | MSDS Uniwersytetu Oksfordzkiego |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Tlenek styrenu to epoksyd pochodzący ze styrenu . Można go otrzymać przez epoksydowanie styrenu kwasem nadbenzoesowym w reakcji Prilezhaeva :
Tlenek styrenu jest słabo rozpuszczalny w wodzie. Śladowe ilości kwasu w wodzie powodują hydrolizę do racemicznego glikolu fenyloetylenowego poprzez kation benzylowy. Jeśli ilość wody nie jest wystarczająca, nastąpi katalizowana kwasami izomeryzacja fenyloacetaldehydu .
Tlenek styrenu w organizmie jest metabolizowany do kwasu migdałowego , kwasu fenyloglioksylowego , kwasu benzoesowego i kwasu hipurowego .
Uwodornienie tlenku styrenu daje alkohol fenetylowy .
Stereospecyficzne reakcje
Ponieważ tlenek styrenu ma centrum chiralne na benzylowym atomie węgla, istnieją ( R )-tlenek styrenu i ( S )-tlenek styrenu. Jeśli zastosuje się optycznie czysty odczynnik, otrzyma się tylko jeden optycznie czysty związek.
Toksykologia
Tlenek styrenu jest głównym metabolitem styrenu u ludzi i zwierząt, powstającym w wyniku utleniania przez cytochrom P450 . Uważa się, że może być rakotwórczy po wstrzyknięciu znacznych ilości myszom i szczurom. Tlenek styrenu jest następnie hydrolizowany in vivo do glikolu styrenowego przez hydrolazę epoksydową .
Tlenek styrenu ma centrum chiralne , a więc dwa enancjomery . Istnieją doniesienia, że oba enancjomery mają różną toksykokinetykę i toksyczność [ potrzebne źródło ] . Doniesiono, że tlenek ( R )-styrenu był tworzony preferencyjnie u myszy, zwłaszcza w płucach, podczas gdy tlenek ( S )-styrenu był preferencyjnie generowany u szczurów. U ochotników skumulowane wydalanie ( S )-enancjomeru glikolu styrenowego i kwasu migdałowego było większe niż R tworzą się po ekspozycji na styren. W mikrosomach ludzkiej wątroby utlenianie styrenu za pośrednictwem cytochromu P450 wykazało wytwarzanie większej ilości enancjomeru S w stosunku do enancjomeru R. Stwierdzono również, że tlenek ( S )-styrenu był preferencyjnie hydrolizowany niż enancjomer R w mikrosomach ludzkiej wątroby. Badania na zwierzętach wykazały, że ( R )-enancjomer tlenku styrenu był bardziej toksyczny niż ( S )-enancjomer u myszy.
