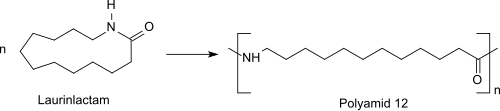
laurolaktam

|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
Azacyklotridekan-2-on
|
|
| Inne nazwy Dodekalaktam
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA | 100.012.204 |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C12H23NO _ _ _ _ _ | |
| Masa cząsteczkowa | 197,322 g·mol -1 |
| Wygląd | bezbarwne ciało stałe |
| Temperatura topnienia | 152,5 ° C (306,5 ° F; 425,6 K) |
| Temperatura wrzenia | 314,9±10°C |
| 0,03% wag. | |
| Zagrożenia | |
| Punkt zapłonu | 192 ° C (378 ° F; 465 K) |
| 320 do 330 ° C (608 do 626 ° F; 593 do 603 K) | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Laurolaktam jest związkiem organicznym z grupy makrocyklicznych laktamów . Laurolaktam jest stosowany głównie jako monomer w konstrukcyjnych tworzywach sztucznych , takich jak nylon-12 i kopoliamidy.
Synteza
Chociaż jest pochodną kwasu 12-aminododekanowego , jest wytwarzany z cyklododekatrienu . Trien uwodornia się do nasyconego alkanu, cyklododekanu . Do produkcji laurolaktamu cyklododekan utlenia się powietrzem lub tlenem w obecności kwasu borowego i soli metali przejściowych (np. octanu kobaltu(II) ), otrzymując mieszaninę cyklododekanolu i cyklododekanonu . Ta mieszanina jest ilościowo odwodorniana na miedzianym katalizatorze kontaktowym do cyklododekanonu i poddawana jest reakcji hydroksyloaminy do oksymu cyklododekanonu. Oksym jest przegrupowany do laurolaktamu w przegrupowaniu Beckmanna w obecności mocnego kwasu.
Alternatywnym procesem jest fotonitrozowanie cyklododekanu chlorkiem nitrozylu w obecności bezwodnego chlorowodoru . Powstały oksym cyklododekanonu ekstrahuje się stężonym kwasem siarkowym i przekształca w laurolaktam przez ogrzewanie do 160°C. Całkowita wydajność (fotoazotowanie + przegrupowanie Beckmanna) wynosi do 93%.
Nieruchomości
Laurolaktam jest nierozpuszczalnym w wodzie, krystalicznym ciałem stałym; w jakości technicznej zwykle w kolorze beżowym, aw stanie czystym (czystość 99,9%) w kolorze białym. Jest rozpuszczalny w wielu rozpuszczalnikach organicznych, np. 1,4-dioksanie , benzenie czy cykloheksanie . Proces oczyszczania prowadzi się konwencjonalnie przez wieloetapową destylację pod zmniejszonym ciśnieniem. Połączenie destylacji i krystalizacji z roztworu lub stopu daje bardzo czysty laurolaktam (> 99%). Ryzyko stwarzane przez laurolaktam jest uważane za niskie.
Używa
Polimeryzację z otwarciem pierścienia stosuje się do polimeryzacji monomeru do nylonu-12 . Reakcję można prowadzić za pomocą inicjatorów kationowych lub anionowych albo za pomocą wody. Uważa się, że polimeryzacja kationowa z kwasem obejmuje początkowe O-protonowanie. Atak nukleofilowy monomeru na reaktywny protonowany azot, po którym następuje kolejne acylowanie pierwszorzędowej aminy z otwarciem pierścienia, prowadzi do powstania poliamidu. Polimeryzacja z otwarciem pierścienia monomeru laurynolaktamu początkowo przebiega po dodaniu wody w prepolimeryzacji w około 300 ° C pod ciśnieniem do prepolimeru . Ten prepolimer poddaje się reakcji w późniejszej polikondensacji pod ciśnieniem otoczenia lub obniżonym iw temperaturze około 250°C do poliamidu 12 o wyższej masie cząsteczkowej (PA 12: -[NH-(CH 2 ) 11 -CO] n- ).
Jako komonomer laurolaktam jest stosowany razem z ε-kaprolaktamem do wytwarzania kopoliamidu 6/12.