2-Metylopirydyna
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2-Metylopirydyna |
|||
| Inne nazwy 2-Pikolina
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CHEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.003.313 | ||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 6 H 7 N | |||
| Masa cząsteczkowa | 93,13 g/mol | ||
| Wygląd | Lekko żółtozielona przezroczysta ciecz | ||
| Gęstość | 0,943 g/ml | ||
| Temperatura topnienia | -70 ° C (-94 ° F; 203 K) | ||
| Temperatura wrzenia | 128 do 129 ° C (262 do 264 ° F; 401 do 402 K) | ||
| Mieszalny | |||
| -60,3· 10-6 cm3 / mol | |||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
2-Metylopirydyna lub 2-pikolina jest związkiem opisanym wzorem C 6 H 7 N. 2-Pikolina jest bezbarwną cieczą o nieprzyjemnym zapachu podobnym do pirydyny . Stosowany jest głównie do produkcji winylopirydyny i agrochemicznej nitrapiryny .
Synteza
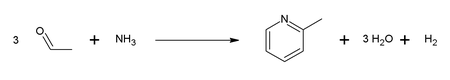
2-Pikolina była pierwszym związkiem pirydyny , który został wyizolowany w czystej postaci. Został wyizolowany ze smoły węglowej w 1846 roku przez T. Andersona. Ta chemia była praktykowana przez Reilly Industries. Obecnie jest produkowany głównie dwoma głównymi trasami. Jedna metoda obejmuje kondensację aldehydu octowego i amoniaku w obecności katalizatora tlenkowego. Ta metoda daje mieszaninę 2- i 4-pikolin:
Inna metoda polega na kondensacji acetonu i akrylonitrylu z wytworzeniem 5-oksoheksanonitrylu, który następnie cyklizuje, dając 2-pikolinę. W 1989 roku na całym świecie wyprodukowano około 8000 ton rocznie.
Reakcje
Większość reakcji pikoliny koncentruje się na grupie metylowej. Na przykład, głównym zastosowaniem 2-pikoliny jest prekursor 2-winylopirydyny . Konwersję uzyskuje się przez kondensację z formaldehydem :
Kopolimer 2-winylopirydyny, butadienu i styrenu jest stosowany jako klej do tekstylnego kordu opony. 2-Pikolina jest także prekursorem związku agrochemicznego, nitrapiryny , która zapobiega utracie amoniaku z nawozów. Utlenianie nadmanganianem potasu daje kwas pikolinowy :
Traktowanie 2-metylopirydyny butylolitem powoduje deprotonowanie grupy metylowej:
- H 3 CC 5 H 4 N + BuLi → LiH 2 CC 5 H 4 N + BuH
Biodegradacja
Podobnie jak inne pochodne pirydyny, 2-metylopirydyna jest często zgłaszana jako zanieczyszczenie środowiska związane z obiektami przetwarzającymi łupki bitumiczne lub węgiel, a także została znaleziona w starszych miejscach obróbki drewna. Związek jest łatwo rozkładany przez niektóre mikroorganizmy, takie jak Arthrobacter sp. szczep R1 (szczep ATTC numer 49987), który został wyizolowany z warstwy wodonośnej zanieczyszczonej złożoną mieszaniną pochodnych pirydyny. że Arthrobacter i blisko spokrewnione Actinomycetota są związane z degradacją pochodnych pirydyny i innych heterocyklicznych związków azotu. 2-Metypirydyna i 4-Metypirydyna są łatwiej rozkładane i wykazują mniejszą utratę lotności z próbek środowiskowych niż 3-Metypirydyna.
Używa
2-Metylopirydyna jest półproduktem używanym do produkcji niektórych leków farmaceutycznych, w tym amprolium , pikoplatyny , dimetyndenu i enkainidu .
Toksyczność
Podobnie jak większość alkilopirydyn, LD50 2-metylopirydyny jest skromne i wynosi 790 mg/kg (doustnie, szczur).