Linamaryna
|
|

|
|
|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
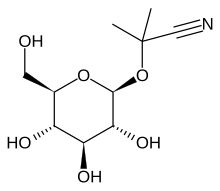
2-(β- D -glukopiranozyloksy)-2-metylopropanonitryl
|
|
|
Preferowana nazwa IUPAC
2-Metylo-2-{[(2S , 3R , 4S , 5S , 6R ) -3,4,5-trihydroksy-6-(hydroksymetylo)oksan-2-ylo]oksy}propanonitryl |
|
| Inne nazwy Fazolunatyna
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.164.971 |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C10H17NO6 _ _ _ _ _ _ | |
| Masa cząsteczkowa | 247,248 g/mol |
| Wygląd | igły bezbarwne |
| Gęstość | 1,41 g·cm -3 |
| Temperatura topnienia | 143 do 144 ° C (289 do 291 ° F; 416 do 417 K) |
| Dobry | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Linamarin to glikozyd cyjanogenny występujący w liściach i korzeniach roślin takich jak maniok , fasola lima i len . Jest to glukozyd cyjanohydryny acetonu . Po wystawieniu na działanie enzymów i flory jelitowej w jelicie człowieka linamaryna i jej metylowana względna lotaustralina mogą rozkładać się do toksycznego związku chemicznego cyjanowodoru ; stąd zastosowania żywnościowe roślin zawierających znaczne ilości linamaryny wymagają intensywnego przygotowania i detoksykacji. Połknięta i wchłonięta linamaryna jest szybko wydalana z moczem, a sam glukozyd nie wydaje się być ostro toksyczny. Konsumpcja produktów z manioku o niskim poziomie linamaryny jest powszechna w nizinnych tropikach. Spożywanie żywności przygotowanej z niedostatecznie przetworzonych korzeni manioku z wysokim poziomem linamaryny wiąże się z toksycznością pokarmową, szczególnie w przypadku górnego neuronu ruchowego znanej jako konzo w Afryce populacje, w których został po raz pierwszy opisany przez Trolliego, a później przez sieć badawczą zainicjowaną przez Hansa Roslinga . Uważa się jednak, że toksyczność jest wywoływana przez spożycie cyjanohydryny acetonu , produktu rozpadu linamaryny. Narażenie na linamarynę w diecie było również zgłaszane jako czynnik ryzyka rozwoju nietolerancji glukozy i cukrzycy , chociaż badania na zwierzętach doświadczalnych były niespójne w odtwarzaniu tego efektu i mogą wskazywać, że głównym efektem jest pogorszenie istniejących warunków, a nie samo indukowanie cukrzycy.
Wytwarzanie cyjanku z linamaryny jest zwykle enzymatyczne i występuje, gdy linamaryna jest wystawiona na działanie linamarazy , enzymu normalnie wyrażanego w ścianach komórkowych roślin manioku. Ponieważ powstałe pochodne cyjanku są lotne, metody przetwarzania, które powodują taką ekspozycję, są powszechnymi tradycyjnymi sposobami przygotowania manioku; artykuły spożywcze są zwykle wytwarzane z manioku po dłuższym blanszowaniu , gotowaniu lub fermentacji . Produkty spożywcze wytwarzane z roślin manioku obejmują garri (prażone bulwy manioku ), przypominające owsiankę fufu , ciasto agbelima i mąkę z manioku .
Dzięki wysiłkom badawczym opracowano transgeniczną roślinę manioku, która stabilnie ogranicza produkcję linamaryny poprzez interferencję RNA .
- ^ a b c Shmuel Yannai: Dictionary of Food Compounds with CD-ROM: Additives, Flavours and Ingredients. CRC Press, 2003, ISBN 978-1-58488-416-3 , str. 695
- ^ Banea-Mayambu JP, Tylleskar T, Gitebo N, Matadi N, Gebre-Medhin M, Rosling H. (1997). Geograficzny i sezonowy związek między narażeniem na linamarinę i cyjanek z manioku a chorobą górnego neuronu ruchowego konzo w byłym Zairze. Trop Med Int Health 2(12):1143-51. PMID 9438470
- ^ Soto-Blanco B, Marioka PC, Górniak SL. (2002). Skutki długotrwałego podawania małej dawki cyjanku szczurom. Ecotoxicol Environ Saf 53(1):37-41. PMID 12481854
- ^ a b Soto-Blanco B, Sousa AB, Manzano H, Guerra JL, Gorniak SL. 2001. Czy przedłużona ekspozycja na cyjanek ma działanie diabetogenne? Weterynarz Hum Toxicol. 43(2):106-8.
- ^ Yessoufou A, Ategbo JM, Girard A, Prost J, Dramane KL, Moutairou K, Hichami A, Khan NA. (2002). Dieta wzbogacona w maniok nie jest diabetogenna, raczej zaostrza cukrzycę u szczurów. Fundam Clin Pharmacol 20(6):579-86. PMID 17109651
- ^ Padmaja G. (1995). Detoksykacja cyjankiem w manioku do zastosowań spożywczych i paszowych. Crit Rev Food Sci Nutr 35(4):299-339. PMID 7576161
- ^ Siritunga D, Sayre R (2003). „Generacja manioku transgenicznego wolnego od cyjanów”. Planta 217 (3): 367-73. doi : 10.1007/s00425-003-1005-8 PMID 14520563