Monokrzemek żelaza
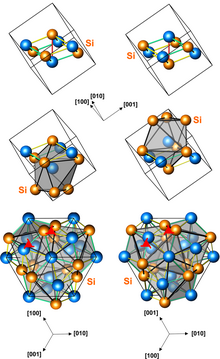 Struktury lewoskrętnych i prawoskrętnych kryształów FeSi. Górna prezentacja przedstawia osiem atomów komórki elementarnej. Środek przedstawia wielościany otaczające atomy żelaza. Dno pokazuje obecność osi śrubowych.
|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
krzemek żelaza
|
|
| Inne nazwy Naquite, fersilicite
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA | 100.031.506 |
| Numer WE |
|
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| FeSi | |
| Masa cząsteczkowa | 83,931 g/mol |
| Wygląd | szare sześcienne kryształy |
| Gęstość | 6,1 g/ cm3 |
| Temperatura topnienia | 1410 ° C (2570 ° F; 1680 K) |
| Przerwa pasmowa |
0,05 eV ( ind. ) 0,14 eV (kier.) |
| 8,5 × 10-6 emu /g | |
| Struktura | |
| Sześcienny | |
| P2 1 3 (nr 198), cP8 | |
|
a = 0,44827(1) nm
|
|
|
Jednostki wzoru ( Z )
|
4 |
| Zagrożenia | |
| Punkt zapłonu | Nie palne |
| Związki pokrewne | |
|
Inne aniony
|
Żelazo germanek |
|
Inne kationy
|
Krzemek kobaltu Krzemek manganu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Monokrzemek żelaza ( FeSi ) jest związkiem międzymetalicznym , krzemkiem żelaza występującym w przyrodzie jako rzadki minerał naquit . Jest to półprzewodnik o wąskim pasmie wzbronionym o rezystywności elektrycznej w temperaturze pokojowej ok. 10 000 Ohm·cm i niezwykłe właściwości magnetyczne w niskich temperaturach. FeSi ma sześcienną sieć krystaliczną bez centrum inwersji ; dlatego jego struktura magnetyczna jest spiralna, z chiralnością prawoskrętną i lewoskrętną .
Struktura jest podobna do chlorku sodu , z czterema atomami żelaza i czterema atomami krzemu w każdej komórce elementarnej. Podczas gdy w chlorku sodu osiem atomów znajduje się w rogach sześcianu, a każdy jon jest otoczony sześcioma przeciwjonami, w monokrzemku żelaza wszystkie atomy są przesunięte równolegle do przekątnych ciała (wzdłuż 3-krotnych osi) z pozycji sodu i chlorku. Kryształ traci zatem symetrię, ale zachowuje 2-krotne osie śrubowe i 3-krotne osie struktury krystalicznej chlorku sodu. W wyniku tego przemieszczenia atom żelaza znajduje się mniej więcej tak blisko atomu krzemu na tej samej potrójnej osi, jak do dowolnego z pozostałych sześciu otaczających go atomów krzemu (zamiast być 3 {\ displaystyle {\ czas dalej, jak w chlorku sodu). Oznacza to, że każdy atom żelaza ma siedem pobliskich atomów krzemu i odwrotnie, każdy atom krzemu znajduje się w podobnym ( enancjomorficznym ) klatka atomów żelaza. Klatki mają tylko 3-krotną symetrię obrotową, z trzema nieco różnymi odległościami między atomami między atomem centralnym a siedmioma atomami otaczającymi (odpowiednio do 3 atomów, 3 atomów i 1 atomu). Istnieją prawoskrętne i lewoskrętne 3-krotne osie śrubowe bez elementu symetrii prowadzącego jeden do drugiego. (Trzykrotne osie śrub istnieją również w chlorku sodu, ale są powiązane przez lustro). Oznacza to, że kryształy monokrzemku żelaza istnieją w dwóch różnych enancjomorfikach.
W 1948 Linus Pauling zbadał naturę wiązań w monokrzemku żelaza.
