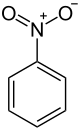
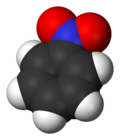
Nitrobenzen
|
|
|||

|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Nitrobenzen |
|||
| Inne nazwy Nitrobenzol Olejek mirbanu |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 507540 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.002.469 | ||
| Numer WE |
|
||
| 50357 | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS |
|
||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 6 H 5 NIE 2 | |||
| Masa cząsteczkowa | 123,11 g/mol | ||
| Wygląd | żółtawa, oleista ciecz | ||
| Zapach | ostry jak pasta do butów | ||
| Gęstość | 1,199 g/cm 3 | ||
| Temperatura topnienia | 5,7 ° C (42,3 ° F; 278,8 K) | ||
| Temperatura wrzenia | 210,9 ° C (411,6 ° F; 484,0 K) | ||
| 0,19 g/100 ml w temperaturze 20°C | |||
| Ciśnienie pary | 0,3 mmHg (25°C) | ||
| -61,80· 10-6 cm3 / mol | |||
| Lepkość | 1,8112 mPa·s | ||
| Zagrożenia | |||
| Oznakowanie GHS : | |||
 
|
|||
| Niebezpieczeństwo | |||
| H301 , H311 , H331 , H351 , H360 , H372 , H412 | |||
| P201 , P202 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P301+P310 , P302+P352 , P304 +P340 , P308+P313 , P311 , P312 , P314 , P321 , P322 , P330 , P361 , P363 , P403+P233 , P405 , P501 | |||
| NFPA 704 (ognisty diament) | |||
| Punkt zapłonu | 88 ° C (190 ° F; 361 K) | ||
| 480 ° C (896 ° F; 753 K) | |||
| Wybuchowe granice | 1,8%-? | ||
| Śmiertelna dawka lub stężenie (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
780 mg/kg (szczur, doustnie) 600 mg/kg (szczur, doustnie) 590 mg/kg (mysz, doustnie) |
||
|
LD Lo ( najniższy opublikowany )
|
750 mg/kg (pies, doustnie) | ||
| NIOSH (limity ekspozycji na zdrowie w USA): | |||
|
PEL (dopuszczalny)
|
TWA 1 ppm (5 mg/m 3 ) [skóra] | ||
|
REL (zalecane)
|
TWA 1 ppm (5 mg/m 3 ) [skóra] | ||
|
IDLH (bezpośrednie zagrożenie)
|
200 str./min | ||
| Związki pokrewne | |||
|
Związki pokrewne
|
Anilina Chlorek benzenodiazoniowy Nitrozobenzen |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Nitrobenzen jest związkiem organicznym o wzorze chemicznym C 6 H 5 NO 2 . Jest to nierozpuszczalny w wodzie bladożółty olej o migdały . Zamarza, dając zielonkawo-żółte kryształy. Produkowany jest na dużą skalę z benzenu jako prekursor aniliny . W laboratorium jest czasami używany jako rozpuszczalnik , zwłaszcza w przypadku odczynników elektrofilowych .
Produkcja
Nitrobenzen otrzymuje się przez nitrowanie benzenu mieszaniną stężonego kwasu siarkowego , wody i kwasu azotowego . Ta mieszanina jest czasami nazywana „kwasem mieszanym”. Produkcja nitrobenzenu jest jednym z najniebezpieczniejszych procesów prowadzonych w przemyśle chemicznym ze względu na egzotermię reakcji (Δ H = −117 kJ/mol).
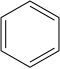 +
+
Światowe zdolności produkcyjne nitrobenzenu w 1985 roku wynosiły około 1 700 000 ton .
Proces nitrowania polega na wytworzeniu jonu nitroniowego (NO 2 + ), a następnie elektrofilowej reakcji podstawienia aromatycznego z benzenem. Jon nitroniowy jest generowany w reakcji kwasu azotowego i kwaśnego środka odwadniającego, zazwyczaj kwasu siarkowego:
- HNO 3 + H + ⇌ NIE 2 + + H 2 O
Używa
Około 95% nitrobenzenu produkowanego przemysłowo jest uwodorniane do aniliny :
- C 6 H 5 NO 2 + 3 H 2 → C 6 H 5 NH 2 + 2 H 2 O
Anilina jest prekursorem polimerów uretanowych , chemikaliów gumowych , pestycydów , barwników (zwłaszcza barwników azowych ), materiałów wybuchowych i farmaceutyków .
 Większość aniliny jest zużywana do produkcji metylenodianiliny , prekursora poliuretanów.
Większość aniliny jest zużywana do produkcji metylenodianiliny , prekursora poliuretanów.
Aplikacje specjalistyczne
Nitrobenzen jest również używany do maskowania nieprzyjemnych zapachów w pastach do butów i podłóg, opatrunkach skórzanych, rozpuszczalnikach do farb i innych materiałach. Redestylowany jako olej mirbany nitrobenzen był używany jako niedrogi środek zapachowy do mydeł . W tym celu został zastąpiony mniej toksycznymi chemikaliami. Znaczącym rynkiem zbytu dla nitrobenzenu jest jego zastosowanie do produkcji przeciwbólowego paracetamolu ( znanego również jako acetaminofen) (Mannsville 1991). Nitrobenzen jest również stosowany w komórkach Kerra , ponieważ ma niezwykle dużą stałą Kerra . Dowody wskazują na jego zastosowanie w rolnictwie jako stymulator wzrostu / kwitnienia roślin.
Reakcje organiczne
Oprócz konwersji do aniliny, nitrobenzen można selektywnie redukować do azoksybenzenu , azobenzenu , nitrozobenzenu , hydrazobenzenu i fenylohydroksyloaminy . Był używany jako łagodny utleniacz w reakcjach takich jak synteza chinoliny Skraupa .
Bezpieczeństwo
Nitrobenzen jest wysoce toksyczny ( wartość progowa 5 mg/m 3 ) i łatwo wchłaniany przez skórę.
Długotrwałe narażenie może spowodować poważne uszkodzenie ośrodkowego układu nerwowego , zaburzenia widzenia, uszkodzenie wątroby lub nerek, anemię i podrażnienie płuc. Wdychanie oparów może powodować ból głowy, nudności, zmęczenie, zawroty głowy, sinicę , osłabienie rąk i nóg, aw rzadkich przypadkach może być śmiertelne. Olej jest łatwo wchłaniany przez skórę i może przyspieszyć tętno, spowodować drgawki lub rzadko śmierć. Spożycie może podobnie powodować bóle głowy, zawroty głowy, nudności, wymioty i podrażnienie przewodu pokarmowego, utratę czucia/użytkowania w kończynach, a także powoduje krwawienie wewnętrzne.
Nitrobenzen jest uważany przez Agencję Ochrony Środowiska Stanów Zjednoczonych za prawdopodobny czynnik rakotwórczy dla ludzi i jest klasyfikowany przez IARC jako czynnik rakotwórczy grupy 2B , który jest „prawdopodobnie rakotwórczy dla ludzi”. Wykazano, że powoduje gruczolaki i raki wątroby, nerek i tarczycy u szczurów.
Został sklasyfikowany jako wyjątkowo niebezpieczna substancja w Stanach Zjednoczonych, zgodnie z definicją zawartą w sekcji 302 amerykańskiej ustawy o planowaniu kryzysowym i wspólnotowym prawie do wiedzy (42 USC 11002), i podlega ścisłym wymogom zgłaszania przez zakłady, które produkują, przechowują, lub używać go w znacznych ilościach.
Kultura popularna
- Opowiadanie The Avenging Chance z 1927 roku autorstwa Anthony'ego Berkeleya omawia współczesne zastosowania nitrobenzenu. Znajduje się również w centrum fabuły w The Poisoned Chocolates Case Berkeleya z 1929 roku.
- W powieści detektywistycznej Nero Wolfe'a The Red Box autorstwa Rexa Stouta z 1937 roku osoba zostaje zamordowana przez wylanie na nią nitrobenzenu (zwanego także „esencją mirbany”) w jego samochodzie.
- Juliana Symonsa „Klub Świętego Mikołaja” z 1960 roku osoba zostaje zamordowana nitrobenzenem.