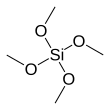
Ortokrzemian tetrametylu
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
nazwa IUPAC
tetrametoksysilan
|
|||
| Inne nazwy ortokrzemian tetrametylu; krzemian metylu; kwas krzemowy, ester tetrametylowy; metanolan krzemu; TMOS
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.010.598 | ||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| SiC4H12O4 _ _ _ _ _ | |||
| Masa cząsteczkowa | 152,25 | ||
| Wygląd | bezbarwna ciecz | ||
| Gęstość | 1.032 | ||
| Temperatura topnienia | 4 do 5 ° C (39 do 41 ° F; 277 do 278 K) | ||
| Temperatura wrzenia | 121 do 122 ° C (250 do 252 ° F; 394 do 395 K) | ||
| rozpuszczalniki organiczne | |||
| Ciśnienie pary | 12 mmHg (25°C) | ||
| Zagrożenia | |||
| Bezpieczeństwo i higiena pracy (BHP): | |||
|
Główne zagrożenia
|
toksyczny | ||
| Punkt zapłonu | 96°C; 205 ° F; 369 k | ||
| NIOSH (limity ekspozycji na zdrowie w USA): | |||
|
PEL (dopuszczalny)
|
nic | ||
|
REL (zalecane)
|
TWA 1 ppm (6 mg/m 3 ) | ||
|
IDLH (bezpośrednie zagrożenie)
|
ND | ||
| Związki pokrewne | |||
|
Inne kationy
|
Boran trimetylu Fosforyn trimetylu |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Ortokrzemian tetrametylu (TMOS) to związek chemiczny o wzorze Si(OCH 3 ) 4 . Cząsteczka ta składa się z czterech grup metoksylowych związanych z atomem krzemu . Podstawowe właściwości są podobne do bardziej popularnego ortokrzemianu tetraetylu , który jest zwykle preferowany, ponieważ produkt hydrolizy , etanol , jest mniej toksyczny niż metanol .
Ortokrzemian tetrametylu hydrolizuje do SiO 2 :
W syntezie organicznej Si(OCH 3 ) 4 został użyty do przekształcenia odpowiednio ketonów i aldehydów w odpowiednie ketale i acetale .
Bezpieczeństwo
W wyniku hydrolizy Si(OCH 3 ) 4 powstaje nierozpuszczalny SiO 2 i CH 3 OH (metanol). Nawet przy niskich stężeniach wdychanie powoduje uszkodzenia płuc, a przy nieco wyższych stężeniach kontakt oczu z oparami powoduje ślepotę [ potrzebne źródło ] . Co gorsza, przy niskich stężeniach (200 ppm/15 min) uszkodzenie jest często podstępne, a objawy pojawiają się w kilka godzin po ekspozycji. Sposób działania polega na wytrącaniu krzemionki w oczach i/lub płucach [ potrzebne źródło ] . Wbrew powszechnym informacjom, w tym kilku błędnym MSDS , wytwarzany metanol stanowi zagrożenie jedynie w wyniku chronicznego narażenia i jest stosunkowo niewielkim problemem. Mechanizmy toksyczności metanolu są dobrze poznane, metanol powoduje ślepotę poprzez konwersję do formaldehydu, a następnie do toksycznego kwasu mrówkowego w wątrobie; Dostanie się metanolu do oczu powoduje jedynie umiarkowane i odwracalne podrażnienie oczu.
- ^ a b c d e Kieszonkowy przewodnik NIOSH dotyczący zagrożeń chemicznych. "#0428" . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ Sakurai, H. „metanolan krzemu (IV)” w Encyklopedii odczynników do syntezy organicznej 2001 John Wiley & Sons. doi : 10.1002/047084289X.rs012
- ^ „Krzemian tetrametylu” . Narodowa Biblioteka Lekarska - Bank Danych o Substancjach Niebezpiecznych . Narodowa Biblioteka Lekarska . Źródło 11 lutego 2013 r .
- Bibliografia _ _ Bank Danych o Substancjach Niebezpiecznych - Narodowa Biblioteka Lekarska . Narodowa Biblioteka Lekarska . Źródło 11 lutego 2013 r .
Linki zewnętrzne
- Strona książki internetowej dla SiC 4 H 12 O 4
- CDC - Kieszonkowy przewodnik NIOSH dotyczący zagrożeń chemicznych