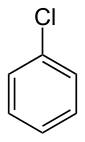
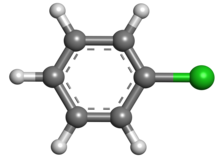
Chlorobenzen
|
|
|||
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Chlorobenzen |
|||
| Inne nazwy Chlorek fenylu, monochlorobenzen
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 3DMet | |||
| Skróty | PhCl | ||
| 605632 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.003.299 | ||
| Numer WE |
|
||
| 26704 | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS |
|
||
| UNII | |||
| Numer ONZ | 1134 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C6H5Cl _ _ _ _ | |||
| Masa cząsteczkowa | 112,56 g/mol | ||
| Wygląd | bezbarwna ciecz | ||
| Zapach | przypominający migdały | ||
| Gęstość | 1,11 g/cm3 , ciecz | ||
| Temperatura topnienia | -45,58 ° C (-50,04 ° F; 227,57 K) | ||
| Temperatura wrzenia | 131,70 ° C (269,06 ° F; 404,85 K) | ||
| 0,5 gl -1 w wodzie o temperaturze 20°C | |||
| Rozpuszczalność w innych rozpuszczalnikach | rozpuszczalny w większości rozpuszczalników organicznych | ||
| Ciśnienie pary | 9 mmHg | ||
| −69,97·10 −6 cm 3 /mol | |||
|
Współczynnik załamania światła ( n D )
|
1,52138 | ||
| Lepkość | 0,7232 | ||
| Zagrożenia | |||
| Bezpieczeństwo i higiena pracy (BHP): | |||
|
Główne zagrożenia
|
Niskie do umiarkowanego zagrożenie | ||
| Oznakowanie GHS : | |||
  
|
|||
| Ostrzeżenie | |||
| H226 , H302 , H305 , H315 , H332 , H411 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P273 , P280 , P302+P352 , P303 +P361+P353 , P304+P312 , P304 + P340 , P312 , P 321 , P332 + P313 , P362 , P370+P378 , P391 , P403+P235 , P501 | |||
| NFPA 704 (ognisty diament) | |||
| Punkt zapłonu | 29 ° C (84 ° F; 302 K) | ||
| Wybuchowe granice | 1,3%-9,6% | ||
| Śmiertelna dawka lub stężenie (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
2290 mg/kg (szczur, doustnie)
|
||
|
LC Lo ( najniższy opublikowany )
|
8000 ppm (kot, 3 godz.) | ||
| NIOSH (limity narażenia na zdrowie w USA): | |||
|
PEL (dopuszczalny)
|
TWA 75 ppm (350 mg/ m3 ) | ||
|
REL (zalecane)
|
nic | ||
|
IDLH (bezpośrednie zagrożenie)
|
1000 stron na minutę | ||
| Związki pokrewne | |||
|
Powiązane halobenzeny
|
Fluorobenzen Bromobenzen Jodobenzen |
||
|
Związki pokrewne
|
benzen 1,4-dichlorobenzen |
||
| Strona danych uzupełniających | |||
| Chlorobenzen (strona danych) | |||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Chlorobenzen jest aromatycznym związkiem organicznym o wzorze chemicznym C 6 H 5 Cl. Ta bezbarwna, łatwopalna ciecz jest powszechnym rozpuszczalnikiem i szeroko stosowanym półproduktem do produkcji innych chemikaliów.
Używa
Historyczny
Głównym zastosowaniem chlorobenzenu jest półprodukt do produkcji herbicydów, barwników i gumy. Chlorobenzen jest również stosowany jako wysokowrzący rozpuszczalnik w zastosowaniach przemysłowych, a także w laboratoriach. Chlorobenzen jest nitrowany na dużą skalę z wytworzeniem mieszaniny 2-nitrochlorobenzenu i 4-nitrochlorobenzenu , które są rozdzielane. Te mononitrochlorobenzeny są przekształcane w pokrewny 2-nitrofenol , 2-nitroanizol, bis (2-nitrofenylo) disiarczek i 2-nitroanilinę przez nukleofilowe wypieranie chlorku odpowiednio wodorotlenkiem sodu , metanolanem sodu , disiarczkiem sodu i amoniakiem . Konwersje pochodnej 4-nitrowej są podobne.
Chlorobenzen był kiedyś używany do produkcji pestycydów , w szczególności DDT , w reakcji z chloralem (trichloroacetaldehydem), ale to zastosowanie spadło wraz ze spadkiem użycia DDT. Kiedyś chlorobenzen był głównym prekursorem do produkcji fenolu :
- C6H5Cl + NaOH → C6H5OH + NaCl _ _
Produktem ubocznym reakcji jest również sól . Reakcja jest znana jako proces Dow , przy czym reakcję przeprowadza się w temperaturze 350°C przy użyciu stopionego wodorotlenku sodu bez rozpuszczalnika. Eksperymenty ze znakowaniem pokazują, że reakcja przebiega poprzez eliminację/dodanie, przez benzynę jako produkt pośredni.
Produkcja
Po raz pierwszy został opisany w 1851 roku. Chlorobenzen jest wytwarzany przez chlorowanie benzenu w obecności katalitycznej ilości kwasu Lewisa , takiego jak chlorek żelazowy , dichlorek siarki i bezwodny chlorek glinu :
Katalizator zwiększa elektrofilowość chloru. Ponieważ chlor jest elektroujemny, C 6 H 5 Cl wykazuje nieco zmniejszoną podatność na dalsze chlorowanie. Na skalę przemysłową reakcję prowadzi się w sposób ciągły, aby zminimalizować powstawanie dichlorobenzenów .
Trasy laboratoryjne
Chlorobenzen jest wytwarzany z aniliny poprzez chlorek benzenodiazoniowy , inaczej znany jako reakcja Sandmeyera .
Bezpieczeństwo
LD50 , na co wskazuje jego wynoszący 2,9 g/kg. Administracja ds. Bezpieczeństwa i Higieny Pracy ustaliła dopuszczalny limit narażenia na 75 ppm (350 mg/m 3 ) w ciągu ośmiogodzinnej średniej ważonej dla pracowników mających kontakt z chlorobenzenem.
Toksykologia i biodegradacja
Chlorobenzen może utrzymywać się w glebie przez kilka miesięcy, w powietrzu przez około 3,5 dnia, aw wodzie przez mniej niż jeden dzień. Ludzie mogą być narażeni na ten czynnik poprzez wdychanie zanieczyszczonego powietrza (głównie w wyniku narażenia zawodowego), spożywanie skażonej żywności lub wody lub kontakt ze skażoną glebą (zwykle w pobliżu niebezpiecznych składowisk odpadów). Jednakże, ponieważ został znaleziony tylko w 97 z 1177 składowisk odpadów niebezpiecznych NPL, nie jest uważany za powszechne zanieczyszczenie środowiska. Bakteria Rhodococcus phenolicus rozkłada chlorobenzen jako jedyne źródło węgla.
Po przedostaniu się do organizmu, zwykle przez zanieczyszczone powietrze, chlorobenzen jest wydalany zarówno przez płuca, jak i układ moczowy.
Na innych planetach
W 2015 roku zespół naukowy SAM ogłosił, że łazik Curiosity zgłosił dowody na wyższe stężenia chlorobenzenu w skale osadowej o nazwie „ Cumberland ” na Marsie . Zespół spekulował, że chlorobenzen mógł powstać, gdy próbka była podgrzewana w komorze do pobierania próbek instrumentu. Ogrzewanie wywołałoby reakcję substancji organicznych w marsjańskiej glebie, o której wiadomo, że zawiera nadchloran.
Zobacz też
Linki zewnętrzne
-
 Media związane z chlorobenzenem w Wikimedia Commons
Media związane z chlorobenzenem w Wikimedia Commons