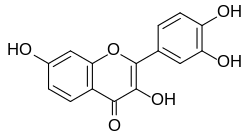
Fisetyna
|
|

|
|
| Nazwy | |
|---|---|
|
nazwa IUPAC
2-(3,4-dihydroksyfenylo)-3,7-dihydroksychromen-4-on
|
|
|
Preferowana nazwa IUPAC
2-(3,4-dihydroksyfenylo)-3,7-dihydroksy-4H - 1-benzopiran-4-on |
|
| Inne nazwy Kotynina (nie mylić z kotyniną ) 5-Deoksykwercetyna Superfustel Fisetholz Fietin Fustel Fustet Viset Junger fustik |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Bank Leków | |
| Karta informacyjna ECHA | 100.007.669 |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C15H10O6 _ _ _ _ _ | |
| Masa cząsteczkowa | 286,2363 g/mol |
| Gęstość | 1,688 g/ml |
| Temperatura topnienia | 330 ° C (626 ° F; 603 K) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Fisetyna (7,3′,4′- flavon-3-ol ) to roślinny flawonol z grupy flawonoidów polifenoli . Można go znaleźć w wielu roślinach, gdzie służy jako środek barwiący na żółto/ ochrę . Występuje również w wielu owocach i warzywach, takich jak truskawki, jabłka, persymony, cebula i ogórki. Jego wzór chemiczny został po raz pierwszy opisany przez austriackiego chemika Josefa Herziga w 1891 roku.
Biologiczną aktywność fisetyny badano w wielu testach laboratoryjnych; podobnie jak inne polifenole wykazuje wiele działań.
Źródła biologiczne
Fisetynę można znaleźć w wielu różnych roślinach. Występuje w Eudicotyledons , takich jak drzewa i krzewy z rodziny bobowatych , takich jak akacje Acacia greggii i Acacia berlandieri , drzewo papugowe ( Butea frondosa ), szarańcza miodowa ( Gleditsia triacanthos ), członkowie rodziny Anacardiaceae , tacy jak Quebracho colorado i gatunek z rodzaju Rhus , który zawiera sumaki. Wraz z mirycetyną , fisetyna zapewnia kolor tradycyjnego żółtego barwnika młodego fustyka , który został wyekstrahowany z eurazjatyckiego drzewa dymnego ( Rhus cotinus ). Wiele owoców i warzyw zawiera również fisetynę, w tym truskawki , jabłka i winogrona. Fisetynę można ekstrahować z owoców i ziół w sokach, winach i naparach, takich jak herbaty. Występuje również w roślinach jednoliściennych , takich jak cebula . Występuje również w Pinophyta , takich jak cyprys żółty ( Callitropsis nootkatensis ).
| Źródło roślinne |
Ilość Fisetyny (μg /g) |
|---|---|
| Toxicodendron vernicifluum | 15000 |
| Truskawka | 160 |
| Jabłko | 26 |
| Persymona | 10.6 |
| Cebula | 4.8 |
| korzeń lotosu | 5.8 |
| Winogrona | 3.9 |
| Kiwi | 2.0 |
| Brzoskwinia | 0,6 |
| Ogórek | 0,1 |
| Pomidor | 0,1 |
Biosynteza
Fisetyna jest flawonoidem , który jest podgrupą polifenoli . Synteza flawonoidów rozpoczyna się od fenylopropanoidowego , w którym fenyloalanina , aminokwas, jest przekształcana w 4-kumaroilo-CoA . Jest to związek, który wchodzi na szlak biosyntezy flawonoidów. Syntaza chalkonu , pierwszy enzym tego szlaku, wytwarza chalkon z 4-kumaroilo-CoA. Wszystkie flawonoidy pochodzą z tego szkieletu chalkonu (ta rodzina to tak zwane chalkonoidy ). Aktywność różnych enzymów, w tym izomeraz i hydroksylaz, zmienia szkielet w zależności od podklasy produkowanego flawonoidu. Transferazy pomagają kontrolować zmiany w rozpuszczalności i reaktywności flawonoidów poprzez katalizowanie dodawania rzeczy, takich jak grupy metylowe i cukry. Pozwala to na kontrolowane wahania czynności fizjologicznych.
Regulacja genu biosyntezy flawonoidów zachodzi poprzez interakcję różnych czynników transkrypcyjnych. W zależności od kombinacji oddziaływań czynników transkrypcyjnych geny strukturalne biorące udział w biosyntezie flawonoidów ulegają ekspresji w określonych miejscach rośliny iw określonym czasie. Wiele czynników transkrypcyjnych mieloblastozy (MYB) zidentyfikowano w różnych owocach i roślinach, w tym truskawkach, kukurydzy i Arabidopsis, jako ważnych w regulacji biosyntezy i akumulacji flawonoidów. Te czynniki transkrypcyjne są nadal badane w modelowych organizmach roślinnych, takich jak kukurydza i Arabidopsis.
Wykazano również, że środowisko rośliny wpływa na szlak biosyntezy flawonoidów. Krótsze długości fal światła, od światła niebieskiego do światła UV, pozwalają na większą produkcję i akumulację flawonoidów w owocach. Te długości fal aktywują enzymy biorące udział w szlakach biosyntezy fenylopropanoidów i flawonoidów, stymulując produkcję flawonoidów. Poziom stymulacji może się różnić w zależności od poszczególnych owoców.
Znaczenie kliniczne
Fisetyna, podobnie jak inne polifenole, takie jak resweratrol , jest związkiem aktywującym sirtuinę i wykazano w badaniach laboratoryjnych, że przedłuża życie drożdży, robaków, much i myszy. Podobnie jak inne związki, wykazano również, że jest reaktywny w wielu różnych testach aktywności biologicznej, co zwiększa prawdopodobieństwo, że jakikolwiek lek wytworzony z fisetyny miałby zbyt wiele skutków ubocznych, aby był użyteczny.
Fisetyna wykazała działanie przeciwnowotworowe w badaniach na komórkach i zwierzętach modelowych przeprowadzonych w laboratoriach i wydaje się, że blokuje szlak PI3K/AKT/mTOR wraz z innymi mechanizmami indukującymi aktywację apoptozy i zapobiega oporności na apoptozę.
W badaniach laboratoryjnych wykazano, że fisetyna jest środkiem antyproliferacyjnym , zakłócającym cykl komórkowy na kilka sposobów. Podobnie jak niektóre inne flawonoidy , w badaniach laboratoryjnych stwierdzono, że jest inhibitorem topoizomerazy , co może okazać się działaniem rakotwórczym lub przeciwnowotworowym; potrzebne są dalsze badania.
Wykazano, że fisetyna jest skutecznym środkiem senolitycznym u myszy typu dzikiego, z efektem wydłużenia życia, zmniejszonymi markerami starzenia w tkankach i zmniejszonymi patologiami związanymi z wiekiem. Badania kultur komórkowych starzejących się ludzkich komórek śródbłonka żyły pępowinowej wykazały, że fisetyna indukuje apoptozę poprzez hamowanie antyapoptotycznego białka Bcl-xL . Fisetyna ma mniej więcej dwa razy większą moc senolityczną niż kwercetyna . Od października 2018 r. Trwało badanie kliniczne w USA w celu wykazania skuteczności u ludzi.
cytokin prozapalnych , w tym czynnika martwicy nowotworów alfa , interleukiny 6 i czynnika jądrowego kappa B (NF-κB). Działanie przeciwzapalne wynika z deacylacji prozapalnego czynnika transkrypcyjnego NF-κB przez sirtuinę 1 .
W badaniach laboratoryjnych wykazano, że fisetyna zwiększa poziom glutationu , endogennego przeciwutleniacza. Ma bezpośrednie działanie jako środek redukujący , reagując chemicznie z reaktywnymi formami tlenu w celu ich zneutralizowania. Badania sugerują, że osadza się w błonach komórkowych i zapobiega uszkodzeniom oksydacyjnym lipidów w błonie komórkowej. Podobnie jak inne flawonoidy, ma płaską strukturę z wieloma pierścieniami węglowymi. Zmiata wolne rodniki dzięki zdolności oddawania elektronów, dzięki obecności dwóch hydroksylowych na jednym pierścieniu i grupy hydroksylowej na drugim.
Badania przesiewowe in vitro wykazały, że fisetyna jest związkiem antymitotycznym .