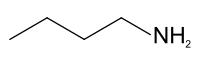
n -Butyloamina
|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Butan-1-amina |
|
Inne nazwy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| Skróty | NBA |
| 605269 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Bank Leków | |
| Karta informacyjna ECHA | 100.003.364 |
| Numer WE |
|
| 1784 | |
| Siatka | n-butyloamina |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS |
|
| UNII | |
| Numer ONZ | 1125 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C4H11N _ _ _ _ | |
| Masa cząsteczkowa | 73,139 g · mol -1 |
| Wygląd | Bezbarwna ciecz |
| Zapach | rybny, amoniakalny |
| Gęstość | 740 mg ml -1 |
| Temperatura topnienia | −49°C; −56 ° F; 224 k |
| Temperatura wrzenia | 77 do 79°C; 170 do 174 ° F; 350 do 352 K |
| Mieszalny | |
| dziennik P | 1.056 |
| Ciśnienie pary | 9,1 kPa (przy 20 °C) |
|
Stała prawa Henry'ego
( k H ) |
570 μmol Pa -1 kg -1 |
| Zasadowość (p K b ) | 3.22 |
| -58,9· 10-6 cm3 / mol | |
|
Współczynnik załamania światła ( n D )
|
1.401 |
| Lepkość | 500 µPa·s (przy 20 °C) |
| Termochemia | |
|
Pojemność cieplna ( C )
|
188 JK -1 mol -1 |
|
Standardowa entalpia formowania (Δ f H ⦵ 298 ) |
−128,9–126,5 kJ mol −1 |
|
Standardowa entalpia spalania (Δ c H ⦵ 298 ) |
−3,0196–−3,0174 MJ mol −1 |
| Zagrożenia | |
| Oznakowanie GHS : | |
  
|
|
| Niebezpieczeństwo | |
| H225 , H302 , H312 , H314 , H332 | |
| P210 , P280 , P305+P351+P338 , P310 | |
| NFPA 704 (ognisty diament) | |
| Punkt zapłonu | -7 ° C (19 ° F; 266 K) |
| 312 ° C (594 ° F; 585 K) | |
| Wybuchowe granice | 1,7–9,8% |
| Śmiertelna dawka lub stężenie (LD, LC): | |
|
LD 50 ( mediana dawki )
|
|
|
LC Lo ( najniższy opublikowany )
|
4000 ppm (szczur, 4 godz.) 263 ppm (mysz, 2 godz.) |
| NIOSH (limity ekspozycji na zdrowie w USA): | |
|
PEL (dopuszczalny)
|
C 5 ppm (15 mg/m 3 ) [skóra] |
|
REL (zalecane)
|
C 5 ppm (15 mg/m 3 ) [skóra] |
|
IDLH (bezpośrednie zagrożenie)
|
300 str./min |
| Karta charakterystyki (SDS) | hazard.com |
| Związki pokrewne | |
|
Powiązane alkanoaminy
|
|
|
Związki pokrewne
|
2-Metylo-2-nitrozopropan |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
n -Butyloamina jest związkiem organicznym (konkretnie aminą ) o wzorze CH 3 (CH 2 ) 3 NH 2 . Ta bezbarwna ciecz jest jedną z czterech izomerycznych amin butanu , pozostałe to sec -butyloamina , tert -butyloamina i izobutyloamina . Jest to ciecz o rybim, podobnym do amoniaku zapachu typowym dla amin. Ciecz nabiera żółtego koloru podczas przechowywania na powietrzu. Jest rozpuszczalny we wszystkich rozpuszczalnikach organicznych. Jego opary są cięższe od powietrza, a podczas spalania wydzielają się toksyczne tlenki azotu.
Synteza i reakcje
Powstaje w reakcji amoniaku i alkoholi z tlenkiem glinu :
- CH 3 (CH 2 ) 3 OH + NH 3 → CH 3 (CH 2 ) 3 NH 2 + H 2 O
n -Butyloamina jest słabą zasadą . pKa dla [ CH3 ( CH2 ) 3NH3 ] + wynosi 10,78 .
n -Butyloamina wykazuje reakcje typowe dla innych prostych alkiloamin, tj. alkilowanie, acylowanie, kondensację z karbonylkami. Tworzy kompleksy z jonami metali, na przykład cis- i trans- [PtI 2 (NH 2 Bu) 2 ].
Używa
Związek ten jest stosowany jako składnik do produkcji pestycydów (takich jak tiokarbozydy ), farmaceutyków i emulgatorów . Jest także prekursorem do produkcji N , N′ dibutylotiomocznika , przyspieszacza - wulkanizacji kauczuku oraz n -butylobenzenosulfonamidu, plastyfikatora nylonu . Jest stosowany w syntezie fengabiny , fungicydu benomylowego i butamoksanu oraz tolbutamid przeciwcukrzycowy .

Bezpieczeństwo
LD50 dla . szczurów drogą doustną wynosi 366 mg/kg
Jeśli chodzi o narażenie zawodowe na n -butyloaminę, Administracja ds. Bezpieczeństwa i Higieny Pracy oraz Narodowy Instytut Bezpieczeństwa i Higieny Pracy ustaliły limity narażenia zawodowego na pułap 5 ppm (15 mg/m 3 ) dla narażenia przez skórę.
Linki zewnętrzne
-
 Media związane z N-butyloaminą w Wikimedia Commons
Media związane z N-butyloaminą w Wikimedia Commons
