2,5-dimetylofuran

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
2,5-dimetylofuran |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.009.923 |
| Numer WE |
|
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C6H8O _ _ _ _ | |
| Masa cząsteczkowa | 96.13 |
| Wygląd | Płyn |
| Gęstość | 0,8897 g/cm 3 |
| Temperatura topnienia | -62 ° C (-80 ° F; 211 K) |
| Temperatura wrzenia | 92 do 94 ° C (198 do 201 ° F; 365 do 367 K) |
| Nierozpuszczalny | |
| -66,37· 10-6 cm3 / mol | |
|
Współczynnik załamania światła ( n D )
|
1,44 – 1,442 |
| Zagrożenia | |
| Bezpieczeństwo i higiena pracy (BHP): | |
|
Główne zagrożenia
|
Bardzo łatwopalny, szkodliwy |
| Punkt zapłonu | −1 ° C (30 ° F; 272 K) |
| 285,85 ° C (546,53 ° F; 559,00 K) | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
2,5-dimetylofuran jest związkiem heterocyklicznym o wzorze (CH 3 ) 2 C 4 H 2 O. Chociaż często jest określany skrótem DMF , nie należy go mylić z dimetyloformamidem . Pochodna furanu , ten prosty związek jest potencjalnym biopaliwem , pochodzącym z celulozy.
Produkcja
Fruktozę można przekształcić w 2,5-dimetylofuran w katalitycznym procesie przekształcania biomasy w ciecz . Konwersja fruktozy do DMF odbywa się za pośrednictwem hydroksymetylofurfuralu .
Fruktozę można uzyskać z glukozy, budulca celulozy.
Potencjał jako biopaliwo
DMF posiada szereg atrakcji jako biopaliwo . Ma gęstość energii o 40% większą niż etanol , co czyni go porównywalnym z benzyną (benzyną). Jest również stabilny chemicznie, a ponieważ jest nierozpuszczalny w wodzie, nie wchłania wilgoci z atmosfery. Odparowanie dimetylofuranu podczas procesu produkcyjnego wymaga również około jednej trzeciej mniej energii niż odparowanie etanolu, chociaż ma temperaturę wrzenia o około 14 ° C wyższą, przy 92 ° C, w porównaniu z 78 ° C dla etanolu.
Zdolność do wydajnego i szybkiego wytwarzania dimetylofuranu z fruktozy, znajdującej się w owocach i niektórych warzywach korzeniowych , lub z glukozy, którą można otrzymać ze skrobi i celulozy – wszystkie powszechnie dostępne w przyrodzie – zwiększa atrakcyjność dimetylofuranu, chociaż należy wziąć pod uwagę kwestie bezpieczeństwa badany. Bioetanol i biodiesel to obecnie wiodące biopaliwa płynne.
Stosunek stechiometryczny powietrze/paliwo w dimetylofuranie wynosi 10,72, w porównaniu do etanolu 8,95 i benzyny 14,56. Oznacza to, że spalanie dimetylofuranu wymaga około 33% mniej powietrza niż ta sama ilość benzyny, ale około 20% więcej powietrza niż ta sama ilość etanolu.
Wartość opałowa ciekłego dimetylofuranu wynosi 33,7 MJ/kg, w porównaniu do 26,9 MJ/kg dla etanolu i 43,2 MJ/kg dla benzyny. Badana liczba oktanowa (RON) dimetylofuranu wynosi 119. Utajone ciepło parowania w temperaturze 20°C wynosi 31,91 kJ/mol. Niedawne testy jednocylindrowego silnika benzynowego wykazały, że sprawność cieplna spalania dimetylofuranu jest podobna do sprawności benzyny.
Inne zastosowania
2,5-dimetylofuran służy jako zmiatacz tlenu singletowego , właściwość, która została wykorzystana do oznaczania tlenu singletowego w wodach naturalnych. Mechanizm obejmuje reakcję Dielsa-Aldera , po której następuje hydroliza , ostatecznie prowadząca do produktów diacetyloetylenu i nadtlenku wodoru . Niedawno w tym samym celu zastosowano alkohol furfurylowy . 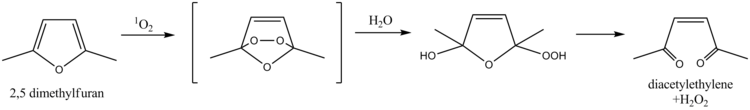
2,5-dimetylofuran został również zaproponowany jako wzorzec wewnętrzny dla spektroskopii NMR . 2,5-dimetylofuran ma singlety w swoim 1H NMR przy 8 2,2 i 5,8; singlety dają wiarygodne całki, podczas gdy pozycje pików nie zakłócają wielu analitów. Związek ma również odpowiednią temperaturę wrzenia wynoszącą 92°C, co zapobiega stratom wskutek parowania, a jednocześnie jest łatwy do usunięcia.
Rola w chemii żywności
2,5-dimetylofuran powstaje w wyniku termicznego rozkładu niektórych cukrów i został zidentyfikowany w śladowych ilościach jako składnik cukrów karmelizowanych .
Toksykologia
2,5-dimetylofuran odgrywa rolę w mechanizmie neurotoksyczności heksanu u ludzi. Wraz z heksano-2,5-dionem i 4,5-dihydroksy-2-heksanonem jest jednym z głównych metabolitów heksanu .
2,5-dimetylofuran został zidentyfikowany jako jeden ze składników dymu cygarowego o niskiej toksyczności dla rzęsek (zdolność do niekorzystnego oddziaływania na rzęski w drogach oddechowych , które są odpowiedzialne za usuwanie ciał obcych). Jego stężenie we krwi może służyć jako biomarker palenia .
Porównanie kart charakterystyki pokazuje, że obchodzenie się z 2,5-dimetylofuranem przez ludzi jest w przybliżeniu tak samo niebezpieczne jak obchodzenie się z benzyną.