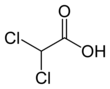
Kwas dichlorooctowy
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Kwas dichlorooctowy |
|||
| Inne nazwy Kwas dichloroetanowy, kwas bichlorooctowy, DCA, BCA, kwas dichlorooctowy, kwas bichlorooctowy
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 1098596 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Bank Leków | |||
| Karta informacyjna ECHA | 100.001.098 | ||
| Numer WE |
|
||
| 2477 | |||
| KEGG | |||
| Siatka | Dichlorooctan | ||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS |
|
||
| UNII | |||
| Numer ONZ | 1764 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C2H2Cl2O2 _ _ _ _ _ _ _ | |||
| Masa cząsteczkowa | 128,94 g·mol -1 | ||
| Wygląd | Bezbarwna ciecz | ||
| Gęstość | 1,5634 g/cm3 ( 20°C) | ||
| Temperatura topnienia | 9 do 11 ° C (48 do 52 ° F; 282 do 284 K) | ||
| Temperatura wrzenia | 194 ° C (381 ° F; 467 K) | ||
| mieszalny | |||
| Rozpuszczalność | mieszalny z etanolem , eterem dietylowym | ||
| Kwasowość ( p Ka ) | 1.35 | ||
| -58,2· 10-6 cm3 / mol | |||
| Termochemia | |||
|
Standardowa entalpia formowania (Δ f H ⦵ 298 ) |
−496,3 kJ·mol −1 | ||
| Zagrożenia | |||
| Oznakowanie GHS : | |||
 
|
|||
| Ostrzeżenie | |||
| H314 , H400 | |||
| P260 , P264 , P273 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P391 , P405 , P501 | |||
| NFPA 704 (ognisty diament) | |||
| Karta charakterystyki (SDS) | MSDS (jtbaker) | ||
| Związki pokrewne | |||
|
Powiązane kwasy chlorooctowe
|
Kwas chlorooctowy Kwas trichlorooctowy |
||
|
Związki pokrewne
|
Kwas octowy Kwas difluorooctowy Kwas dibromooctowy |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Kwas dichlorooctowy ( DCA ), czasami CH Cl
2 COOH nazywany kwasem bichlorooctowym ( BCA ), jest związkiem chemicznym o wzorze . Jest kwasem , analogiem kwasu octowego , w którym 2 z 3 atomów wodoru grupy metylowej zostały zastąpione atomami chloru . Podobnie jak inne kwasy chlorooctowe ma różne zastosowania praktyczne. Sole i estry kwasu dichlorooctowego nazywane są dichlorooctanami . Sole DCA były badane jako potencjalne leki , ponieważ hamują enzym kinazę dehydrogenazy pirogronianowej .
Chociaż wstępne badania wykazały, że DCA może spowolnić wzrost niektórych nowotworów w badaniach na zwierzętach i badaniach in vitro , od 2012 r. Nie ma wystarczających dowodów na poparcie stosowania DCA w leczeniu raka.
Chemia i występowanie
Chemia kwasu dichlorooctowego jest typowa dla fluorowcowanych kwasów organicznych . Należy do kwasów chlorooctowych . Jon dichlorooctanowy powstaje, gdy kwas miesza się z wodą. Jako kwas o p Ka równym 1,35, czysty kwas dichlorooctowy jest klasyfikowany jako mocny kwas organiczny ; jest bardzo żrący i skrajnie destrukcyjny dla tkanek błon śluzowych i górnych dróg oddechowych poprzez inhalację .
Wykazano, że DCA występuje w naturze w co najmniej jednym wodoroście, Asparagopsis taxiformis . Jest śladowym produktem chlorowania wody pitnej i jest wytwarzany w wyniku metabolizmu różnych leków lub chemikaliów zawierających chlor . DCA jest zwykle przygotowywany przez redukcję kwasu trichlorooctowego (TCA). DCA otrzymuje się z hydratu chloralu również w reakcji z węglanem wapnia i cyjankiem sodu w wodzie, a następnie zakwaszanie kwasem solnym . Można go również wykonać przepuszczając acetylen przez roztwory kwasu podchlorawego. [ potrzebne źródło ]
Jako odczynnik laboratoryjny , zarówno DCA, jak i TCA są używane jako środki wytrącające , które powodują wytrącanie makrocząsteczek , takich jak białka , z roztworu . [ potrzebne źródło ]
Zastosowania terapeutyczne
Miejscowa chemioablacja
i TCA są stosowane w zabiegach kosmetycznych (takich jak peelingi chemiczne i usuwanie tatuaży ) oraz jako miejscowe leki do chemioablacji brodawek , w tym kłykcin kończystych . Może również zabijać normalne komórki. [ potrzebne źródło ]
Kwasica mleczanowa
Randomizowane kontrolowane badanie na dzieciach z wrodzoną kwasicą mleczanową wykazało, że chociaż DCA było dobrze tolerowane, było nieskuteczne w poprawie wyników klinicznych. Oddzielne badanie DCA u dzieci z MELAS (zespół nieprawidłowej funkcji mitochondriów , prowadzący do kwasicy mleczanowej) zostało wcześnie przerwane, ponieważ wszystkie 15 dzieci otrzymujących DCA doświadczyło znacznej toksyczności nerwowej bez żadnych dowodów korzyści z leczenia. Randomizowane kontrolowane badanie DCA u dorosłych z kwasicą mleczanową wykazało, że chociaż DCA obniżyło poziom mleczanu we krwi, nie przyniosło żadnych korzyści klinicznych i nie poprawiło hemodynamiki ani przeżycia.
Tak więc, podczas gdy wczesne opisy przypadków i dane przedkliniczne sugerowały, że DCA może być skuteczne w przypadku kwasicy mleczanowej, późniejsze kontrolowane badania nie wykazały żadnych korzyści klinicznych z DCA w tym ustawieniu. Ponadto uczestnicy badań klinicznych nie byli w stanie kontynuować przyjmowania DCA jako badanego leku z powodu postępującej toksyczności.
Rak
W 2007 roku w prasie i Internecie pojawiły się doniesienia, że Evangelos Michelakis i współpracownicy z University of Alberta odkryli, że kwas dichlorooctowy, a raczej jego sól sodowa, dichlorooctan sodu, zmniejsza guzy u szczurów i zabija komórki nowotworowe in vitro . Artykuł w New Scientist wzbudził „bezprecedensowe zainteresowanie wśród czytelników”, ponieważ mówił o „tanim i prostym leku”, o którym „znano, że jest stosunkowo bezpieczny” i może zabić większość nowotworów. Towarzyszący artykuł redakcyjny wskazywał, że żadna firma farmaceutyczna nie byłaby zainteresowana uzyskaniem zatwierdzenia tego związku jako leku na raka, ponieważ nie ma on zdolności patentowej. Później w czasopiśmie opublikowano artykuł, w którym zwrócono uwagę na związane z tym niebezpieczeństwa, takie jak uszkodzenie nerwów. Amerykańska Agencja ds. Żywności i Leków zaczęła egzekwować prawo zabraniające sprzedaży substancji z sugestią, że są to leki na raka, chyba że zostały zatwierdzone przez FDA.
American Cancer Society w 2012 roku stwierdziło, że „dostępne dowody nie potwierdzają obecnie stosowania DCA w leczeniu raka”. Lekarze ostrzegali przed potencjalnymi problemami, jeśli ludzie spróbują wypróbować DCA poza kontrolowanym badaniem klinicznym . Jednym z problemów związanych z próbą tego jest zdobycie substancji chemicznej. Jeden oszust został skazany na 33 miesiące więzienia za sprzedaż białego proszku zawierającego skrobię, ale niezawierającego DCA, osobom chorym na raka.
Jedyna monitorowana dawka in vivo pięciu ludzkich pacjentów z glejakiem z DCA nie została zaprojektowana w celu sprawdzenia jej skuteczności przeciwko ich nowotworom. Badanie to miało raczej na celu sprawdzenie, czy można go bezpiecznie podawać w określonej dawce bez powodowania skutków ubocznych (np. neuropatii ). Wszystkich pięciu pacjentów otrzymywało inne leczenie podczas badania. Obserwacje in vitro i guzów pobranych od tych pięciu pacjentów sugerują, że DCA może działać przeciwko komórkom nowotworowym poprzez depolaryzację nieprawidłowych mitochondriów występujących w komórkach raka glejaka – umożliwiając mitochondriom indukowanie apoptozy (śmierci komórki) złośliwych komórek . Praca in vitro z DCA na nerwiakach niedojrzałych (które mają mniej rozpoznanych nieprawidłowości mitochondrialnych) wykazała aktywność przeciwko złośliwym, niezróżnicowanym komórkom. Opis przypadku z 2016 roku omawia i dokonuje przeglądu potencjalnego zastosowania DCA w nowotworach ośrodkowego układu nerwowego. Badanie z 2018 roku wykazało, że DCA może wywołać przemianę metaboliczną z glikolizy ( efekt Warburga ) do mitochondrialnego OXPHOS i zwiększyć reaktywny stres tlenowy wpływający na komórki nowotworowe. Efektów tych nie obserwowano w komórkach nienowotworowych.
Neuropatia
Neuropatia była problemem w niektórych badaniach klinicznych z DCA, powodując ich skuteczne zatrzymanie, ale przegląd BJC z 2008 roku wykazał, że nie wystąpiła ona w innych badaniach DCA. Mechanizm neuropatii indukowanej DCA nie jest dobrze poznany. Z jednej strony in vitro z nerwami zasugerowała mechanizm neuropatycznego efektu DCA; z DCA wykazującym zależną od dawki i ekspozycji demielinizację nerwów (zdzieranie „osłony”) nerwów, która to demielinizacja była częściowo odwracalna w czasie, po wypłukaniu DCA. Z drugiej strony przegląd BJC z 2008 roku stwierdza: „Ta neurotoksyczność przypominała wzorzec zależnej od długości, aksonalnej polineuropatii czuciowo-ruchowej bez demielinizacji”. w odniesieniu do badania z 2006 r. przeprowadzonego przez Kaufmana i in .
Niewydolność serca
DCA zostało zbadane jako leczenie powrotu do zdrowia po niedokrwieniu. Istnieją również dowody na to, że DCA poprawia metabolizm poprzez stymulację produkcji NADH, ale może prowadzić do wyczerpania NADH w normoksji.
Zobacz też
- Dalapon (kwas dichloropropionowy)