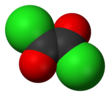
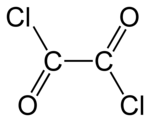
Chlorek oksalilu
|
|||
|
|
|||

|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Dichlorek oksalilu |
|||
|
Systematyczna nazwa IUPAC
Dichlorek etanodioilu |
|||
| Inne nazwy Chlorek kwasu szczawiowego Dichlorek kwasu szczawiowego (1:2) Dichlorek szczawiu Chlorek szczawiu |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA | 100.001.092 | ||
| Numer WE |
|
||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS |
|
||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 2 O 2 Cl 2 | |||
| Masa cząsteczkowa | 126,93 g/mol | ||
| Wygląd | Bezbarwna ciecz | ||
| Zapach | podobny do fosgenu | ||
| Gęstość | 1,4785 g/ml | ||
| Temperatura topnienia | -16 ° C (3 ° F; 257 K) | ||
| Temperatura wrzenia | 63 do 64 ° C (145 do 147 ° F; 336 do 337 K) przy 1,017 bara | ||
| Reaguje | |||
|
Współczynnik załamania światła ( n D )
|
1.429 | ||
| Zagrożenia | |||
| Bezpieczeństwo i higiena pracy (BHP): | |||
|
Główne zagrożenia
|
Toksyczny, żrący, łzawiący | ||
| Oznakowanie GHS : | |||
 
|
|||
| Niebezpieczeństwo | |||
| H314 , H331 | |||
| P261 , P280 , P305+P351+P338 , P310 | |||
| NFPA 704 (ognisty diament) | |||
| Karta charakterystyki (SDS) | Zewnętrzna karta charakterystyki | ||
| Związki pokrewne | |||
|
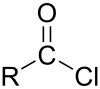
Powiązane chlorki acylowe
|
Chlorek malonylu Chlorek sukcynylu Fosgen |
||
|
Związki pokrewne
|
Kwas szczawiowy Szczawian dietylu Oksamid Hydrazyd oksalilu Kuprizon 1 |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|||
Chlorek oksalilu jest organicznym związkiem chemicznym o wzorze (COCl) 2 . Ta bezbarwna ciecz o ostrym zapachu, chlorek diacylu kwasu szczawiowego , jest użytecznym odczynnikiem w syntezie organicznej .
Przygotowanie
Chlorek oksalilu został po raz pierwszy przygotowany w 1892 roku przez francuskiego chemika Adriena Fauconniera, który poddał reakcji szczawian dietylu z pięciochlorkiem fosforu. Można go również wytworzyć przez traktowanie kwasu szczawiowego pięciochlorkiem fosforu .
Chlorek oksalilu jest produkowany komercyjnie z węglanu etylenu . Fotochlorowanie daje tetrachlorek, który następnie ulega degradacji:
- C 2 H 4 O 2 CO + 4 Cl 2 → C 2 Cl 4 O 2 CO + 4 HCl
- C 2 Cl 4 O 2 CO → C 2 O 2 Cl 2 + COCl 2
Reakcje
Chlorek oksalilu reaguje z wodą wydzielając tylko produkty gazowe: chlorowodór (HCl), dwutlenek węgla (CO 2 ) i tlenek węgla (CO).
- (COCl) 2 + H2O → 2 HCl + CO2 + CO
Pod tym względem różni się znacznie od innych chlorków acylowych , które hydrolizują z wytworzeniem chlorowodoru i pierwotnego kwasu karboksylowego .
Zastosowania w syntezie organicznej
Utlenianie alkoholi
Roztwór zawierający DMSO i chlorek oksalilu, a następnie gaszenie trietyloaminą przekształca alkohole w odpowiednie aldehydy i ketony w procesie znanym jako utlenianie Swerna .
Synteza chlorków acylowych
Chlorek oksalilu jest używany głównie razem z katalizatorem N , N -dimetyloformamidowym w syntezie organicznej do otrzymywania chlorków acylu z odpowiednich kwasów karboksylowych . Podobnie jak chlorek tionylu , w tym zastosowaniu odczynnik rozkłada się na lotne produkty uboczne, co upraszcza obróbkę. Jednym z pomniejszych produktów ubocznych N , N -dimetyloformamidem jest silny czynnik rakotwórczy, pochodzący z N , N -rozkład dimetyloformamidu. W porównaniu z chlorkiem tionylu chlorek oksalilu jest zwykle łagodniejszym, bardziej selektywnym odczynnikiem . Jest również droższy niż chlorek tionylu , dlatego jest zwykle stosowany na mniejszą skalę.
Ta reakcja polega na przekształceniu DMF w pochodną chlorku imidoilu (Me 2 N=CHCl + ), podobnie jak w pierwszym etapie reakcji Vilsmeiera-Haacka . Chlorek imidoilu jest aktywnym środkiem chlorującym.
Formylowanie arenów
Chlorek oksalilu reaguje ze związkami aromatycznymi w obecności chlorku glinu , dając odpowiedni chlorek acylu w procesie znanym jako acylowanie Friedela-Craftsa . Otrzymany chlorek acylu można hydrolizować z wytworzeniem odpowiedniego kwasu karboksylowego .
Przygotowanie diestrów szczawianu
Podobnie jak inne chlorki acylowe, chlorek oksalilu reaguje z alkoholami, dając estry:
- 2 RCH 2 OH + (COCl) 2 → RCH 2 OC(O)C(O)OCH 2R + 2 HCl
Typowo, takie reakcje prowadzi się w obecności zasady, takiej jak pirydyna . Diester pochodzący z fenolu , estru szczawianu fenylu , to Cyalume, aktywny składnik świecących sztyftów .
Inny
Podobno chlorek oksalilu był używany w pierwszej syntezie tetraketonu dioksanu (C 4 O 6 ), tlenku węgla .
Środki ostrożności
W marcu 2000 r. Airbus A330 -300 Malaysia Airlines został uszkodzony nie do naprawienia po tym, jak ładunek zakazanego chlorku oksalilu (fałszywie zadeklarowanego jako hydroksychinolina ) wyciekł do ładowni. Jest toksyczny przy wdychaniu, chociaż jest o rząd wielkości mniej toksyczny niż pokrewny związek fosgen .