Hesperydyna
|
|

|
|
| Nazwy | |
|---|---|
|
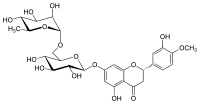
nazwa IUPAC
(2S ) -3′,5-dihydroksy-4′-metoksy-7-[α- L -ramnopiranozylo-(1→6)-β- D- glukopiranozyloksy]flawan-4-on
|
|
|
Preferowana nazwa IUPAC
(2 2 S ,4 2 S ,4 3 R ,4 4 S ,4 5 S ,4 6 R ,7 2 R ,7 3 R ,7 4 R ,7 5 R ,7 6 S )-1 3 ,2 5 ,4 3 ,4 4 ,4 5 ,7 3 ,7 4 ,7 5 -Oktahydroksy-1 4 -metoksy-7 6 -metylo-2 2 ,2 3 -dihydro-2 4 H -3,6-dioksa-2(2,7)-[1]benzopirana-4(2,6),7(2)- bis(oksana)-1(1)-benzenaheptafan-2 4 -on |
|
| Inne nazwy Hesperetyna 7-rutynozyd
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA | 100.007.536 |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C28H34O15 _ _ _ _ _ | |
| Masa cząsteczkowa | 610,565 g · mol -1 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w stanie normalnym (przy 25°C [77°F], 100 kPa).
|
|
Hesperydyna to glikozyd flawanonu występujący w owocach cytrusowych . Jej aglikonu nazywa się hesperetyną . Jego nazwa pochodzi od słowa „ hesperidium ”, oznaczającego owoce wytwarzane przez drzewa cytrusowe.
Hesperydyna została po raz pierwszy wyizolowana w 1828 roku przez francuskiego chemika M. Lebretona z białej wewnętrznej warstwy skórek owoców cytrusowych ( mezokarp , albedo).
Uważa się, że hesperydyna odgrywa rolę w obronie roślin .
Źródła
Rutaceae
- 700–2500 ppm w owocach Citrus aurantium ( gorzka pomarańcza , petitgrain )
- w soku pomarańczowym ( Citrus sinensis )
- w Zanthoxylum gilletii
- w cytrynie
- w wapnie
- w liściach Agathosma serratifolia
Jasnotowate
Mięta pieprzowa zawiera hesperydynę.
Zawartość w żywności
Orientacyjna zawartość hesperydyny na 100 ml
- 481 mg mięty pieprzowej, suszonej
- 44 mg czerwonej pomarańczy , czysty sok
- 26 mg pomarańczy , czysty sok
- 18 mg cytryny , czysty sok
- 14 mg limonki , czysty sok
- 1 mg grejpfruta , czysty sok
Metabolizm
Hesperydyna 6- O -α- L -ramnozylo-β- D -glukozydaza , enzym, który wykorzystuje hesperydynę i wodę do produkcji hesperetyny i rutynozy , występuje w gatunku Ascomycetes .
Badania
Jako flawanon występujący w skórkach owoców cytrusowych (takich jak pomarańcze lub cytryny), hesperydyna jest przedmiotem wstępnych badań pod kątem jej możliwych właściwości biologicznych in vivo . W jednym przeglądzie nie znaleziono dowodów na to, że hesperydyna wpływa na lipidów we krwi lub nadciśnienie . W innym przeglądzie stwierdzono, że hesperydyna może poprawiać funkcję śródbłonka u ludzi, ale ogólne wyniki były niejednoznaczne.
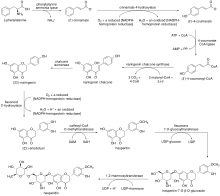
Biosynteza
Biosynteza hesperydyny zachodzi na szlaku fenylopropanoidowym , w którym naturalny aminokwas L - fenyloalanina ulega deaminacji przez liazę fenyloalaninowo-amoniakalną, dając ( E )-cynamonian . Otrzymany monokarboksylan ulega utlenieniu przez 4 -hydroksylazę cynamonianową z wytworzeniem ( E )-4-kumaranu, który jest przekształcany w ( E )-4-kumaroilo-CoA przez ligazę 4-kumaranu-CoA . ( E )-4-kumaroilo-CoA jest następnie poddawany syntazie poliketydowej typu III, syntazie chalkonowej naringeniny , przechodzącej kolejne reakcje kondensacji i ostatecznie kondensacji Claisena z zamknięciem pierścienia, z wytworzeniem chalkonu naringeniny . Odpowiedni chalkon ulega izomeryzacji przez izomerazę chalkonową , dając (2S ) -naringeninę , która jest utleniana do (2S ) -eriodiktyolu przez 3′-hydroksylaza flawonoidowa . Po O -metylacji przez O -metylotransferazę kawoilo-CoA , produkt hesperytyny ulega glikozylacji przez 7- O -glukozylotransferazę flawanonu , dając hesperytyno-7- O -β- D -glukozyd. Wreszcie, ramnozylu jest wprowadzane do monoglikozylowanego produktu przez 1,2-ramnozylotransferazę, tworząc hesperydynę.
Zobacz też
Linki zewnętrzne
-
 Media związane z hesperydyną w Wikimedia Commons
Media związane z hesperydyną w Wikimedia Commons